
- •2)Ускорение точки. Нормальное и тангенсальное кскорение. Проекции ускорения на координатные оси.
- •3) Кинематика вращательного движения. Угловая скорость и ускорение.
- •4)Динамика мат. Т-ки. Сила,масса и импульс частицы. З-ны Ньютона.
- •5) Инерциальные системы отсчета. Принцип относительности Галилея. Преобразования Галилея.
- •7)Центр инерции (масс). Движение центра инерции замкнутой с-мы.
- •8) Работа. Работа переменной силы. Мощность.
- •11)Полная механическая энергия системы. З-н сохранения механической энергии.
- •12) Вращательноe движение твердого тела. Момент инерции мат т-ки и тв тела относительно неподвижной оси. Кинетическая энергия вращающегося тв тела. Т-ма Штейнера.
- •13)Работа, совершаемая при вращении тв тела. Момент силы от-но точки и оси вращения. Осн ур-е динамики вращательного двожения тв тела.
- •14)Момент импульса мат т-ки и тв тела от-но неподвижной оси вращения. З-н сохранения импульса.
- •15)Понятие о неинерциальных системах отсчета и силах инерции
- •Скорости газовых молекул. Закон Максвелла для распределения молекул идеального газа по скоростям. Наиболее вероятная ,средняя квадратичная и средняя арифметическая скорости молекул.
- •Барометрическая формула. Распределение молекул в поле силы тяжести. Распределение Больцмана.
- •Среднее число столкновений и средняя длина свободного пробега молекул. Зависимость средней длины свободного пробега молекул от давления и температуры.
- •Явления переноса в газах.З-ны диффузии, внут трения и теплопроводности.
- •23, Число степеней свободы молекул. З-н равномерного распространения энергии по степеням свободы молекул. Внут энергия ид газа
- •Теплоемкость. Зависимость теплоемкости ид газа от вида процесса. Классическая теория теполемкости ид газа и ее ограниченность.
- •Первое начало термодинамики и изопроцессы.
- •Первое начало термодинамики и адиабатический процесс.Политропический процесс.
- •Реальные газы. Силы и потенц энергия межмолекулярного воздействия.Ур-е Ван-дер-Ваальсса.
- •Поверхностный слой жидкости.Поверхностное натяжение.Коэф пов нат и его зависимость от т-ры и примесей пав.
- •32. Явление смачивания.Краевой угол.Св-ва тонких пленок.
- •31. Давление под ихогнутой пов-тью жтдкости.Ф-ла Лапласа. Капиллярные давления.
Явления переноса в газах.З-ны диффузии, внут трения и теплопроводности.
Процесс перехода газа из неравновесного в равновесное состояние сопровождается переносом ряда физ величин(массы, импульса,кин эн),явления наз явлениями переноса:1)диффузия-явление взаимного проникновения молекул в межмолек-е пространство контактирующих газов 𝒟(коэф диф-ии)=1\3 λ𝓋 2)внутреннее трение (вязкость) обусловлено появление сил трения м\у 2мя слоями газа,движущимися с различными скоростями. Это явление объясняется переносом импульса направленного движения хаотически движущимися и взаимодействующими молекулами.η(коэф вязкости)=1\3 ρλ𝓋 3)Теплопроводность — перенос теплоты структурными частицами вещества (молекулами, атомами, электронами) в процессе их теплового движения
Внутренняя энергия системы. Работа газа при изменениях его объема. Кол-во теплоты.1начало т\д.
Внут энергия с-мы складывается из кин эн движения молекул , энергии покоя этих мол-л и потенц энергии взаимодействия м\у ними .Вн.эн с-мы яв-ся однозначной ф-ей ее состояния. Работа яв-ся количественной мерой убывания одной энергией и количественной мерой возрастания другой.A’=∆U, Q= ∆U
В общем случае работа и теплообмен могут происходить одновременно ∆U= A’+ Q, А= -A’, ∆U= -A+ Q, Q= ∆U+А- мат выражение 1н т\д. кол-во теплоты сообщенное системе идет на увеличение ее внут энергии и на совершение работы системой против внеш сил. Для бесконечно малого процесса δQ=dU+δA
23, Число степеней свободы молекул. З-н равномерного распространения энергии по степеням свободы молекул. Внут энергия ид газа
Число степней свободы-минимальное кол-во независимых величин про помощи к-х однозначно опред-ся его положение в пр-ве. Для мат т-ки=3. Благодаря трехмерности пр-ва любое вращательно движение ТВ тела можно разложить на 3 независ вращения вокруг 3 взаимно ⊥ осей,проходящих ч\з центр инерции ТВ тела. Тв тело обладает 6 степенями(3 поступательные,3 вращательные),двухатомная молекула с жесткой связью имеет 5(3 поступ,2 вращ),если связь не жесткая то добавится еще одна степень-колебательная. При взаимных сталкиваниях молекулы обмениваются энергиями поступ,вращ и колеб движений,при этом происходит превращение кин эн одного вида движения в энергию др вида движения.В результате чего происходит выравнивание средней кин энергии, приходящей на степени свободы молекул. U=imRT\2μ. Вн эн зависит от рода газа,т-ры массы, μ
Теплоемкость. Зависимость теплоемкости ид газа от вида процесса. Классическая теория теполемкости ид газа и ее ограниченность.
Теплоемкость
тела-скалярная
величина равная кол-ву тепла необходимого
для его нагревания на 1К СТ= ,
Зависит от хим состава в-ва , массы, от
т\д состояния тела.
,
Зависит от хим состава в-ва , массы, от
т\д состояния тела.
Удельная
теплоемкость-физ
величина равная кол-ву тепла необходимого
для нагревания ед массы в-ва на 1К. С=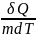 ,
применяется для однородных тел,зависит
от природы тела и от его т\д состояния.
,
применяется для однородных тел,зависит
от природы тела и от его т\д состояния.
Молярная
теплоемкость-
скал,физ величина,равная кол-ву
тепла,неоюходимого для нагревания
одного моля газа на 1К, СМ=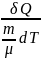 ,
зависит от усл нагревания.
,
зависит от усл нагревания.
При
V=const - СМV= R
R
При p=const- CMP= СМV +R
Ур-е Майера устанавливает связь м\у мол теплоемкостями ид газа при порт давл и объеме.
CMР= R+ R
