
- •5. Биологические функции и классификация белков.
- •6. Значение и специфичность действия ферментов.
- •7. Строение фермента.
- •8. Активный центр.
- •9. Определение активности ферментов.
- •10. Локализация ферментов в клетке, маркёрные и органоспецифические ферменты.
- •11. Механизм действия ферментов.
- •12 . Кинетика ферментативных реакций.
- •13. Регуляция активности ферментов.
- •14. Ингибирование ферментов.
- •15 . Номенклатура и классификация. Изоферменты. Изменение активности в энтогенезе.
- •15 . Энзимопатия.
- •16. Обмен веществ. Ката- и анаболизм .
- •17.Биологическое окисление.
- •18. Природа макроэргичности атф.
- •19. Цикл кребса.
- •20 . Тканевое дыхание.
- •21 . Дыхательная цепь.
- •22. Механизм сопряжения окислительного фосфорилирования.
- •23 . Термогенез.
- •24 . Микросомальная дыхательная цепь.
- •25 . Перекисное окисление и антиоксидантная защита.
- •26 . Углеводы и их переваривание.
- •1) Гиалуроновая кислота.
- •2) Кондратин – сульфат
- •3) Гепарин
- •27 . Биологические функции углеводов.
- •28 . Переваривание углеводов .
- •Галактоза
- •Фруктоза
- •29 . Пути метаболизма глюкозы.
- •30 . Синтез и распад гликогена.
- •31.Гликогенозы.
- •32 . Гликогенолиз и гликолиз.
- •33. Механизм гликолитической оксидоредукции. Субстратное фосфорилирование.
- •34 . Спиртовое брожение и метаболизм этанола.
- •34.Эробный распад глюкозы. Окислительное декарбоксилиро -
- •35. Глюконеогенез.
- •36. Гипо - и гипергликемия.
- •37.Регуляция уровня глюкозы в крови.
- •38. Сахарный диабет.
- •39. Липиды . Строение , классификация , биологическая роль .
- •40.Переваривание и всасывание липидов .
- •41. Ресинтез липидов в стенке кишечника .
- •42 . Метаболизм липидов .
- •45. Пути обмена ацетил-КоА . Обмен кетоновых тел .
- •46. Биосинтез триглицеридов.
- •47. Интеграция углеводного и липидного обмена .
- •48. Белковый обмен.
- •49. Состав желудочного сока. Механизм секреции hCl .
- •9. Ряд аминокислот, имеющих диагностическое значение .
- •50. Панкреатический сок.
- •51. Кишечный сок.
- •1.Энтерокиназа .
- •9. Фосфолипаза и липаза .
- •52 . Переваривание белков .
- •53. Гниение белков в толстом кишечнике .
- •54. Механизм всасывания аминокислот и пути их утилизации .
- •55.Трансаминирование аминокислот .
- •56. Токсичность аммиака и пути его обезвреживания .
- •57. Биосинтез мочевины .
- •58. Цикл кребса-гензеляйта .
- •59. Пути вступления аминокислот в цтк .
- •60. Декарбоксилирование аминокислот .
- •61.Метаболизм серина и глицина .
- •62. Нарушение обмена глицина .
- •63. Обмен серосодержащих аминокислот и триптофана.
- •64. Метаболизм триптофана.
- •65. Обмен фенилаланина и тирозина.
- •66. Обмен гистидина, глутамина, аспарагина, пролина.
- •67. Интеграция углеводного, белкового и липидного обмена.
- •72. Распад пуриновых нуклеотидов. Подагра.
- •73. Синтез и распад пиримидиновых оснований.
66. Обмен гистидина, глутамина, аспарагина, пролина.
Общая схема метаболизма глутамата и глутамина:
Ц







 ТК
аКГК
аКетоглутарамат
ТК
аКГК
аКетоглутарамат



 а-амино
NH3
карбомаил
кетокислоты
а-амино
NH3
карбомаил
кетокислоты

 бутират
фосфат
бутират
фосфат
аминокислоты










 N-ацетил
N-ацетил


 глутамат Глутамат
Глутамин
транспорт N2
глутамат Глутамат
Глутамин
транспорт N2







 ГАМК цис
о-про
карбомаил
ГАМК цис
о-про
карбомаил
 ГОМК
фосфат
ГОМК
фосфат
гамма-глу-амино фенилацетил

 гамма-глу-цис гли
кислота глутамин
гамма-глу-цис гли
кислота глутамин

гамма-глу-цис-гли аминокислота






с
 интез
из ГИС ПРОЛИН
интез
из ГИС ПРОЛИН
Глутаминовая кислота – сильное антитоксическое и антиоксидантное средство. Является центральным компонентом аминокислотного обмена, так как обеспечивает интеграцию белкового обмена с энергетическим (углеводным и липидным). Это осуществляется благодаря реакциям прямого и непрямого дезаминирования:
 ЦТК
ЦТК
Щ


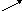

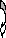
 УК
аминокислота аКГК
NH3
мочевина
УК
аминокислота аКГК
NH3
мочевина
А
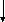
 СП
кетокислоты ГЛУ
СП
кетокислоты ГЛУ
 кетоновые тела
кетоновые тела
 фумарат глюкоза
фумарат глюкоза
мочевина
Глутамин играет роль антитоксического фактора. Это связано с тем, что при поступлении в клетку большого количества патологического материала, изменяется соотношение НАД и НАД*Н2, начинается конкуренция между субстратами за обладание НАД, в то время как концентрация НАД*Н2, возникает угроза энергетического голода тканей и дыхательная цепь переключается на ФАД-зависимое окисление именно благодаря глутамину, которая идёт на синтез эндогенного сукцинил-КоА.
Г


 ЛУ
ГАМК янтарный полуальдегид
сукцинилКоА ФАД-зависимый
ЛУ
ГАМК янтарный полуальдегид
сукцинилКоА ФАД-зависимый
COOH вход ДЦ
|
H
 OOC
– CH2
– CH2
– CH – COOH CH2
OOC
– CH2
– CH2
– CH – COOH CH2
| - CO2 |
NH2 CH2
ГЛУ |
CH2 – NH2
ГАМК
 аКГК
ГЛУ
COOH
COOH COOH
аКГК
ГЛУ
COOH
COOH COOH
. | HSKoA
|
|
| HSKoA
|
|


 CH2
CH2
CH2
ФАД (ДЦ)
CH2
CH2
CH2
ФАД (ДЦ)
| | |
CH2 CH2 CH2
| | |
H – C = O O = C – SKoA COOH
Янтарный полуальдегид сукцинилКоА сукцинат
Глутаминовая кислота является одним из немногих соединений в дополнение к глюкозе, которые служат энергетическим материалом для мозга (глутамин составляет 25% пула аминокислот мозга), поэтому в тканях мозга высока активность глутаматдекарбоксилазы:
HOOC – CH2 HOOC COOH COOH
| | | |
 CH2
а-декарбоксили
(CH2)
аКГК
ГЛУ
CH2
CH2
CH2
а-декарбоксили
(CH2)
аКГК
ГЛУ
CH2
CH2




 | рование
| |
| ДЦ
| рование
| |
| ДЦ
CH – NH2 CH2 CH CH2
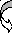 | |
| |
НАД*Н2
| |
| |
НАД*Н2
COOH NH2 O = C – H COOH
Глутамин ГАМК янтарный полуальдегид
НАД
COOH
|
CH2
|
CH2
|
ГОМК CH2OH
ГАМК и ГОМК – медиаторы торможения. Они оказывают тормозной эффект на синаптическую передачу. В общих реакциях (декарбоксилирование глутамина и трансаминирование ГАМК принимает участие ПФ, поэтому судороги, наблюдаемые при гиповитаминозе В6, связаны со снижением образования ГАМК в глутаматкарбоксилазной реакции.
Антиоксидантная активность глутамина заключается в том, что она входит в состав глутатиона. Поэтому при отравлении тяжёлыми металлами принимают глутамин во внутрь. Но ввиду слабой усвояемости чистого глутамина, его используют в качестве лекарственного препарата в виде солей (калиевой соли глутамина). Глутамин имеет вкус куриного бульона.
Метаболизм аспарагина.
Синтез аспарагина осуществляется реакцией трансаминирования:
COOH COOH COOH COOH
| | | |
CH2 (CH2) АсАТ CH2 (CH2)

 |
+ |
| + |
|
+ |
| + |
C = O CH – NH2 CH – NH2 C = O
| | | |
COOH COOH COOH COOH
ЩУК глутамин аспарагин аКГК
Аспартат утилизируется:
-
В ГНГ (глюкогенная аминокислота)
-
Синтез мочевины
-
Синтез пуринов и пиримидинов
-
Образование в-аланина или а-аланина
COOH CH3 – CH – COOH

 |
|
COOH анзерин
|
|
COOH анзерин
CH2 NH2 |

 |
CH2
|
CH2
CH – NH2 - CO2 | карнозин
| CH2 – NH2
COOH в-аланин
В-аланин входит в состав пантогеновой кислоты, идущей на синтез HS-KoA. Опухолевые ткани не способны воспроизводить аспарагин, поэтому введение аспарагиназы приводит к торможению роста опухоли.
-
Трансаминирование аспарагина даёт ЩУК
 ЩУК
сукцинат, который наполняет эндогенный
пул янтарной кислоты.
ЩУК
сукцинат, который наполняет эндогенный
пул янтарной кислоты.
-
Синтез аспарагина. Нужно отметить, что глицин и аспарагин в тканях подвергаются сочетанному трансаминированию и дезаминированию:
O O HOOC – C = O
|| || R |

 R – C – COOH + HOOC – CH – CH2
– C | +
CH2
R – C – COOH + HOOC – CH – CH2
– C | +
CH2
Кетокислота | | CH – NH2 |
NH2 NH2 | C = O
Аспсрагин COOH |
Аминокислота NH2
а-кетосукцинамовая
кислота
NH2 COOH
| |
C = O CH2
| + HOH | + NH3
C H2
C
= O
H2
C
= O
| СО-оксидаза |
C = O COOH
| ЩУК
COOH
а-кетосукцинамовая кислота
То же самое возможно и с глицином, при этом образуется а-кетоглутарамовая кислота.
-
Аспартат является нейротрансмиттером ЦНС (в виде препарата натриевой соли аспартата применяется для лечения заболеваний сердца).
Метаболизм гистидина.
Известны 3 пути метаболизма гистидина:
1.



 N
N
N
N


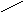
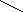




 CH2
– CH – COOH
CH2
– CH2
– NH2
CH2
– CH – COOH
CH2
– CH2
– NH2
| - CO2
NH NH2 NH гистамин
O

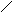

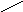
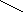

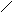




 N
+
HOH N
//
N
+
HOH N
//

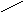
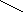

 CH2
– CH2
– NH2
NH3
+ CH2
– C + H2O2
CH2
– CH2
– NH2
NH3
+ CH2
– C + H2O2
NH диаминооксидаза NH \
альдегид гистидина H
2
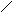

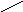
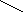 .
.
N



 CH2
– CH – COOH + H2N
– CH2
– CH2
– COOH
CH2
– CH – COOH + H2N
– CH2
– CH2
– COOH
NH | в-аланин - НОН


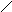

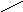
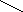 гистидин
NH2
гистидин
NH2

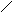
 N
N
N
N



 CH2
– CH – COOH
CH2
– CH – COOH
CH2
– CH – COOH
CH2
– CH – COOH

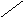


 |
|
|
|
NH NH N NH
| | |
H2N – CH2 – CH2 – C = O CH3 CO
карнозин |
анзерин (CH2)2 – NH2 Внутреннее дезаминирование:
3. 






 N
гистидинаммиаклиаза
N
N
гистидинаммиаклиаза
N



 CH2
– CH – COOH
CH
= CH – COOH
CH2
– CH – COOH
CH
= CH – COOH
NH | - NH3 NH
NH2


 имидазолилпропионат
ГЛУ
имидазолилпропионат
ГЛУ
Метаболизм пролина.
Пролин синтезируется из глутамата:
O
НАДФ*Н2 НАДФ //
H

 OOC
– CH2
– CH2
– CH – COOH HOOC – CH2
– (CH2)
– C
OOC
– CH2
– CH2
– CH – COOH HOOC – CH2
– (CH2)
– C
- НОН гамма-полуальдегид \



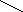 H
H
г
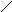
 лутаматдегидрогеназа
лутаматдегидрогеназа


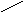
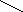
 COOH
O = COOH
COOH
O = COOH


 - НОН
NH
пролиноксидаза
NH
- НОН
NH
пролиноксидаза
NH
пролин 5-оксопролин
оксипролиназа COOH COOH


 O = COOH
| | GSH
O = COOH
| | GSH
 NH
CH2
– CH2
– CH – NH2
NH
CH2
– CH2
– CH – NH2
5-оксопролин АТФ АДФ+Фн глутамат
