
- •Липиды, определение.
- •К лассификация липидов по происхождению, химическому составу и функциям.
- •Важнейшие жиры тканей человека. Резервные и структурные липиды.
- •Биологическая роль липидов в процессах жизнедеятельности.
- •Триацилглицерины тканей человека, строение, биологическая роль.
- •Жирные кислоты, предельные и непредельные, характерные для триацилглицеринов человека. Особенности строения, ω3-и ω6- жирные кислоты, и их биологическая роль.
- •Транспорт жирных кислот альбуминами крови.
- •Основные фосфолипиды тканей человека, строение, функции.
- •Гликолипиды тканей человека, особенности строения, функции.
- •Переваривание нейтрального жира в желудочно-кишечном тракте. Липазы и их роль. Факторы, влияющие на степень гидролиза нейтрального жира.
- •Переваривание фосфолипидов и стероидов в желудочно-кишечном тракте. Ферменты, роль.
- •Всасывание продуктов переваривания липидов.
- •Желчные кислоты, строение, роль в переваривании и всасывании липидов.
- •Ресинтез триацилглицеринов в энтероцитах. Ресинтез фосфолипидов.
- •Образование хиломикронов и транспорт жиров.
- •Л ипопротеинлипаза, ее роль.
- •Обмен нейтрального жира. Резервирование и мобилизация жиров в жировой ткани.
- •Регуляция процессов мобилизации и резервирования нейтрального жира, , физиологическое значение процессов. Нарушение при ожирении.
- •Р оль адреналина и глюкагона
- •Липопротеины как транспортная форма липидов. Типы, состав и строение липопротеинов крови, взаимопревращения липопротеинов.
- •Катаболизм липидов, биологическое значение.
- •Биосинтез жирных кислот, химизм, ферменты.
- •Биосинтез жирных кислот с длинной цепью углеродных атомов и непредельных.
- •Кетоновые тела, биосинтез и использование, физиологическое значение процессов.
- •Биосинтез фосфолипидов в тканях, химизм, физиологическое значение.
- •Холестерин, строение, биосинтез, судьба в организме.
- •В ыведение холестерина и жёлчных кислот из организма.
- •Нормальный уровень холестерина в крови. Гиперхолестеринемия и ее причины.
- •Биохимия атеросклероза и жёлчнокаменной болезни, факторы риска.
- •Биохимические основы профилактики и лечения атеросклероза.
- •Биосинтез фосфолипидов
- •Биосинтез и катаболизм сфинголипидов
- •Нарушения обмена сфинголипидов. Сфинголипидозы.
- •Принцип и химизм количественного определения общего холестерина крови, диагностическое значение.
- •Принцип и химизм количественного определения β-липопротеинов крови. Диагностическое значение.
Биосинтез фосфолипидов в тканях, химизм, физиологическое значение.
Синтез фосфолипидов может происходить в различных тканях и по нескольким путям: в кишечнике с использованием пищевого холина или этаноламина (ресинтез фосфолипидов) и в печени (собственно биосинтез)
С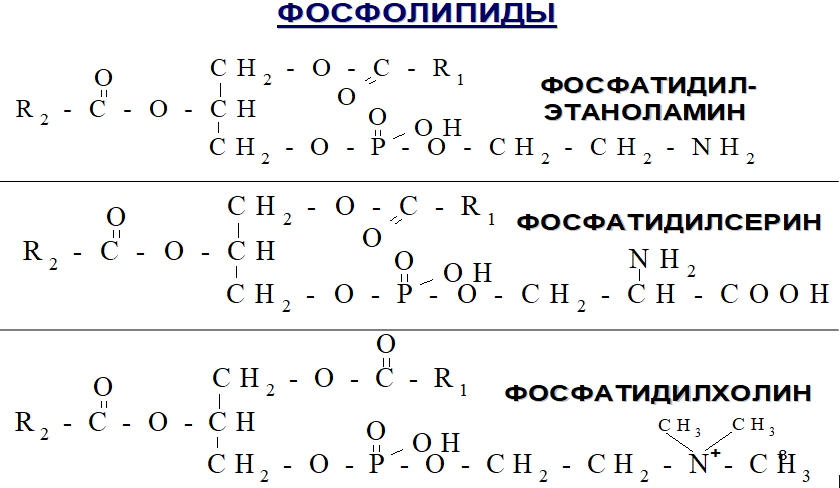 интез
фосфатидилхолинов, фосфатидилэтаноламинов
и фосфатидилсеринов.
Начальные
этапы синтеза глицерофосфолипидов и
жиров происходят одинаково до образования
фосфатидной кислоты. Фосфатидная кислота
может синтезироваться двумя разными
путями: через глицеральдегид-3-фосфат
и через дигидроксиацетонфосфат
интез
фосфатидилхолинов, фосфатидилэтаноламинов
и фосфатидилсеринов.
Начальные
этапы синтеза глицерофосфолипидов и
жиров происходят одинаково до образования
фосфатидной кислоты. Фосфатидная кислота
может синтезироваться двумя разными
путями: через глицеральдегид-3-фосфат
и через дигидроксиацетонфосфат
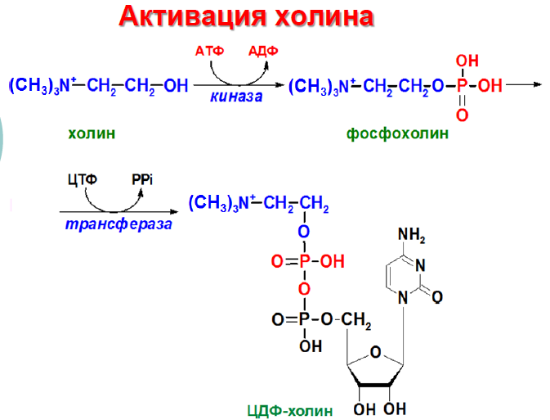
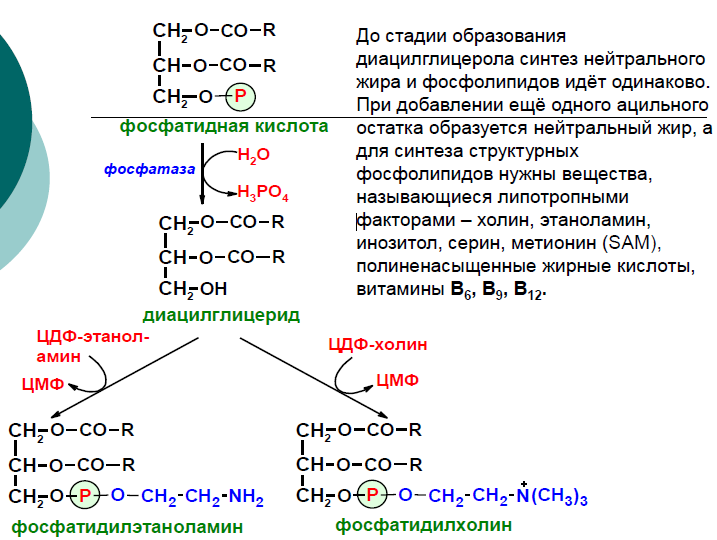
Н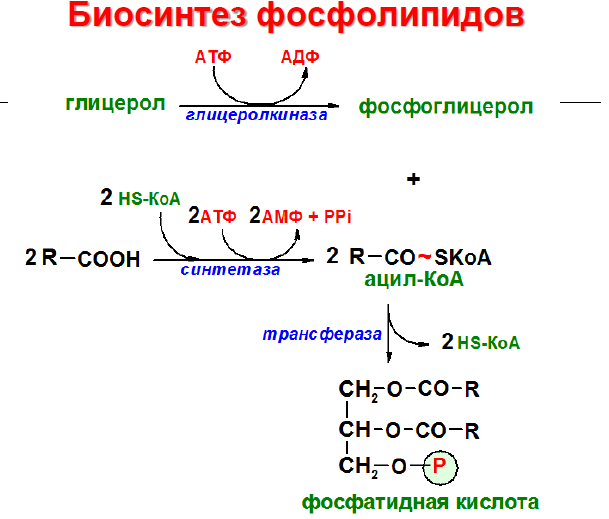 а
следующем этапе фосфатидаза отщепляет
от фосфатидной кислоты фосфатный
остаток, в результате чего образуется
диацилглицерол. Дальнейшие превращения
диацилглицерола также могут идти разными
путями. Один из вариантов - образование
активной формы "полярной головки"
фосфолипида: холин, серии или этаноламин
превращаются в ЦДФ-холин, ЦДФ-серин или
ЦДФ-этаноламин. Далее диацилглицерол
взаимодействует с ЦМФ-производными,
при этом выделяется ЦМФ, и образуется
соответствующий фосфолигид, например,
фосфатидилхолин. Между глицерофосфолипидами
возможны различные взаимопревращения.
Фосфатидилхолин может образовываться
и другим путём: из фосфатидилэтаноламина,
получая последовательно 3 метальные
группы от SAM. Фосфатидилсерин может
превращаться в фосфатидилэтаноламин
путём декарбоксилирования.
Фосфатидилэтаноламин может превращаться
в фосфатидилсерин путём обмена этаноламина
на серии.
а
следующем этапе фосфатидаза отщепляет
от фосфатидной кислоты фосфатный
остаток, в результате чего образуется
диацилглицерол. Дальнейшие превращения
диацилглицерола также могут идти разными
путями. Один из вариантов - образование
активной формы "полярной головки"
фосфолипида: холин, серии или этаноламин
превращаются в ЦДФ-холин, ЦДФ-серин или
ЦДФ-этаноламин. Далее диацилглицерол
взаимодействует с ЦМФ-производными,
при этом выделяется ЦМФ, и образуется
соответствующий фосфолигид, например,
фосфатидилхолин. Между глицерофосфолипидами
возможны различные взаимопревращения.
Фосфатидилхолин может образовываться
и другим путём: из фосфатидилэтаноламина,
получая последовательно 3 метальные
группы от SAM. Фосфатидилсерин может
превращаться в фосфатидилэтаноламин
путём декарбоксилирования.
Фосфатидилэтаноламин может превращаться
в фосфатидилсерин путём обмена этаноламина
на серии.
Б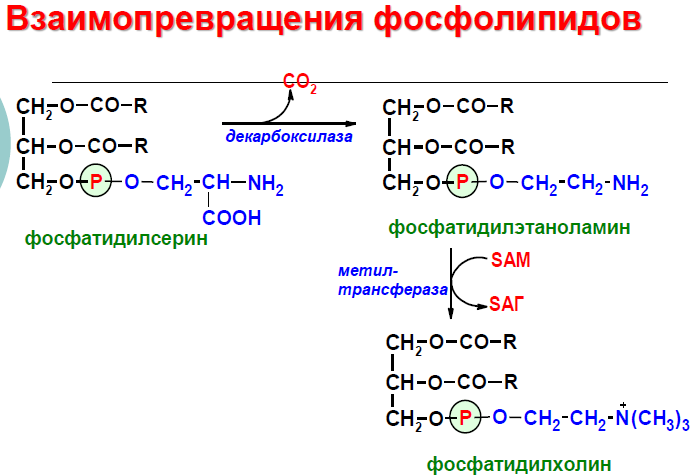 иологическая
роль.
иологическая
роль.
Входят в состав мембран, участвуя в их избирательной проницаемости.
Дипальмитоилфосфатидилхолин (до 80%), является компонентом сурфактанта, выстилающего альвеолы легких и препятствующей слипанию стенок альвеол во время вдоха.
Фосфатидилэтаноламин и фосфатидилхолин мембран взаимодействует с ферментами, образуя комплексы, которые активируют факторы свертывания крови. Фосфатидилсерин активирует процессы фибринолиза, связываясь с другими ферментами.
Обладают липотропным действием, препятствуя отложению нейтрального жира в печени.
Продукты их распада участвуют в патогенезе бронхиальной астмы, атеросклероза.
Фосфатидилсерин влияет на освобождение гистамина.
Холестерин, строение, биосинтез, судьба в организме.
Х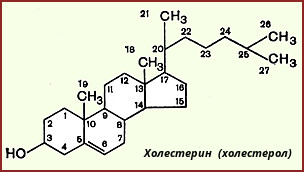
 олестерол
- стероид, характерный только для животных
организмов. Он синтезируется во многих
тканях человека, но основное место
синтеза - печень. В печени синтезируется
более 50% холестерола, в тонком кишечнике
- 15-20%, остальной холестерол синтезируется
в коже, коре надпочечников, половых
железах. В сутки в организме синтезируется
около 1 г холестерола; с пищей поступает
300-500 мг. Холестерол выполняет много
функций: входит в состав всех мембран
клеток и влияет на их свойства, служит
исходным субстратом в синтезе жёлчных
кислот и стероидных гормонов.
Предшественники в метаболическом пути
синтеза холестерола превращаются также
в убихинон - компонент дыхательной цепи
и долихол, участвующий в синтезе
гликопротеинов.
олестерол
- стероид, характерный только для животных
организмов. Он синтезируется во многих
тканях человека, но основное место
синтеза - печень. В печени синтезируется
более 50% холестерола, в тонком кишечнике
- 15-20%, остальной холестерол синтезируется
в коже, коре надпочечников, половых
железах. В сутки в организме синтезируется
около 1 г холестерола; с пищей поступает
300-500 мг. Холестерол выполняет много
функций: входит в состав всех мембран
клеток и влияет на их свойства, служит
исходным субстратом в синтезе жёлчных
кислот и стероидных гормонов.
Предшественники в метаболическом пути
синтеза холестерола превращаются также
в убихинон - компонент дыхательной цепи
и долихол, участвующий в синтезе
гликопротеинов.
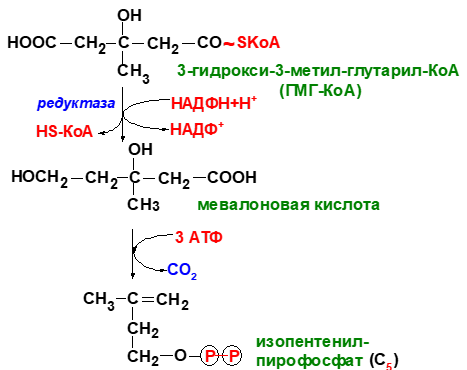
Биосинтез холестерина
1 стадия – синтез мевалоновой кислоты
2 стадия – конденсация
3 стадия - циклизация
Регуляция ключевого фермента синтеза хо-лестерола (ГМГ-КоА-редуктазы) происходит разными способами.
Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы
П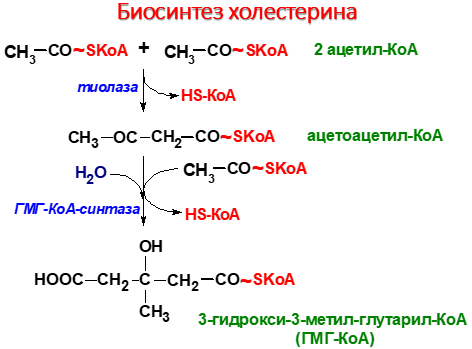
 ри
увеличении соотношения инсулин/глюкагон
этот фермент дефосфорилируется и
переходит в активное состояние. Действие
инсулина осуществляется через 2
фермента: фосфатазу
киназы ГМГ-КоА-редуктазы, которая
превращает киназу в неактивное
дефосфо-рилированное состояние; фосфатазу
ГМГ-КоА-редуктазыпутём
превращения её в дефосфорилированное
активное состояние. Результатом этих
реакций служит образование
дефосфорилированной активной формы
ГМГ-КоА-редуктазы. Следовательно, в
абсорбтивный период синтез холестерола
увеличивается. В этот период увеличивается
и доступность исходного субстрата для
синтеза холестерола - ацетил-КоА (в
результате приёма пищи, содержащей
углеводы, так как ацетил-КоА образуется
в основном при распаде глюкозы). В
постабсорбтивном состоянии глюкагон
через протеинкиназу А стимулирует
фосфо-рилирование ГМГ-КоА-редуктазы,
переводя её в неактивное состояние. Это
действие усиливается тем, что одновременно
глюкагон стимулирует фосфорилирование
и инактивацию фосфатазы ГМГ-КоА-редук-тазы
и фосфорилирование киназы ГМГ-КоА-редуктазы,
удерживая, таким образом, ГМГ-КоАредуктазу
в фосфорилированном неактивном состоянии.
В результате синтез холестерола в
постабсорбтивном периоде и при голодании
ингибируется. Ингибирование
синтеза ГМГ-КоА-редуктазы. Конечный
продукт метаболического пути (холестерол)
снижает скорость транскрипции гена
ГМГ-КоА-редуктазы, подавляя таким образом
собственный синтез. В печени активно
идёт синтез жёлчных кислот из холестерола,
поэтому и жёлчные кислоты (как конечные
продукты синтеза) подавляют активность
гена ГМГ-КоА-редуктазы. Так как молекула
ГМГ-КоА-редук-тазы существует около 3 ч
после синтеза, то ингибирование синтеза
этого фермента
ри
увеличении соотношения инсулин/глюкагон
этот фермент дефосфорилируется и
переходит в активное состояние. Действие
инсулина осуществляется через 2
фермента: фосфатазу
киназы ГМГ-КоА-редуктазы, которая
превращает киназу в неактивное
дефосфо-рилированное состояние; фосфатазу
ГМГ-КоА-редуктазыпутём
превращения её в дефосфорилированное
активное состояние. Результатом этих
реакций служит образование
дефосфорилированной активной формы
ГМГ-КоА-редуктазы. Следовательно, в
абсорбтивный период синтез холестерола
увеличивается. В этот период увеличивается
и доступность исходного субстрата для
синтеза холестерола - ацетил-КоА (в
результате приёма пищи, содержащей
углеводы, так как ацетил-КоА образуется
в основном при распаде глюкозы). В
постабсорбтивном состоянии глюкагон
через протеинкиназу А стимулирует
фосфо-рилирование ГМГ-КоА-редуктазы,
переводя её в неактивное состояние. Это
действие усиливается тем, что одновременно
глюкагон стимулирует фосфорилирование
и инактивацию фосфатазы ГМГ-КоА-редук-тазы
и фосфорилирование киназы ГМГ-КоА-редуктазы,
удерживая, таким образом, ГМГ-КоАредуктазу
в фосфорилированном неактивном состоянии.
В результате синтез холестерола в
постабсорбтивном периоде и при голодании
ингибируется. Ингибирование
синтеза ГМГ-КоА-редуктазы. Конечный
продукт метаболического пути (холестерол)
снижает скорость транскрипции гена
ГМГ-КоА-редуктазы, подавляя таким образом
собственный синтез. В печени активно
идёт синтез жёлчных кислот из холестерола,
поэтому и жёлчные кислоты (как конечные
продукты синтеза) подавляют активность
гена ГМГ-КоА-редуктазы. Так как молекула
ГМГ-КоА-редук-тазы существует около 3 ч
после синтеза, то ингибирование синтеза
этого фермента
