
- •IV. Построение кинетической модели и нахождение активационных параметров для каталитической составляющей исследуемой реакции (опыты 25-41)…………………………..52
- •I. Условия задания.
- •III. Предварительные эксперименты (опыты 1-8).
- •III. Построение кинетической модели и нахождение активационных параметров для каталитической составляющей исследуемой реакции (опыты 10-24).
- •IV. Построение кинетической модели и нахождение активационных параметров для каталитической составляющей исследуемой реакции (опыты 25-41).
III. Построение кинетической модели и нахождение активационных параметров для каталитической составляющей исследуемой реакции (опыты 10-24).
Так как при малых концентрациях реагента В СВ в данной реакционной системе в сравнении с концентрациями других реагентов - А и Y влияние автокаталитической составляющей исследуемой реакции на её ход является пренебрежительно малым, то мы можем этим воспользоваться и найти порядки каталитической составляющей реакции по реагентам А, Y и катализатору К nA, nY и nK соответственно с помощью интегрального метода.
Сначала мы определяем порядок каталитической составляющей данной реакции по исходному реагенту Y, так как, согласно условиям данного задания, мы можем создать большой избыток другого исходного реагента - реагента А над реагентом Y (при этих условиях начальная концентрация реагента А в реакционной системе СА0 много больше, чем
начальная концентрация реагента Y в реакционной системе СY0).
Опыты 10-14. Определение критерия воспроизводимости для концентрации реагента Y CY для основных экспериментов по исследованию каталитической составляющей данной реакции.
Условия опытов 10-14: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 100ºC.
Результаты опыта 10:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
9,0309·10-2 |
3 |
0,2 |
7,8943·10-2 |
4 |
0,3 |
7,0404·10-2 |
5 |
0,4 |
6,4649·10-2 |
6 |
0,5 |
5,5728·10-2 |
7 |
0,6 |
5,0533·10-2 |
8 |
0,7 |
4,3417·10-2 |
9 |
0,8 |
3,9686·10-2 |
10 |
0,9 |
3,53·10-2 |
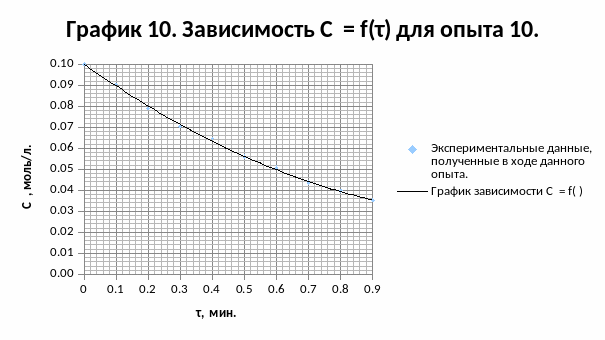
Результаты опыта 11:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
8,7651·10-2 |
3 |
0,2 |
7,8655·10-2 |
4 |
0,3 |
7,0698·10-2 |
5 |
0,4 |
6,3792·10-2 |
6 |
0,5 |
5,6644·10-2 |
7 |
0,6 |
4,9745·10-2 |
8 |
0,7 |
4,6831·10-2 |
9 |
0,8 |
3,9774·10-2 |
10 |
0,9 |
3,5206·10-2 |
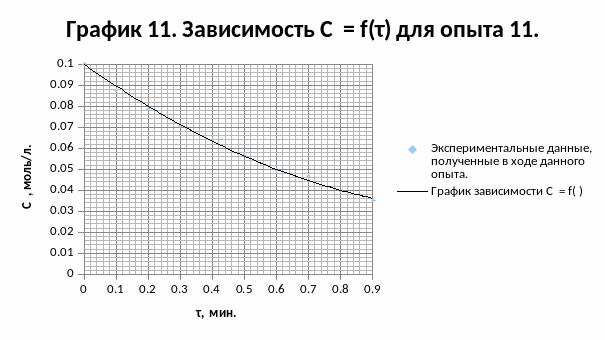
Результаты опыта 12:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
8,7440·10-2 |
3 |
0,2 |
7,7704·10-2 |
4 |
0,3 |
7,0016·10-2 |
5 |
0,4 |
6,24·10-2 |
6 |
0,5 |
5,7876·10-2 |
7 |
0,6 |
4,8464·10-2 |
8 |
0,7 |
4,5105·10-2 |
9 |
0,8 |
4,0678·10-2 |
10 |
0,9 |
3,6067·10-2 |
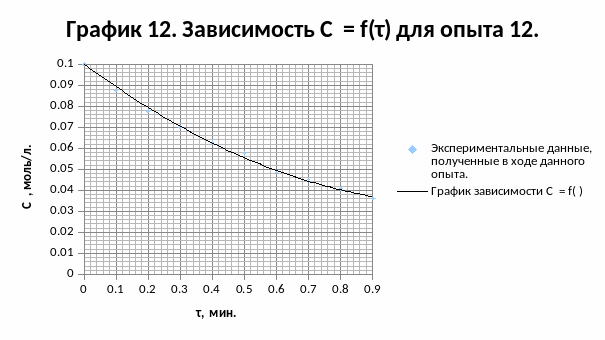
Результаты опыта 13:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
9,1634·10-2 |
3 |
0,2 |
8,2966·10-2 |
4 |
0,3 |
7,1369·10-2 |
5 |
0,4 |
6,375·10-2 |
6 |
0,5 |
5,7357·10-2 |
7 |
0,6 |
5,1613·10-2 |
8 |
0,7 |
4,4343·10-2 |
9 |
0,8 |
3,9202·10-2 |
10 |
0,9 |
3,6185·10-2 |

Результаты опыта 14:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
8,7953·10-2 |
3 |
0,2 |
7,7689·10-2 |
4 |
0,3 |
7,4141·10-2 |
5 |
0,4 |
6,3812·10-2 |
6 |
0,5 |
5,6967·10-2 |
7 |
0,6 |
4,9756·10-2 |
8 |
0,7 |
4,4814·10-2 |
9 |
0,8 |
4,1024·10-2 |
10 |
0,9 |
3,5368·10-2 |

Находим критерий воспроизводимости S2воспр. CY’ для данного параметра (концентрации СY) для основных экспериментов по исследованию каталитической составляющей данной реакции при τ = 0,9 мин. по формуле:
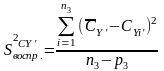 ,
где СY’
- среднее арифметическое из n1
значений концентрации реагента Y
для основных экспериментов по исследованию
каталитической составляющей данной
реакции CY’,
i
- номер данного измерения из n3
измерений (в нашем случае n3
= 5),
,
где СY’
- среднее арифметическое из n1
значений концентрации реагента Y
для основных экспериментов по исследованию
каталитической составляющей данной
реакции CY’,
i
- номер данного измерения из n3
измерений (в нашем случае n3
= 5),
p3 - число параметров для данной величины данной серии измерений (в нашем случае р3 = 1),
 .
.
CY’ = (3,53+3,5206+3,6067+3,6185+3,5368)·10-2/5 = 3,5625·10-2 моль/л.
Показатели |
Опыт 10 |
Опыт 11 |
Опыт 12 |
Опыт 13 |
Опыт 14 |
СY’, моль/л. |
3,53·10-2 |
3,5206·10-2 |
3,6067·10-2 |
3,6185·10-2 |
3,5368·10-2 |
СY’-СYi’, моль/л. |
3,252·10-4 |
4,192·10-4 |
-4,418·10-4 |
-5,598·10-4 |
2,572·10-4 |
(СY’-СYi’)2, моль2/л2. |
1,05755·10-7 |
1,75729·10-7 |
1,95187·10-7 |
3,13376·10-7 |
6,61518·10-8 |
S2воспр. CY’ = 2,1405·10-7 моль2/л2.
Выводы: После проведения данных опытов мы определили значение критерия воспроизводимости S2воспр. CY’ для данного параметра (концентрации СY) для основных экспериментов по исследованию каталитической составляющей данной реакции.
Опыты 15, 16. Определение порядка каталитической составляющей исследуемой реакции по реагенту Y.
Условия опыта 15: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,3 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,3 |
2 |
0,1 |
0,2698 |
3 |
0,2 |
0,2381 |
4 |
0,3 |
0,2118 |
5 |
0,4 |
0,1856 |
6 |
0,5 |
0,1697 |
7 |
0,6 |
0,1457 |
8 |
0,7 |
0,1334 |
9 |
0,8 |
0,1193 |
10 |
0,9 |
0,1026 |
Условия опыта 16: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,5 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,5 |
2 |
0,1 |
0,4348 |
3 |
0,2 |
0,3963 |
4 |
0,3 |
0,3465 |
5 |
0,4 |
0,3205 |
6 |
0,5 |
0,2773 |
7 |
0,6 |
0,2533 |
8 |
0,7 |
0,2261 |
9 |
0,8 |
0,1936 |
10 |
0,9 |
0,1722 |
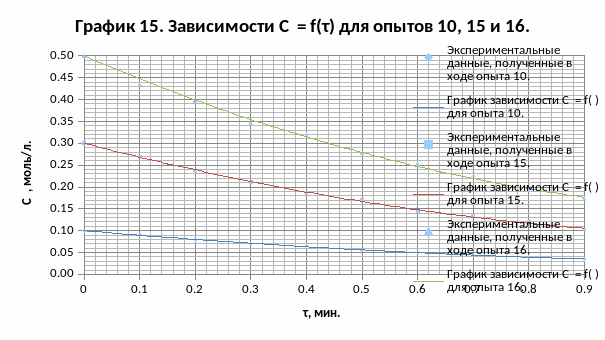
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту Y nY, равный 1.
Строим графики зависимостей ln(СY) = f(τ) для опытов 10, 15 и 16:
Время, прошедшее после начала опыта τ, мин. |
ln(СY). |
||
Опыт 10 |
Опыт 15 |
Опыт 16 |
|
0 |
-2,302585093 |
-1,20397 |
-0,69314718 |
0,1 |
-2,404518156 |
-1,31007 |
-0,83286912 |
0,2 |
-2,539029206 |
-1,43506 |
-0,92558378 |
0,3 |
-2,653505199 |
-1,55211 |
-1,05987246 |
0,4 |
-2,738782642 |
-1,68416 |
-1,137873 |
0,5 |
-2,887272565 |
-1,77372 |
-1,28265533 |
0,6 |
-2,985128691 |
-1,92621 |
-1,37318072 |
0,7 |
-3,13690421 |
-2,0144 |
-1,4867779 |
0,8 |
-3,226756798 |
-2,12611 |
-1,6419611 |
0,9 |
-3,343872315 |
-2,27692 |
-1,75909869 |

При nY = 1 эффективная константа скорости каталитической составляющей реакции Кэф.К равна по формуле: Кэф.К = -tg α (угол наклона графика зависимости ln(СY) = f(τ)).
tg α10= -1,1578 1/мин;
tg α15= -1,1727 1/мин;
tg α16= -1,1667 1/мин.
Кэф.K 10 = 1,1578 1/мин;
Кэф.K 15 = 1,1727 1/мин;
Кэф K 16 = 1,1667 1/мин.
Доказываем эту гипотезу.
Находим критерий адекватности Sад. СY’2 для данного параметра для основных измерений
по исследованию каталитической составляющей данной реакции (концентрации СY) по формуле:
 ,
где СYi’;.теор
- значения СY
для опыта 10, найденные по формуле:
СYi’;.теор
= CY0·e-Кэф.К
10·τ,
СYi;.эксп
- экспериментальные значения СY
для опыта 10,
,
где СYi’;.теор
- значения СY
для опыта 10, найденные по формуле:
СYi’;.теор
= CY0·e-Кэф.К
10·τ,
СYi;.эксп
- экспериментальные значения СY
для опыта 10,
i - номер данного измерения из n4 измерений (в нашем случае n4 = 10), p4 - число параметров для данной величины данной серии измерений (в нашем случае р4 = 2).
Время, прошедшее после начала опыта τ, мин. |
СYi;.теор, моль/л |
СYi;.эксп, моль/л |
0 |
0,1 |
0,1 |
0,1 |
0,089067115 |
0,090309 |
0,2 |
0,07932951 |
0,078943 |
0,3 |
0,070656506 |
0,070404 |
0,4 |
0,062931711 |
0,064649 |
0,5 |
0,056051459 |
0,055728 |
0,6 |
0,049923418 |
0,050533 |
0,7 |
0,044465348 |
0,043417 |
0,8 |
0,039604002 |
0,039686 |
0,9 |
0,035274142 |
0,0353 |
S2ад. СY’ = 7,8589·10-7 моль2/л2.
Проверяем адекватность данной гипотезы, рассчитав критерий Фишера Fоп СY’ по формуле:
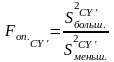 ,
где S2больш.
СY’
- больший критерий для величины СY’,
S2меньш
.СY’
-
меньший критерий для величины СY’,
,
где S2больш.
СY’
- больший критерий для величины СY’,
S2меньш
.СY’
-
меньший критерий для величины СY’,
и сравнив его с табличным значением, взятым из [1].
Так как S2ад. СY’ > S2воспр CY’, то:
Fоп. СY’= 7,8589·10-7/ 2,1405·10-7 = 3,6715.
При fСY’.1 = faд. СY’ = nад. СY’ - pад. СY’ = 10 - 2 = 8, fСY’.1 = fвоспр. СY’ = nвоспр .СY’ - pвоспр. СY’ = 5 - 1 = 4, и α = 0,01:
Fтабл. СY’ = 14,8.
Так как Fтабл. СY’ > Fоп. СY’, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту Y, равный 1, верна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту Y nY, равный 0,5.
Строим графики зависимостей (СY0,5) = f(τ) для опытов 10, 15 и 16:
Время, прошедшее после начала опыта τ, мин. |
(СY0,5), (моль/л)0,5. |
||
Опыт 10 |
Опыт 15 |
Опыт 16 |
|
0 |
0,316227766 |
0,547723 |
0,707106781 |
0,1 |
0,300514559 |
0,519423 |
0,659393661 |
0,2 |
0,28096797 |
0,487955 |
0,629523629 |
0,3 |
0,265337521 |
0,460217 |
0,588642506 |
0,4 |
0,254261676 |
0,430813 |
0,566127194 |
0,5 |
0,236067787 |
0,411947 |
0,526592822 |
0,6 |
0,224795463 |
0,381707 |
0,503289181 |
0,7 |
0,208367464 |
0,36524 |
0,475499737 |
0,8 |
0,199213453 |
0,345398 |
0,44 |
0,9 |
0,187882942 |
0,320312 |
0,414969878 |
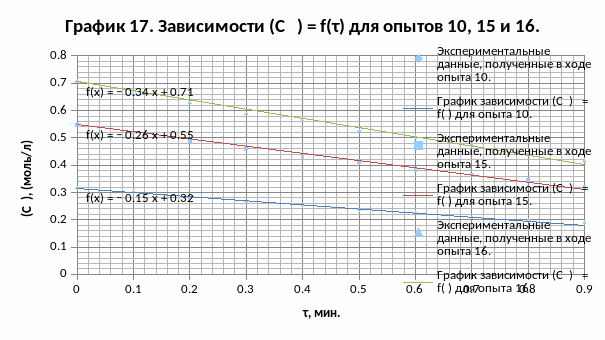
При nY = 0,5 эффективная константа скорости каталитической составляющей реакции Кэф.К’ равна по формуле: Кэф.К’ = -2tg β (угол наклона графика зависимости (СY0,5) = f(τ)).
tg β10 = -0,1503 моль0,5/(л0,5·мин);
tg β15 = -0,2630 моль0,5/(л0,5·мин);
tg β16= -0,3381 моль0,5/(л0,5·мин).
Кэф.K 10’ = 2·0,1503 = 0,3006 моль0,5/(л0,5·мин);
Кэф.К 15’ = 2·0,263 = 0,526 моль0,5/(л0,5·мин);
Кэф.К 16’ = 2·0,3381 = 0,6762 моль0,5/(л0,5·мин).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. СY’ для данного параметра (концентрации СY) для основных измерений по исследованию каталитической составляющей данной реакции по формуле:
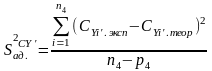 ,
где СYi’.теор
- значения СY
для опыта 10, найденные по формуле:
СYi’.теор
= (CY00,5
– 0,5Кэф.К
10’·τ)2
, i
- номер данного измерения из n4
измерений (в нашем случае n4
= 10), p4
- число параметров для данной величины
данной серии измерений (в нашем случае
р4
= 2).
,
где СYi’.теор
- значения СY
для опыта 10, найденные по формуле:
СYi’.теор
= (CY00,5
– 0,5Кэф.К
10’·τ)2
, i
- номер данного измерения из n4
измерений (в нашем случае n4
= 10), p4
- число параметров для данной величины
данной серии измерений (в нашем случае
р4
= 2).
Время, прошедшее после начала опыта τ, мин. |
СYi.теор, моль/л |
СYi.эксп, моль/л |
0 |
0,1 |
0,1 |
0,1 |
0,090720094 |
0,090309 |
0,2 |
0,08189199 |
0,078943 |
0,3 |
0,073515688 |
0,070404 |
0,4 |
0,065591188 |
0,064649 |
0,5 |
0,058118489 |
0,055728 |
0,6 |
0,051097593 |
0,050533 |
0,7 |
0,044528498 |
0,043417 |
0,8 |
0,038411204 |
0,039686 |
0,9 |
0,032745713 |
0,0353 |
S2ад. СY’ = 4,3567·10-6 моль2/л2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп СY’ и сравнив его с табличным значением, взятым из [1].
Так как S2ад. СY’ > S2воспр CY’, то:
Fоп .СY = 4,3567·10-6/2,1405·10-7 = 20,35.
При fСY’.1 = faд. СY’ = nад. СY’ - pад. СY’ = 10 - 2 = 8, fСY’.1 = fвоспр. СY’ = nвоспр .СY’ - pвоспр. СY’ = 5 - 1 = 4, и α = 0,01:
Fтабл. СY’ = 14,8.
Так как Fтабл. СY’ < Fоп. СY’, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту Y, равный 0,5, неверна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту Y nY, равный 1,5.
Строим графики зависимостей 1/(СY)0,5 = f(τ) для опытов 10, 15 и 16:
Время, прошедшее после начала опыта τ, мин. |
1/(СY0,5), (л/моль)0,5. |
||
Опыт 10 |
Опыт 15 |
Опыт 16 |
|
0 |
3,16227766 |
1,8257419 |
1,414213562 |
10 |
3,327625804 |
1,9252141 |
1,516544758 |
20 |
3,559124554 |
2,0493697 |
1,588502724 |
30 |
3,768784741 |
2,1728864 |
1,698823971 |
40 |
3,932956059 |
2,3211917 |
1,766387501 |
50 |
4,236071398 |
2,4274991 |
1,899000439 |
60 |
4,448488366 |
2,6198126 |
1,986929259 |
70 |
4,799213761 |
2,7379284 |
2,103050584 |
80 |
5,019741303 |
2,8952081 |
2,272727273 |
90 |
5,322462954 |
3,1219527 |
2,409813464 |

При nY = 1,5 эффективная константа скорости каталитической составляющей реакции Кэф.К” равна по формуле: Кэф.К” = 2tg γ (угол наклона графика зависимости 1/(СY0,5) = f(τ)).
tg γ10 = 2,2704 л0,5/(моль0,5·мин);
tg γ15 = 1,3316 л0,5/(моль0,5·мин);
tg γ16 = 1,0254 л0,5/(моль0,5·мин).
Кэф.K 10” = 2·2,2704 = 4,5408 л0,5/(моль0,5·мин);
Кэф.К 15” = 2·1,3316 = 2,6632 л0,5/(моль0,5·мин);
Кэф.К 17” = 2·1,0254 = 2,0508 л0,5/(моль0,5·мин).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. СY’ для данного параметра (концентрации СY) для основных измерений по исследованию каталитической составляющей данной реакции по формуле:
, где СYi’.теор - значения СY для опыта 10, найденные по формуле: СYi’.теор = 1/(1/CY00,5 + 0,5Кэф.К 10”·τ)2, i - номер данного измерения из n4 измерений (в нашем случае n4 = 10), p4 - число параметров для данной величины данной серии измерений (в нашем случае р4 = 2).
Время, прошедшее после начала опыта τ, мин. |
СYi.теор, моль/л |
СYi.эксп, моль/л |
0 |
0,1 |
0,1 |
0,1 |
0,09318926 |
0,090309 |
0,2 |
0,087051338 |
0,078943 |
0,3 |
0,081500445 |
0,070404 |
0,4 |
0,076464041 |
0,064649 |
0,5 |
0,071880456 |
0,055728 |
0,6 |
0,06769699 |
0,050533 |
0,7 |
0,063868391 |
0,043417 |
0,8 |
0,06035563 |
0,039686 |
0,9 |
0,057124898 |
0,0353 |
S2ад. СY’ = 2,7676·10-4 моль2/л2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп СY’ и сравнив его с табличным значением, взятым из [1].
Так как S2ад. СY’ > S2воспр CY’, то:
Fоп .СY = 2,7676·10-4/2,1405·10-7 = 1293.
При fСY’.1 = faд. СY’ = nад. СY’ - pад. СY’ = 10 - 2 = 8, fСY’.1 = fвоспр. СY’ = nвоспр .СY’ - pвоспр. СY’ = 5 - 1 = 4, и α = 0,01:
Fтабл. СY’ = 14,8.
Так как Fтабл. СY’ < Fоп. СY’, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту Y, равный 1,5, неверна.
Выводы: После проведения данных опытов мы установили, что порядок каталитической составляющей данной реакции по реагенту Y nY равен 1 и мы можем использовать этот факт при постановке последующих опытов и обработке полученных при этом данных.
Опыты 17, 18. Определение порядка каталитической составляющей исследуемой реакции по реагенту А.
Условия опыта 17: Начальная концентрация реагента А CA0 = 1 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,6 |
8,7234·10-2 |
3 |
1,2 |
7,4403·10-2 |
4 |
1,8 |
6,6393·10-2 |
5 |
2,4 |
5,8625·10-2 |
6 |
3 |
5,0587·10-2 |
7 |
3,6 |
4,3959·10-2 |
8 |
4,2 |
3,6535·10-2 |
9 |
4,8 |
3,2153·10-2 |
10 |
5,4 |
2,8181·10-2 |
Условия опыта 18: Начальная концентрация реагента А CA0 = 3 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,2 |
8,5807·10-2 |
3 |
0,4 |
7,7097·10-2 |
4 |
0,6 |
6,7508·10-2 |
5 |
0,8 |
5,8367·10-2 |
6 |
1 |
5,0487·10-2 |
7 |
1,2 |
4,3802·10-2 |
8 |
1,4 |
3,7436·10-2 |
9 |
1,6 |
3,2571·10-2 |
10 |
1,8 |
2,9384·10-2 |
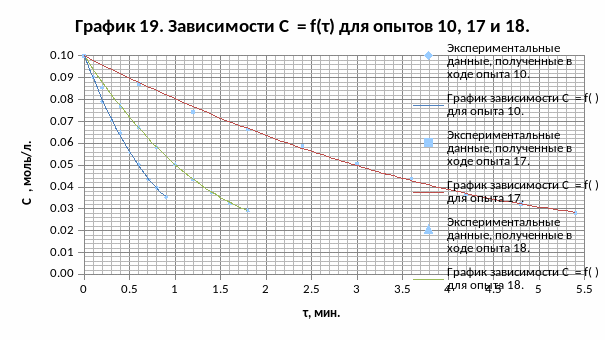
Линеаризуем зависимости СY = f(τ) для опытов 10, 17 и 18, строя графики зависимостей
ln(СY) = f(τ) для этих опытов (так как мы знаем, что порядок каталитической составляющей исследуемой реакции по реагенту Y равен 1).
Время, прошедшее после начала опыта τ, мин. |
ln(СY). |
||
Опыт 10 |
Опыт 17 |
Опыт 18 |
|
0 |
-2,302585093 |
-2,302585093 |
-2,302585093 |
0,1 |
-2,404518156 |
- |
- |
0,2 |
-2,539029206 |
- |
-2,455654399 |
0,3 |
-2,653505199 |
- |
- |
0,4 |
-2,738782642 |
- |
-2,562690975 |
0,5 |
-2,887272565 |
- |
- |
0,6 |
-2,985128691 |
-2,439166779 |
-2,695505881 |
0,7 |
-3,13690421 |
- |
- |
0,8 |
-3,226756798 |
- |
-2,841000266 |
0,9 |
-3,343872315 |
- |
- |
1 |
- |
- |
-2,986044888 |
1,2 |
- |
-2,598258236 |
-3,128083494 |
1,4 |
- |
- |
-3,285128721 |
1,6 |
- |
- |
-3,424320461 |
1,8 |
- |
-2,712161149 |
-3,527321272 |
2,4 |
- |
-2,836598044 |
- |
3 |
- |
-2,984064804 |
- |
3,6 |
- |
-3,124498603 |
- |
4,2 |
- |
-3,309489774 |
- |
4,8 |
- |
-3,437239692 |
- |
5,4 |
- |
-3,569096038 |
- |
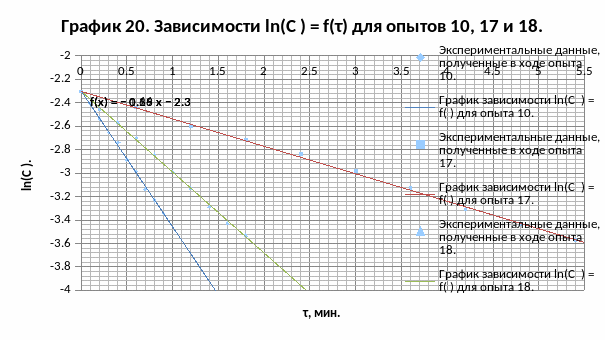
tg α17 = -0,2337 1/мин;
tg α18 = -0,6886 1/мин.
Кэф.K 17 = 0,2337 1/мин;
Кэф.K 18 = 0,6886 1/мин.
Перед тем, как постанавливать и проверять гипотезы о порядке каталитической составляющей исследуемой реакции по А, нам необходимо найти критерий воспроизводимости S2воспр. К.эф. К для эффективной константы скорости каталитической составляющей реакции Кэф.К. Для этого линеаризуем зависимости СY = f(τ) для опытов 10-14, строя графики зависимостей ln(СY)= f(τ) для этих опытов.
τ, мин. |
ln(СY). |
|||
Опыт 11 |
Опыт 12 |
Опыт 13 |
Опыт 14 |
|
0 |
-2,302585093 |
-2,302585093 |
-2,302585093 |
-2,302585093 |
0,1 |
-2,434397153 |
-2,436807616 |
-2,389954665 |
-2,430949833 |
0,2 |
-2,542682413 |
-2,554850319 |
-2,489326165 |
-2,555042593 |
0,3 |
-2,649341984 |
-2,65903769 |
-2,639893135 |
-2,601786094 |
0,4 |
-2,752121249 |
-2,774189555 |
-2,75278175 |
-2,751813157 |
0,5 |
-2,870964215 |
-2,849456479 |
-2,858451947 |
-2,865282951 |
0,6 |
-3,000854992 |
-3,0269254 |
-2,963972672 |
-3,00063043 |
0,7 |
-3,061204393 |
-3,098763194 |
-3,115808943 |
-3,105236808 |
0,8 |
-3,224543732 |
-3,202076182 |
-3,239020065 |
-3,193593094 |
0,9 |
-3,346551084 |
-3,322374187 |
-3,319111108 |
-3,341953025 |

tg α11 = -1,1426 1/мин;
Кэф.К 11 = 1,1426 1/мин.
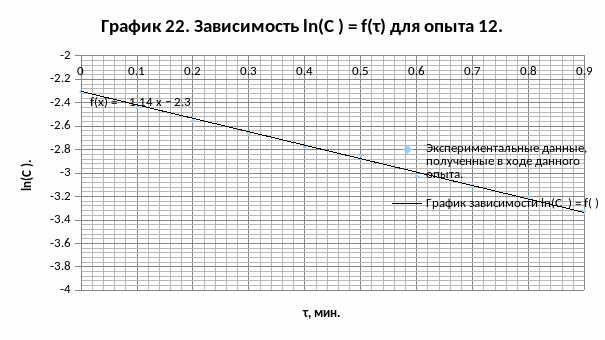
tg α12 = -1,1446 1/мин;
Кэф.К 12 = 1,1446 1/мин.

tg α13 = -1,1352 1/мин;
Кэф.К 13 = 1,1352 1/мин.

tg α14 = -1,1379 1/мин;
Кэф.К 14 = 1,1379 1/мин.
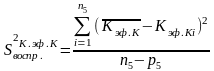 ,
где Кэф.К
- среднее арифметическое из n1
значений эффективной константы скорости
каталитической составляющей реакции
Кэф.К,
i
- номер данного измерения из n3
измерений (в нашем случае n5
= 5), p5
- число параметров для данной величины
данной серии измерений (в нашем случае
р5
= 1),
,
где Кэф.К
- среднее арифметическое из n1
значений эффективной константы скорости
каталитической составляющей реакции
Кэф.К,
i
- номер данного измерения из n3
измерений (в нашем случае n5
= 5), p5
- число параметров для данной величины
данной серии измерений (в нашем случае
р5
= 1),
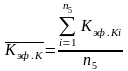 .
.
Кэф.К = (1,1578+1,1426+1,1446+1,1352+1,1379)/5 = 1,1436 1/мин.
Показатели |
Опыт 10 |
Опыт 11 |
Опыт 12 |
Опыт 13 |
Опыт 14 |
Кэф.Кi, 1/мин. |
1,1578 |
1,1426 |
1,1446 |
1,1352 |
1,1379 |
Кэф.К-Кэф.Кi, 1/мин. |
-0,01418 |
0,00102 |
-0,00098 |
0,00842 |
0,00572 |
(Кэф.К-Кэф.Кi)2, 1/мин2. |
2,01072·10-4 |
1,0404·10-6 |
9,604·10-7 |
7,08964·10-5 |
3,27184·10-5 |
S2воспр. К.эф.К = 7,6672·10-5 1/мин2.
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту А nА, равный 1.
Строим график зависимости Кэф.К. = f(СА0):
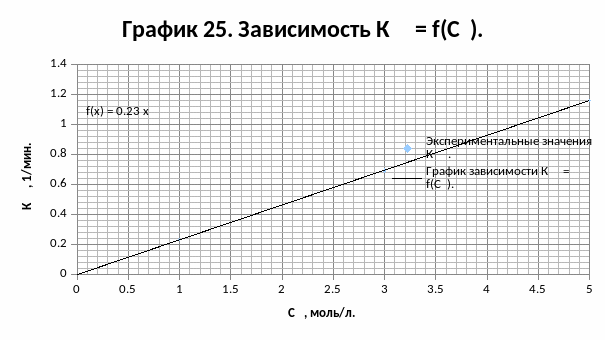
tg δ1 = 0,2311 л/(моль·мин) (угол наклона графика зависимости Кэф.К = f(СА0)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
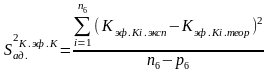 ,
где Кэф.Кi.теор
- значения Кэф.К,
найденные по формуле:
,
где Кэф.Кi.теор
- значения Кэф.К,
найденные по формуле:
Кэф.Кi.теор = tg δ1·CА0, Кэф.Кi.эксп – экспериментальные значения Кэф.К, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3), p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Начальная концентрация реагента А СА0, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
1 |
0,2311 |
0,2337 |
3 |
0,6933 |
0,6886 |
5 |
1,1555 |
1,1578 |
S2ад. К.эф.К = 1,707·10-5 1/мин2.
Проверяем адекватность данной гипотезы, рассчитав критерий Фишера Fоп. К.эф.К по формуле:
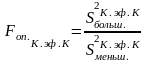 ,
где S2больш.
К.эф.К
- больший критерий для величины Кэф.К,
S2меньш.
К.эф.К
- меньший критерий для величины Кэф.К,
,
где S2больш.
К.эф.К
- больший критерий для величины Кэф.К,
S2меньш.
К.эф.К
- меньший критерий для величины Кэф.К,
и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К < S2воспр. К.эф.К, то:
Fоп. К.эф.К = 7,6672·10-5/ 1,707·10-5 = 4,4916.
При fК.эф.К 1 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4,
fК.эф.К 2 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3-1 = 2 и α = 0,01:
Fтабл. К.эф.K = 99,25.
Так как Fтабл. К.эф.K > Fоп. К.эф.K , то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту А, равный 1, верна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту А nА, равный 0,5.
Строим график зависимости Кэф.К = f(СА00,5):
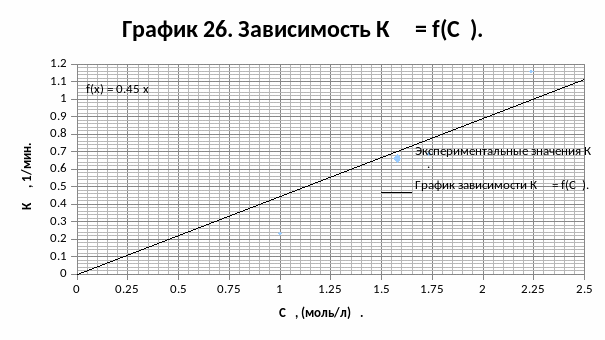
tg ε1 = 0,4461 л0,5/(моль0,5·мин) (угол наклона графика зависимости Кэф.К = f(СА00,5)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
, где Кэф.Кi.теор - значения Кэф.К, найденные по формуле:
Кэф.Кi.теор = tg ε1·CА00,5, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3),
p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Начальная концентрация реагента А СА0, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
1 |
0,4461 |
0,2337 |
3 |
0,772667865 |
0,6886 |
5 |
0,997509925 |
1,1578 |
S2ад. К.эф.К = 3,8937·10-2 1/мин2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. К.эф.К, и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К > S2воспр. К.эф.К, то:
Fоп. К.эф.К = 3,8937·10-2/ 7,6672·10-5 = 507,84.
При fК.эф.К 1 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3 - 1 = 2,
fК.эф.К 2 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4 и α = 0,01:
Fтабл. К.эф.K = 18.
Так как Fтабл. К.эф.K > Fоп. К.эф.K, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту А, равный 0,5, неверна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по реагенту А nА, равный 1,5.
Строим график зависимости Кэф.К = f(СА01,5):
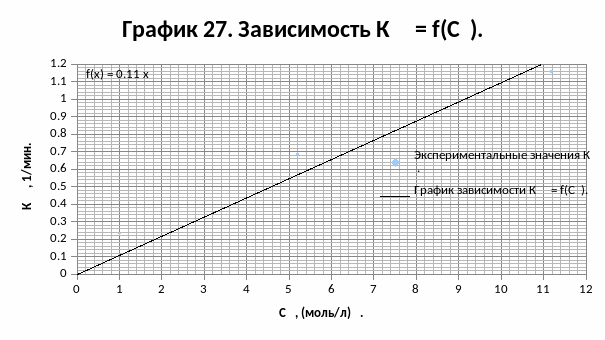
tg ζ1 = 0,1095 л1,5/(моль1,5·мин) (угол наклона графика зависимости Кэф.К = f(СА01,5)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
, где Кэф.Кi.теор - значения Кэф.К, найденные по формуле:
Кэф.Кi.теор = tg ζ1·CА01,5, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3), p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Начальная концентрация реагента А СА0, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
1 |
0,1095 |
0,2337 |
3 |
0,56897869 |
0,6886 |
5 |
1,224247218 |
1,1578 |
S2ад. К.эф.К = 1,7075·10-2 1/мин2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. К.эф.К, и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К > S2воспр. К.эф.К, то:
Fоп. К.эф.К = 1,7075·10-2/ 7,6672·10-5 = 222,7.
При fК.эф.К 1 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3 - 1 = 2,
fК.эф.К 2 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4 и α = 0,01:
Fтабл. К.эф.K = 18.
Так как Fтабл. К.эф.K > Fоп. К.эф.K, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по реагенту А, равный 1,5, неверна.
Выводы: После проведения данных опытов мы установили, что порядок каталитической составляющей данной реакции по реагенту А nА равен 1 и мы можем использовать этот факт при постановке последующих опытов и обработке полученных при этом данных.
Опыты 19, 20. Определение порядка каталитической составляющей исследуемой реакции по катализатору К.
Условия опыта 19: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,2 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
8,6971·10-2 |
3 |
0,2 |
7,314·10-2 |
4 |
0,3 |
6,395·10-2 |
5 |
0,4 |
5,5009·10-2 |
6 |
0,5 |
4,5538·10-2 |
7 |
0,6 |
3,873·10-2 |
8 |
0,7 |
3,4218·10-2 |
9 |
0,8 |
2,9306·10-2 |
10 |
0,9 |
2,4061·10-2 |
Условия опыта 20: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,25 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,1 |
2 |
0,1 |
8,4302·10-2 |
3 |
0,2 |
7,0058·10-2 |
4 |
0,3 |
5,6904·10-2 |
5 |
0,4 |
4,5206·10-2 |
6 |
0,5 |
3,8298·10-2 |
7 |
0,6 |
3,0054·10-2 |
8 |
0,7 |
2,6305·10-2 |
9 |
0,8 |
2,1302·10-2 |
10 |
0,9 |
1,8158·10-2 |

Линеаризуем зависимости СY = f(τ) для опытов 10, 19 и 20, строя графики зависимостей
ln(СY) = f(τ) для этих опытов (так как мы знаем, что порядок каталитической составляющей исследуемой реакции по реагенту Y равен 1).
Время, прошедшее после начала опыта τ, мин. |
ln(Сy). |
||
Опыт 10 |
Опыт 19 |
Опыт 20 |
|
0 |
-2,302585093 |
-2,302585093 |
-2,302585093 |
0,1 |
-2,404518156 |
-2,442185045 |
-2,473351943 |
0,2 |
-2,539029206 |
-2,615378362 |
-2,65842824 |
0,3 |
-2,653505199 |
-2,749653391 |
-2,866391838 |
0,4 |
-2,738782642 |
-2,900261143 |
-3,09653351 |
0,5 |
-2,887272565 |
-3,089217953 |
-3,262362852 |
0,6 |
-2,985128691 |
-3,251134976 |
-3,504749001 |
0,7 |
-3,13690421 |
-3,374991534 |
-3,63800206 |
0,8 |
-3,226756798 |
-3,529979214 |
-3,848972951 |
0,9 |
-3,343872315 |
-3,727162508 |
-4,008670699 |
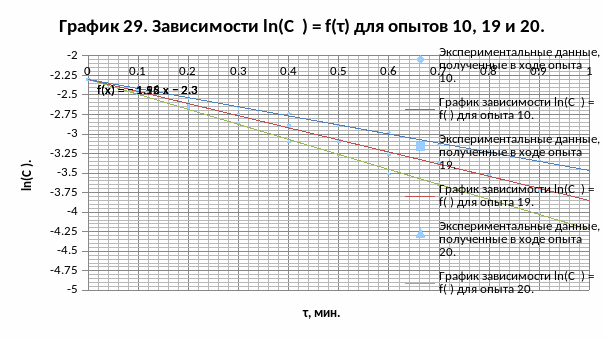
tg α19 = -1,5533 1/мин;
tg α20 = -1,924 1/мин.
Кэф.K 19 = 1,5533 1/мин;
Кэф.K 20 = 1,924 1/мин.
Предположим, что каталитическая составляющая данной реакции имеет порядок по катализатору К nК, равный 1.
Строим график зависимости Кэф.К = f(СК):

tg η1 = 7,7226 л/(моль·мин) (угол наклона графика зависимости Кэф.К = f(СК)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
, где Кэф.Кi.теор - значения Кэф.К, найденные по формуле:
Кэф.Кi.теор = tg η1·CК, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3),
p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Концентрация в реакционной системе катализатора К СК, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
0,15 |
1,15839 |
1,1578 |
0,2 |
1,54452 |
1,5533 |
0,25 |
1,93065 |
1,924 |
S2ад. К.эф.К = 6,083·10-5 1/мин2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. К.эф.К, и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К < S2воспр. К.эф.К, то:
Fоп. К.эф.К = 7,6672·10-5/6,083·10-5 = 1,2604.
При fК.эф.К 1 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4,
fК.эф.К 2 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3-1 = 2 и α = 0,01:
Fтабл. К.эф.K = 99,25.
Так как Fтабл. К.эф.K > Fоп. К.эф.K, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по катализатору К, равный 1, верна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по катализатору К nК, равный 0,5.
Строим график зависимости Кэф.К = f(СК0,5):
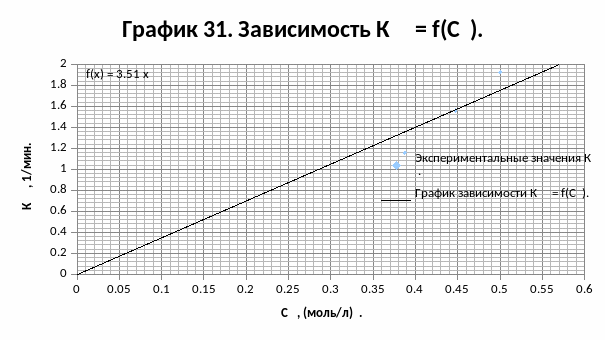
tg θ1 = 7,7226 л0,5/(моль0,5·мин) (угол наклона графика зависимости Кэф.К = f(СК0,5)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
, где Кэф.Кi.теор - значения Кэф.К, найденные по формуле:
Кэф.Кi.теор = tg θ1·CК0,5, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3),
p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Концентрация в реакционной системе катализатора К СК, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
0,15 |
1,358836207 |
1,1578 |
0,2 |
1,5690489 |
1,5533 |
0,25 |
1,75425 |
1,924 |
S2ад. К.эф.К = 3,4739·10-2 1/мин2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. К.эф.К, и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К > S2воспр. К.эф.К, то:
Fоп. К.эф.К = 3,4739·10-2/ 7,6672·10-5 = 453,09.
При fК.эф.К 1 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3 - 1 = 2,
fК.эф.К 2 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4 и α = 0,01:
Fтабл. К.эф.K = 18.
Так как Fтабл. К.эф.K < Fоп. К.эф.K, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по катализатору К, равный 0,5, неверна.
Предположим, что каталитическая составляющая данной реакции имеет порядок по катализатору К nК, равный 1,5.
Строим график зависимости Кэф.К = f(СК1,5):

tg ι1 = 7,7226 л1,5/(моль1,5·мин) (угол наклона графика зависимости Кэф.К = f(СК1,5)).
Доказываем эту гипотезу.
Находим критерий адекватности S2ад. К.эф.К для данного параметра (эффективной константы скорости каталитической составляющей реакции Кэф.К) по формуле:
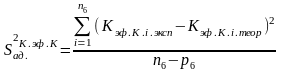 ,
где Кэф.Кi.теор
- значения Кэф.К,
найденные по формуле:
,
где Кэф.Кi.теор
- значения Кэф.К,
найденные по формуле:
Кэф.Кi.теор = tg ι1·CК0,5, i - номер данного измерения из n6 измерений (в нашем случае n6 = 3),
p6 - число параметров для данной величины данной серии измерений (в нашем случае р6 = 1).
Концентрация в реакционной системе катализатора К СК, моль/л. |
Кэф.Кi.теор, 1/мин. |
.Кэф.Кi.эксп, 1/мин. |
0,15 |
0,961131166 |
1,1578 |
0,2 |
1,479758233 |
1,5533 |
0,25 |
2,068025 |
1,924 |
S2ад. К.эф.К = 3,2415·10-2 1/мин2.
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. К.эф.К, и сравнив его с табличным значением, взятым из [1].
Так как S2ад.К.эф.К > S2воспр. К.эф.К2, то:
Fоп. К.эф.К = 3,2415·10-2/ 7,6672·10-5 = 446,25.
При fК.эф.К 1 = faд. К.эф.К = nад. К.эф.К - pад. К.эф.К = 3 - 1 = 2,
fК.эф.К 2 = fвоспр. К.эф.К = nвоспр .К.эф.К - pвоспр. К.эф.К = 5 - 1 = 4 и α = 0,01:
Fтабл. К.эф.K = 18.
Так как Fтабл. К.эф.K < Fоп. К.эф.K, то данная гипотеза о том, что каталитическая составляющая исследуемой реакции имеет порядок по катализатору К, равный 1,5, неверна.
Выводы: После проведения данных опытов мы установили, что порядок каталитической составляющей данной реакции по катализатору К nК равен 1 и мы можем использовать этот факт при постановке последующих опытов и обработке полученных при этом данных.
Опыты 21, 22. Проверка построенной кинетической модели для каталитической составляющей исследуемой реакции на адекватность.
Условия опыта 21: Начальная концентрация реагента А CA0 = 3 моль/л;
Начальная концентрация реагента Y CY0 = 0,3 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,2 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,3 |
2 |
0,2 |
0,2406 |
3 |
0,4 |
0,2014 |
4 |
0,6 |
0,1705 |
5 |
0,8 |
0,14 |
6 |
1 |
0,1138 |
7 |
1,2 |
0,1009 |
8 |
1,4 |
0,0801 |
9 |
1,6 |
0,0677 |
10 |
1,8 |
0,0579 |
Условия опыта 22: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,5 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,25 моль/л;
Температура опыта t = 100ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y CY, моль/л. |
1 |
0 |
0,5 |
2 |
0,1 |
0,4057 |
3 |
0,2 |
0,3476 |
4 |
0,3 |
0,2864 |
5 |
0,4 |
0,2324 |
6 |
0,5 |
0,1914 |
7 |
0,6 |
0,1573 |
8 |
0,7 |
0,1334 |
9 |
0,8 |
0,1042 |
10 |
0,9 |
0,0903 |
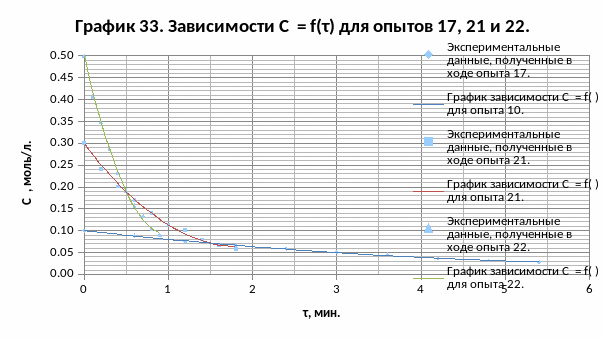
Линеаризуем зависимости СY = f(τ) для опытов 10, 17 и 18, строя графики зависимостей
ln(СY) = f(τ) для этих опытов (так как мы знаем, что порядок каталитической составляющей исследуемой реакции по реагенту Y равен 1).
Время, прошедшее после начала опыта τ, мин. |
ln(СY). |
||
Опыт 17 |
Опыт 21 |
Опыт 22 |
|
0 |
-2,302585093 |
-1,203972804 |
-0,693147181 |
0,1 |
- |
- |
-0,902068228 |
0,2 |
- |
-1,424745793 |
-1,056622452 |
0,3 |
- |
- |
-1,250466687 |
0,4 |
- |
-1,602332764 |
-1,459492003 |
0,5 |
- |
- |
-1,653340271 |
0,6 |
-2,439166779 |
-1,769022387 |
-1,849313098 |
0,7 |
- |
- |
-2,014648078 |
0,8 |
- |
-1,966385394 |
-2,261276177 |
0,9 |
- |
- |
-2,404514579 |
1 |
- |
-2,173400107 |
- |
1,2 |
-2,598258236 |
-2,29362664 |
- |
1,4 |
- |
-2,524441798 |
- |
1,6 |
- |
-2,692062105 |
- |
1,8 |
-2,712161149 |
-2,849316137 |
- |
2,4 |
-2,836598044 |
- |
- |
3 |
-2,984064804 |
- |
- |
3,6 |
-3,124498603 |
- |
- |
4,2 |
-3,309489774 |
- |
- |
4,8 |
-3,437239692 |
- |
- |
5,4 |
-3,569096038 |
- |
- |
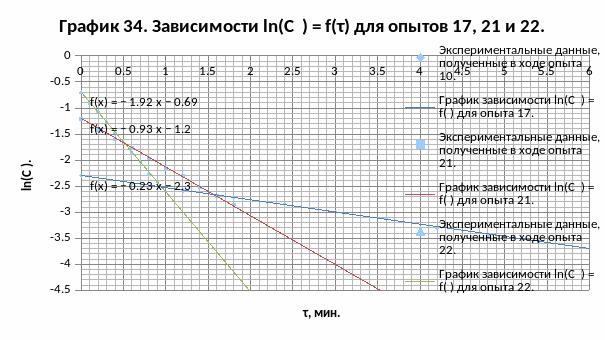
tg α21= -0,9316 1/мин;
tg α22= -1,9161 1/мин.
Кэф.К 21 = 0,9316 1/мин;
Кэф.К 22 = 1,9161 1/мин.
Зная значения Кэф.К для опытов 17, 21 и 22, находим значения истинной константы скорости каталитической составляющей реакции КК для этих опытов по формуле:

КК 17 = 0,2337/(1·0,15) = 1,558 л2/(моль2·мин);
КК 21 = 0,9316/(3·0,2) = 1,5527 л2/(моль2·мин);
КК 22 = 1,9161/(5·0,25) = 1,5329 л2/(моль2·мин).
Находим критерий воспроизводимости S2воспр. КК для истинной константы скорости каталитической составляющей реакции КК:
КК 10 = 1,1578/(0,15·5) = 1,5437 л2/(моль2·мин);
КК 11 = 1,1426/(0,15·5) = 1,5235 л2/(моль2·мин);
КК 12 = 1,1446/(0,15·5) = 1,5261 л2/(моль2·мин);
КК 13 = 1,1352 /(0,15·5) = 1,5136 л2/(моль2·мин);
КК 14 = 1,1379 /(0,15·5) = 1,5172 л2/(моль2·мин).
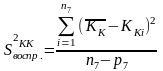 ,
где КК
- среднее арифметическое из n5
значений истинной константы скорости
каталитической составляющей реакции
КК
, i
- номер данного измерения из n5
измерений (в нашем случае n7
= 5), p7
- число параметров для данной величины
данной серии измерений (в нашем случае
р7
= 1).
,
где КК
- среднее арифметическое из n5
значений истинной константы скорости
каталитической составляющей реакции
КК
, i
- номер данного измерения из n5
измерений (в нашем случае n7
= 5), p7
- число параметров для данной величины
данной серии измерений (в нашем случае
р7
= 1).
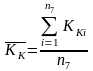 .
.
КК = (1,5437+1,5235+1,5261+1,5136+1,5172)/5 = 1,5248 л2/(моль2·мин).
Показатели |
Опыт 10 |
Опыт 11 |
Опыт 12 |
Опыт 13 |
Опыт 14 |
ККi, л2/(моль2·мин). |
1,5437 |
1,5235 |
1,5261 |
1,5136 |
1,5172 |
КК.-ККi, л2/(моль2·мин). |
0,01888 |
-0,00132 |
0,00128 |
-0,01122 |
-0,00762 |
(КК-ККi)2, л4/(моль4·мин2). |
3,5645·10-4 |
1,7424·10-6 |
1,6384·10-6 |
1,2589·10-4 |
5,8064·10-5 |
S2воспр. КК = 1,3595·10-4 л4/(моль4·мин2).
Находим критерий адекватности S2ад. КК для данного параметра (истинной константы скорости каталитической составляющей реакции К) по формуле:
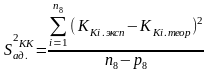 ,
где ККi.теор
- теоретическое значение КК
(она по определению не зависит от
начальных концентраций реагентов А и
Y
СА0
и СY0
соответственно и катализатора К СК
в реакционной системе и её значение
будет равно:
,
где ККi.теор
- теоретическое значение КК
(она по определению не зависит от
начальных концентраций реагентов А и
Y
СА0
и СY0
соответственно и катализатора К СК
в реакционной системе и её значение
будет равно:
ККi.теор = КК = (1,558+1,5527+1,5329)/3 = 1,5479 л2/(моль2·мин)
,ККi.эксп - экспериментальные значения КК, i - номер данного измерения из n6 измерений
(в нашем случае n8 = 3), p8 - число параметров для данной величины данной серии измерений (в нашем случае р8 = 1).
Номер опыта |
ККi.теор, л2/(моль2·мин). |
ККi.эксп, л2/(моль2·мин). |
17 |
1,5479 |
1,558 |
21 |
1,5479 |
1,5527 |
22 |
1,5479 |
1,5329 |
Sад. КК2 =1,7503·10-4 л4/(моль4·мин2).
Проверяем адекватность данной гипотезы, рассчитывая критерий Фишера Fоп. КК по формуле:
 ,
где S2больш
КК
- больший критерий для величины КК,
S2меньш.
КК
- меньший критерий для величины КК,
,
где S2больш
КК
- больший критерий для величины КК,
S2меньш.
КК
- меньший критерий для величины КК,
и сравнив его с табличным значением, взятым из [1].
Так как S2ад КК > S2воспр КК, то:
Fоп. КК = 1,7503·10-4/1,3595·10-4 = 1,2875.
При fКК.1 = faд. КК = nад. КК - pад. КК = 3 - 1 = 2,
fКК.2 = fвоспр. КК = nвоспр .КК - pвоспр. КК = 5 - 1 = 4 и α = 0,01:
Fтабл. КK = 18.
Так как Fтабл. КК > Fоп. КК, то данная гипотеза о виде построенной нами кинетической модели для каталитической составляющей данной реакции верна.
Вывод: После проведения данных опытов мы удостоверились в том, что построенная нами кинетическая модель для каталитической составляющей исследуемой реакции является адекватной. По данной кинетической модели, кинетическое уравнение для каталитической составляющей исследуемой реакции имеет вид:
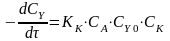 ,
где КК - истинная константа скорости
каталитической составляющей данной
реакции:
,
где КК - истинная константа скорости
каталитической составляющей данной
реакции:
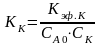 ,
где Кэф.К – эффективная константа
скорости каталитической составляющей
данной реакции.
,
где Кэф.К – эффективная константа
скорости каталитической составляющей
данной реакции.
,а общий порядок каталитической составляющей данной реакции n равен:
n = nA + nY + nK = 1 + 1 + 1 = 3.
Опыты 23, 24. Нахождение активационных параметров для каталитической составляющей исследуемой реакции.
Используя построенную нами кинетическую модель для каталитической составляющей данной реакции и уравнение Аррениуса:
 ,
где КК0 - предэкспоненциальный множитель
каталитической составляющей данной
реакции, EК
- энергия активации каталитической
составляющей данной реакции, R
- универсальная газовая постоянная (R
= 8,314 кДж/моль·К),
,
где КК0 - предэкспоненциальный множитель
каталитической составляющей данной
реакции, EК
- энергия активации каталитической
составляющей данной реакции, R
- универсальная газовая постоянная (R
= 8,314 кДж/моль·К),
Т - термодинамическая температура, при которой протекает данная реакция: T = t+273,15, находим активационные параметры каталитической составляющей данной реакции: КК0 и ЕК.
Для этого нам необходимо выяснить зависимость истинной константы скорости каталитической составляющей исследуемой реакции КК от термодинамической температуры, при которой протекает данная реакция.
Условия опыта 23:Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 80ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y, моль/л. |
1 |
0 |
0,1 |
2 |
0,5 |
8,5085·10-2 |
3 |
1 |
6,8679·10-2 |
4 |
1,5 |
5,5962·10-2 |
5 |
2 |
4,8033·10-2 |
6 |
2,5 |
3,8208·10-2 |
7 |
3 |
3,2113·10-2 |
8 |
3,5 |
2,5863·10-2 |
9 |
4 |
2,2174·10-2 |
10 |
4,5 |
1,8348·10-2 |
Условия опыта 24: Начальная концентрация реагента А CA0 = 5 моль/л;
Начальная концентрация реагента Y CY0 = 0,1 моль/л;
Начальная концентрация реагента B CB0 = 0 моль/л;
Начальная концентрация реагента Z CZ0 = 0 моль/л;
Концентрация катализатора K CK = 0,15 моль/л;
Температура опыта t = 120ºC.
Результаты опыта:
№ измерения |
Время, прошедшее после начала опыта τ, мин. |
Концентрация реагента Y, моль/л. |
1 |
0 |
0,1 |
2 |
0,05 |
8,4191·10-2 |
3 |
0,1 |
7,4519·10-2 |
4 |
0,15 |
6,2775·10-2 |
5 |
0,2 |
5,5818·10-2 |
6 |
0,25 |
4,606·10-2 |
7 |
0,3 |
3,7937·10-2 |
8 |
0,35 |
3,261·10-2 |
9 |
0,4 |
2,8842·10-2 |
10 |
0,45 |
2,46·10-2 |

Линеаризуем зависимости СY = f(τ) для опытов 10, 23 и 24, строя графики зависимостей
ln(СY)= f(τ) для этих опытов (так как мы знаем, что порядок каталитической составляющей исследуемой реакции по реагенту А равен 1).
Время, прошедшее после начала опыта τ, мин. |
ln(СY). |
||
Опыт 10 |
Опыт 23 |
Опыт 24 |
|
0 |
-2,302585093 |
-2,302585093 |
-2,302585093 |
0,05 |
- |
- |
-2,474667252 |
0,1 |
-2,404518156 |
- |
-2,596701153 |
0,15 |
- |
- |
-2,768198374 |
0,2 |
-2,539029206 |
- |
-2,885658881 |
0,25 |
- |
- |
-3,077810385 |
0,3 |
-2,653505199 |
- |
-3,27182839 |
0,35 |
- |
- |
-3,423136289 |
0,4 |
-2,738782642 |
- |
-3,545922621 |
0,45 |
- |
- |
-3,705008836 |
0,5 |
-2,887272565 |
-2,464104522 |
- |
0,6 |
-2,985128691 |
- |
- |
0,7 |
-3,13690421 |
- |
- |
0,8 |
-3,226756798 |
- |
- |
0,9 |
-3,343872315 |
- |
- |
1 |
- |
-2,678311803 |
- |
1,5 |
- |
-2,88308239 |
- |
2 |
- |
-3,035867004 |
- |
2,5 |
- |
-3,264710361 |
- |
3 |
- |
-3,438494346 |
- |
3,5 |
- |
-3,654941903 |
- |
4 |
- |
-3,808834848 |
- |
4,5 |
- |
-3,998234702 |
- |

tg α23 = -0,3789 1/мин;
tg α24 = -3,1294 1/мин.
Кэф.К 23 = 0,3789 1/мин;
Кэф.К 24 = 3,1294 1/мин.
Зная значения Кэф.К для опытов 23 и 24, находим значения КК для этих опытов:
КК 23 = 0,3789/(0,15·5) = 0,5052 л2/(моль2·мин):
КК 24 = 3,1294/(0,15·5) = 4,1725 л2/(моль2·мин).
Строим зависимость ln(КК) = f(1/T):
№ опыта |
КК, л2/(моль2·мин). |
ln(KК). |
T,К. |
1/Т, 1/К. |
10 |
1,5437 |
0,434182132 |
373,15 |
0,002679887 |
23 |
0,5052 |
-0,682800889 |
353,15 |
0,002831658 |
24 |
4,1725 |
1,428515377 |
393,15 |
0,002543558 |

Из данного графика мы узнаём, что а = 20,072 (величина отрезка на оси ординат, отсекаемая интерполированным до значения 1/T = 0 графиком зависимости ln(KК) = f(1/T));
tg κ= -7329 (угол наклона графика зависимости ln(KК) = f(1/T)).
По уравнению Аррениуса: lnKК0 = a; → KК0 = ea ;
tg κ = -EК/R; → EК = -tg κ·R.
Находим значения ЕК и KК0 :
KК0 = e20,072 = 5,2139·108 л2/(моль2·мин);
ЕK = 8,314·7329 = 60933 Дж/моль = 60,93 кДж/моль.
Вывод: После проведения данных опытов мы установили активационные параметры каталитической составляющей исследуемой реакции - её предэкспоненциальный множитель КК0 и энергию активации ЕК. Для данной реакции: КК0 = 5,2139·108 л2/(моль2·мин); ЕК = 60,93
кДж/моль.
Общий вывод: После проведения опытов 10-24 мы полностью исследовали каталитическую составляющую данной реакции, составив её кинетическую модель и найдя её активационные параметры (её предэкспоненциальный множитель КК0 и энергию активации ЕК). По данной кинетической модели, кинетическое уравнение для каталитической составляющей исследуемой реакции имеет вид:
, где КК - истинная константа скорости каталитической составляющей данной реакции:
, где Кэф.К – эффективная константа скорости каталитической составляющей данной реакции.
,общий порядок каталитической составляющей данной реакции n равен: n = nA + nY + nK = 1 + 1 + 1 = 3, КК0 = 5,2139·108 л2/(моль2·мин) и ЕК = 60,93 кДж/моль.
