- •26.08.2011 Г. Протокол №1
- •Выписка из плана учебного процесса
- •Содержание
- •Введение
- •Сферы применения природных и синтетических цеолитов
- •1. Общие свойства и особенности структуры цеолитов
- •1.1 Химические составы природных цеолитов
- •1.2 Номенклатура цеолитов
- •1.3 Классификация цеолитов
- •1.4 Типы кристаллических решеток. Структуры цеолитов
- •Кристаллографические сингонии
- •Формы кристаллов
- •2 Краткие сведения о генезисе природных цеолитов.
- •3 Вода в минералах. Классификация. Вода в цеолитах
- •Измерения усредненных диффузией
- •4 Свойства цеолитов
- •4.1 Физические свойства цеолитов
- •4.2. Химические свойства цеолитов
- •5. Синтез цеолитов. Молекулярные сита
- •Синтезы порошкообразных цеолитов различных типов при кристаллизации алюмокремниевых гидрогелей
- •6. Ионный обмен. Ионный обмен на различных формах цеолитов
- •Цеолиты как ионообменники для защиты окружающей среды.
- •7. Адсорбция. Адсорбционные свойства цеолитов
- •Ионная адсорбция
- •Обманная адсорбция
- •Vpsa генераторы кислорода
- •8. Катализ. Использование цеолитов в качестве катализаторов
- •Типы катализаторов
- •Как работают катализаторы
- •Применение катализа в промышленности
- •9. Использование цеолитов в нефтяной и газовой промышленности Подготовка нефти и газа к транспорту
- •Основные способы отделения воды от нефти
- •Осушка газа молекулярными ситами
- •Экспериментальное исследование адсорбции нефтепродуктов в слое цеолитов б.С.Байзакова, к.К. Сырманова, ф.Е.Алтынбеков
Обманная адсорбция
Если на поверхности адсорбента уже адсорбирован электролит, то при контакте этого сорбента с другим электролитом почти всегда в той или иной степени наблюдается обменная адсорбция, или, правильнее, обмен ионов между двойным электрическим слоем адсорбента и средой. При обменной адсорбции адсорбент, поглощая определенное количество каких-либо ионов, одновременно выделяет в раствор эквивалентное количество других ионов того же знака, вытесненных с поверхности.
К обмену способны не только чужеродные ионы с адсорбированными адсорбентами, но и ионы, образующиеся из самого адсорбента в результате диссоциации его молекул. При этом поверхностное явление, каким является адсорбция, может переходить в объемное явление, т. е. в обмене могут участвовать ионы, расположенные в глубинных слоях адсорбента, если только к ним возможен доступ раствора. В частности, это происходит при обмене ионов на пермутите натрия (Na2[Al2Si2O8] . nH2O – искусственно приготовленные гидратированные алюмосиликаты – пермутиты) и ионообменных смолах, о которых будет сказано ниже. Понятно, что вещества, способные к объемному обмену ионов, обладают особенно высокой емкостью поглощения соответствующего иона из раствора.
Обменная адсорбция имеет ряд особенностей.
1. обменная адсорбция специфична, т. е. к обмену способны только определенные ионы. Иными словами, на обменную адсорбцию сильно влияет как природа твердой фазы и имеющегося на ней двойного электрического слоя, так и природа адсорбируемого иона. В зависимости от химической природы ионов, которые могут обмениваться с ионами, содержащимися в адсорбентах, различают кислотные и основные адсорбенты. Кислотные адсорбенты ведут себя подобно кислоте и способны обменивать с растворами катионы; основные адсорбенты сходны по свойствам с основаниями и обменивают анионы. Впрочем, существует много амфотерных адсорбентов, которые в одних условиях обменивают катионы, а в других – анионы. Специфичность обменной адсорбции указывает на то, что по своей природе этот процесс приближается к химическим явлениям.
2. обменная адсорбция не всегда обратима.
3. обменная адсорбция, как правило, протекает более медленно, чем молекулярная адсорбция. Особенно медленно она протекает, когда происходит обмен ионов, находящихся в глубине адсорбента. Очевидно, в данном случае время необходимо для того, чтобы ионы из раствора продиффундировали в глубь адсорбента и вытеснили оттуда ионы, которые в свою очередь должны перейти в раствор.
4. при обменной адсорбции может изменяться рН среды. Это наблюдается в том случае, когда ионом, обмениваемым адсорбентом, является водородный или гидроксильный ион. Если адсорбент заменяет на какой-нибудь катион водородный ион, то последний, поступая в раствор, уменьшает рН среды, при этом адсорбент ведет себя подобно кислоте. Если адсорбент меняет на какой-нибудь анион гидроксильный ион, то рН раствора, наоборот, увеличивается, причем адсорбент ведет себя как основание. Наглядно обмен ионов в обоих этих случаях можно изобразить следующими схемами:
![]()
![]()
Б. П. Никольский (1939 г.) предложил уравнение, количественно характеризующее обмен ионов 1 и 2 на твердой поверхности:
 (1)
(1)
где g1, g2 – содержание обменивающихся ионов в адсорбенте, г-экв/г;
a1, a2 – активности обменивающихся ионов в растворе;
z1, z2 – валентность ионов;
k – константа.
При z1 = z2 = 1 уравнение упрощается:
![]() (2)
(2)
При небольших концентрациях электролита вместо активности а можно пользоваться значением концентрации. В этом случае уравнение (2), связывающее адсорбционную способность ионов 1 и 2 с их концентрацией в растворе, принимает вид:
![]() (3)
(3)
Обменная адсорбция имеет большое значение в земледелии, биологии и технике. Почва способна поглощать и удерживать определенные ионы, например катионы К+ и NH4+, содержащиеся в удобрениях и необходимые для питания растений. Взамен этих катионов почва выделяет эквивалентные количества других катионов, например Са2+ и Mg2+. Анионы, как, например, Сl–, NO3–, SO4–2, почти не поглощаются почвой. Согласно К. К. Гедройцу (1933 г.), детально исследовавшему явление обмена ионов в почве, поглощать основания способен так называемый поглощающий комплекс – высокодисперсная смесь нерастворимых алюмосиликатов и органоминеральных соединений. От природы поглощенных ионов в значительной мере зависят физические и агротехнические свойства почвы.
В технике обменная адсорбция имеет существенное значение. Например, при крашении растительного волокна оно адсорбирует из среды окрашенные катионы красителя, выделяя эквивалентное количество ионов кальция, всегда присутствующих в техническом волокне. Здесь следует отметить, что очень часто явление обмена обусловлено не самим веществом адсорбента, а содержащимися в адсорбенте незначительными примесями.
Обменная адсорбция широко применяется при умягчении воды. Как известно, наличие в воде больших количеств солей жесткости (ионов Са2+ и Mg2+) очень часто затрудняет применение такой воды в технике. Мыла в жесткой воде переходят в форму нерастворимых кальциевых и магниевых мыл и теряют свое моющее и стабилизующее действие. Применение жесткой воды в паровых котлах приводит к образованию на их стенках накипи, понижающей теплопроводность и увеличивающей потери тепла, а в отдельных случаях может явиться причиной взрыва котла (из-за местного перегревания и постепенного изменения структуры металла). Пища, сваренная в жесткой воде, обычно безвкусная и твердая. Для умягчения жесткой воды Ганс предложил применять алюмосиликатный поглотитель, названный им пермутитом, состав которого можно выразить следующей формулой:
Na2O.Al2O3.3SiO2.2H2O
В настоящее время вместо относительно дорогого пермутита натрия для умягчения воды применяют также природные минералы – глаукониты.
Глауконит – минерал, силикат сложного состава. Встречается обычно в виде мелких зерен зеленого цвета, главным образом в морских песчаниках и известняках. Образуется на шельфе на глубинах 200–300 м. Широко используется для определения изотопного возраста горных пород калий-аргоновым методом.
Умягчение жесткой воды с помощью пермутита можно пояснить следующей схемой:
![]()
Пермутит, обменявший Na+ на Са2+, в согласии с законом действия масс, можно снова легко регенерировать путем обработки концентрированным раствором поваренной соли. При этом ионы Na+ вытесняют ионы Са2+ в раствор, и после промывки пермутит снова пригоден для применения. Нетрудно видеть, что обработка жесткой воды пермутитом ведет к ее умягчению, но не к деминерализации.
В последние годы вместо пермутита и глауконитов для умягчения воды широко применяют ионообменные смолы и цеолит.
Обменная адсорбция используется также для улавливания ценных веществ из чрезвычайно разбавленных растворов, из которых выделять эти вещества другими методами нерентабельно. Таким образом, можно регенерировать, например, медь из рудничных вод и сточных вод производства искусственного медноаммиачного шелка; серебро из сточных вод фабрик, изготовляющих кинопленку; хром из электролитических хромовых ванн и т. д. Обменная адсорбция применяется при извлечении из растворов радиоактивных элементов.
Наконец, на обменной адсорбции основано также точное установление эквивалентной точки при титровании растворов в аналитической химии. Например, если раствор хлорида натрия титровать в присутствии флуоресцеина нитратом серебра, то пока в растворе имеется хотя бы небольшой избыток хлорида натрия, на поверхности образующихся кристаллов AgCl будет возникать двойной электрический слой, состоящий из ионов Сl– и ионов Na+. В результате этого выделяющийся осадок будет белым, а раствор имеет желто-зеленую окраску. Однако как только в растворе окажется небольшой избыток нитрата серебра, на поверхности кристаллов AgCl образуется уже двойной слой из ионов Ag+ и NО3–. Так как окрашенный анион флуоресцеина обладает большой адсорбционной способностью, он вытеснит из двойного электрического слоя ион NО3– и в результате этого осадок окрасится в желто-зеленый цвет, раствор же станет бесцветным. Такое изменение окраски наступает весьма резко, что позволяет легко устанавливать эквивалентную точку при титровании.
ФЛУОРЕСЦЕИН – оксиксантеновый краситель; оранжево-красные кристаллы, плохо растворимые в воде; применяется как кислотный краситель для окрашивания не текстильных материалов в жёлтый цвет, как адсорбционный и кислотно-основной индикатор, как трассёр при изучении направления движения подземных вод и др.
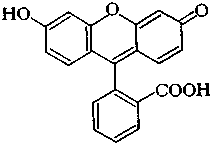
Флуоресцеин
Адсорбционные свойства цеолитов
Адсорбционный (PSA) принцип разделения газов
Принцип адсорбционного (Pressure Swing Adsorption) PSA получения азота основан на физических явлениях адсорбции и диффузии.
Каждый газ, содержащийся в воздухе, имеет свою адсорбционную величину, которая зависит от его физических свойств. По этому, для каждого из них применяется свой адсорбент. Для получения кислорода – синтетические цеолиты. Для получения азота – синтетические углеродные молекулярные сита (CMS).
Величины адсорбции азота и кислорода на углеродных ситах приблизительно одинаковы. Но скорость поглощения азота в десятки раз ниже скорости поглощения кислорода. Это связано с тем, что диаметр молекулы азота немного превосходит диаметр молекулы кислорода. При синтезе молекулярных сит подбирают такой диаметр входа в адсорбирующие поры, чтобы молекулы кислорода проникали в них легко, а молекулы азота – с затруднением. Разница в скоростях поглощения молекул кислорода и азота является основой для построения процесса очистки воздуха от кислорода.
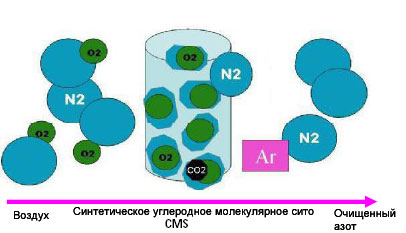
PSA процесс генерации азота можно представить так:
цикл процесса состоит не менее чем из двух стадий:
на первой из стадий («адсорбция») происходит поглощение адсорбентом кислорода с получением первого продукционного потока азота;
на второй стадии («регенерация») кислород выделяется из адсорбента и отводится в качестве второго продукционного потока;
процесс протекает при температуре окружающей среды;
в течение цикла происходят колебания давления с амплитудой от 3 до 10 атм.
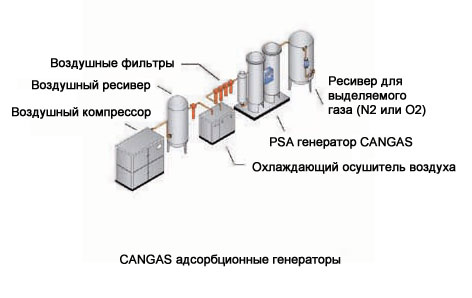
Для PSA получения кислорода из воздуха используется синтетический цеолит – (Zeolite molecular sieve) ZMS.
Величина адсорбции азота на цеолитах приблизительно в 2 раза выше, чем кислорода за счет отличий физических свойств молекул этих газов. Это дает возможность построить процесс очистки воздуха от азота и получение непрерывного потока кислорода
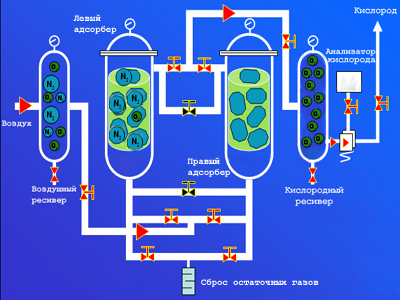
PSA процесс получения кислорода
Генератор состоит из двух адсорберов (обычно цилиндрические емкости), заполненных гранулированным цеолитом.
Очищенный от пыли и масла воздух под давлением 4~6 атм. проходит через один из периодически переключающихся электромагнитных клапанов в первый адсорбер.
Цеолит (Zeolite molecular sieve) ZMS поглощает преимущественно азот, а кислород проходит через слой адсорбента и через обратный клапан поступает в ресивер. В это же время во втором адсорбере происходит понижение давления и выброс накопленного азота. Кроме того, часть кислорода из первого адсорбера поступает через дроссельное устройство во второй адсорбер и дополнительно вытесняет из него накопленный азот.
Через время полуцикла адсорберы обмениваются своими функциями. Второй адсорбер задерживает азот и продуцирует кислород, а первый адсорбер освобождается от накопленного азота.
Такой цикл повторяется многократно. Извлеченный из воздуха концентрированный кислород накапливается в ресивере и может расходоваться в необходимых количествах.
Генератор полностью автоматизирован и работает без непосредственного участия человека.
Таким образом, генератор кислорода является, по сути, устройством очистки воздуха от азота циклического типа с автоматической регенерацией (восстановлением свойств) адсорбента в каждом цикле работы.