
- •Методические указания к практическим занятиям
- •Новороссийск
- •Классификация кислот
- •Названия кислот
- •Способы получения кислот
- •Производство серной кислоты контактным методом
- •Производство Азотной кислоты
- •Производство ортофосфорной кислоты
- •Производство соляной кислоты
- •1 Хлороводород; 2 вата.
- •Диссоциация кислот
- •Свойства кислот
- •Химические свойства
- •Нельзя вливать воду в концентрированную серную кислоту !!!
- •Кислые дожди (кислотные дожди, кислые осадки)
- •***Дополнительно***
- •Классификация кислородсодержащих кислот по их силе в водных растворах
- •Кислоты
- •Нельзя вливать воду в концентрированную серную кислоту !!!
- •Разложение нитратов при нагревании
- •Тривиальные названия химических соединений
- •Окраска пламени газовой горелки при внесении анализируемого вещества на предварительно прокаленной палочке или проволочке
- •Качественные реакции на катионы и анионы
- •Гидроксиды (основания)
- •Названия оснований
- •Классификация оснований
- •Получение оснований
- •Свойства оснований
- •Диссоциация оснований
- •Химические свойства
- •Дополнительно
- •Вопросы для подготовки к занятию
Производство ортофосфорной кислоты
Ортофосфорную кислоту получают:
1) взаимодействием оксида фосфора (V) с водой при нагревании:
P2O5
+ 3H2O
![]() 2h3po4
2h3po4
2) взаимодействием природной соли ортофосфата кальция с серной кислотой при нагревании:
Ca3(po4)2 + 3H2SO4 2h3po4 + 3CaSO4
Производство соляной кислоты
Соляную кислоту получают растворением хлороводорода в воде.
В лаборатории соляную кислоту можно получить в приборе, изображенном на рис. 6. При выполнении этого опыта следят, чтобы конец газоотводной трубки находился вблизи уровня воды, но не погружался в нее. Если это не учесть, то из-за большой растворимости хлороводорода вода попадает в пробирку с серной кислотой и произойдет сильное разогревание, в результате чего содержимое может быть выброшено из пробирки.
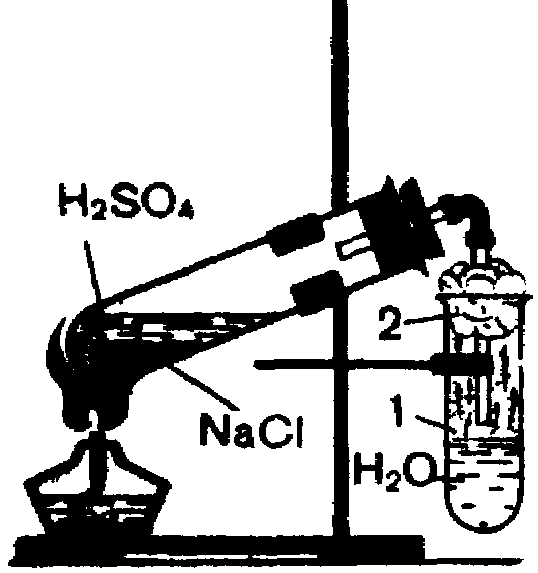
Рисунок 6 – Получение соляной кислоты в лаборатории:
1 Хлороводород; 2 вата.
В промышленности соляную кислоту получают сжиганием водорода в хлоре и растворением продукта реакции в воде. Для осуществления этих процессов пользуются установкой, схема которой изображена на рис. 7.
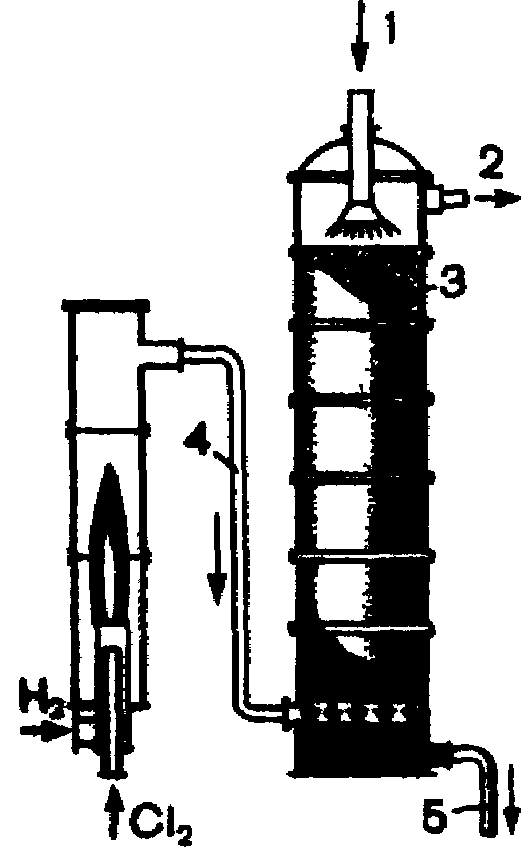
Рисунок 7 – Схема промышленной установки для получения соляной кислоты:
1– вода; 2– не поглощенные водой газы; 3 – керамические кольца;
4 – хлороводород; 5– соляная кислота.
Диссоциация кислот
Кислоты в водных растворах диссоциируют на ионы водорода и ионы кислотного остатка. Например:
HNO3 Н+ + NO3–
Многоосновные кислоты диссоциируют ступенчато:
H2SO4 Н+ + HSO4– 1ступень
кислый анион HSO4– образует кислые соли NaHSO4
HSO4- Н+ + SO4-2 2 ступень
SO4–2 образует средние соли Na2SO4
Диссоциация кислот по первой ступени протекает сильнее, чем по второй. Это связано с тем, что отщепление положительно заряженного иона Н+ от нейтральной молекулы происходит легче, чем от отрицательно заряженных ионов. Ступенчатая диссоциация многоосновных кислот обусловливает образование двух видов солей: кислых и средних.
Свойства кислот
Кислоты обладают общими свойствами (они нейтрализуют основания, окрашивают лакмус в красный цвет, при взаимодействии с металлами выделяют водород, имеют кислый вкус и др.), которые обусловлены положительно заряженными ионами Н+, образующимися при диссоциации. В свете теории электролитической диссоциации кислоты - это электролиты, которые при диссоциации в водных растворах в качестве катионов отщепляют только ионы водорода.
Химические свойства
1. Главное свойство всех кислот это взаимодействие с основаниями с образованием соли и воды (реакция нейтрализации):
НС1 + NaОН = NаС1 + н2О
Ионные уравнения:
Н+ + С1 + Na+ + ОН = Na+ + с1 + н2О
Н+ + ОН = н2О
Таким образом, сущность реакции нейтрализации раствора сильной кислоты раствором щелочи заключается в соединении ионов Н+ и ОН в недиссоциированные молекулы воды.
Слабая кислота, например, сероводородная, реагирует со щелочью потому, что продукт реакции вода, связывает ионы водорода более прочно, чем сероводородная кислотам
Н2S + 2NaOH = Nа2S + 2H2O
Ионные уравнения:
Н2S + 2Nа+ + 2ОН = 2Nа+ + S2 + 2Н2О
Н2S + 2ОН = S2 + 2Н2О
В зависимости от условий проведения реакции нейтрализации можно получить среднюю, кислую или основную соль. Так, если кислота и основание берутся в эквивалентных отношениях, то образуется средняя соль.
Ca(OH)2 + H2SO4 = CaSO4 + 2Н2О [CaSO4 – сульфат кальция]
Если в реакции нейтрализации многоосновная кислота берется в избытке, то образуется кислая соль.
Ca(OH)2 + 2H2SO4 = Ca(HSO4)2 + 2Н2О [Ca(HSO4)2 – гидросульфат кальция]
избыток
Кислую соль можно перевести в среднюю. Для этого ее нужно донейтрализовать. При донейтрализации тем же основанием, которое образует данную соль, получаем одну среднюю соль (а), а при донейтрализации другим основанием - две средние соли (б):
а) Ca(HSO4)2 + Ca(OH)2 = 2 CaSO4 + 2Н2О
б) Ca(HSO4)2 + 2NaOH = CaSO4 + Nа2SO4 + 2Н2О
Если в реакции нейтрализации многокислотное основание берется в избытке, то образуется основная соль.
2Ca(OH)2 + H2SO4 = (CaOH)2SO4 + 2Н2О
избыток гидроксосульфат
кальция
Основную соль можно перевести в среднюю. Для этого ее нужно донейтрализовать. При донейтрализации той же кислотой, которая образует данную соль, получаем одну среднюю соль (а), а при донейтрализации другой кислотой – две средние соли (б):
а) (CaOH)2SO4 + H2SO4 = 2CaSO4 + 2Н2О
б) (CaOH)2SO4 + 2HCl = CaSO4 + CaCl2 + 2Н2О
Иначе ведут себя Ni(OH)3 и Co(OH)3: при их взаимодействии с кислотами не образуются соли с Э3+, а происходит восстановление никеля и кобальта до Э2+, сопровождающееся выделением свободного кислорода или хлора (в отсутствие веществ способных окисляться):
4Ni(OH)3 + 4H2SO4 = NiSO4 + O2 + 10Н2О
2Ni(OH)3 + 6HCl = NiCl2 + Cl2 + 6Н2О
2. Кислоты взаимодействуют с металлами.
Все кислоты по действию на металлы условно делятся на кислоты-неокислители и кислоты-окислители.
Кислоты-неокислители – это кислоты, у которых роль окислителя выполняют ионы водорода, к ним относятся все бескислородные кислоты (HF, HCl, HBr, HI, H2S и др.), а также разбавленная серная, фосфорная, угольная, все органические кислоты и др. С кислотами-неокислителями реагируют металлы, которые в ряду стандартных электродных потенциалов (ряду напряжений) стоят до водорода (чтобы металл вытеснял водород из кислоты) и образуют с этими кислотами растворимые соли (чтобы на поверхности металла не образовалась защитная солевая пленка).
Zn + H2SO4 = Zn SO4 + Н2
разб.
Pb + H2SO4 ╪ т.к. Pb SO4 нерастворим
разб.
Cu + H2SO4 ╪ т.к. Cu стоит после Н2
разб.
Кислоты-окислители это кислоты, у которых роль окислителя выполняет центральный элемент кислотного остатка. К ним относятся азотная любой концентрации и концентрированная серная кислота. С кислотами-окислителями при нагревании реагируют все металлы (даже стоящие в ряду напряжений после водорода, кроме Au и Pt); металл окисляется при этом до характерной степени окисления и образует соль, а продукт восстановления кислоты зависит от активности металла и от степени разбавления кислоты (последнее характерно для HNO3). Взаимодействие металлов с кислотами-окислителями можно выразить следующей таблицей:
металлы |
HCl любая |
H2SO4 |
HNO3 |
|||
разбавлен. |
концентр. |
концентр. |
разбавлен. |
очень разб. |
||
активный металл (Li – Zn) |
Соль + H2 |
Соль + H2 |
Соль + H2O + H2S |
Соль + H2O + NO2* |
Соль + H2O + N2 (или N2O) |
Соль + H2O + NH4NO3 |
металл средней активности [Zn – (H2) ] |
Соль + H2 |
Соль + H2
|
Соль + H2O + S (или SO2) |
Соль + H2O + NO2 |
Соль + H2O+ N2O (или NO) |
Не реагирует |
неактивный металл (Cu – Ag) |
Не реагирует |
Не реагирует |
Соль + H2O + SO2 |
Соль + H2O + NO2 |
Соль + H2O + NO |
Не реагирует |
* для щелочных металлов N2O
Например:
Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O
конц.
4Mg +5H2SO4 = 4 MgSO4 + H2S + 4H2O
конц.
Некоторые металлы (Fe, Al, Cr) не взаимодействуют с концентрированной серной и азотной кислотами при обычной температуре (происходит пассивация металла). Это явление связано с образованием на поверхности металла тонкой оксидной пленки, которая и защищает металл. На этом свойстве основана транспортировка концентрированной H2SO4 в железных емкостях.
Если металл проявляет переменную степень окисления, то с кислотаминеокислителями он образует соли со степенью окисления ниже характерной (а), с кислотами-окислителями соли с характерной степенью окисления (б):
а) Fe + 2HCl = FeCl2 + Н2
б) Fe + 4HNO3 = Fe(NO3)3 + NO + 2H2O
разб.
Благородные металлы растворяются только в царской водке (смесь концентрированных азотной и соляной кислот):
Au + HNO3 + 3HCl = AuCl3 + NO+ 2H2O
3Pt + 4HNO3 + 12HCl = PtCl4 + 4NO+ 8H2O
3Ag + HNO3 + 3HCl = 3AgCl + NO+ 2H2O
При избытке HCl:
Au + HNO3 + 4HCl = H[AuCl4] + NO+ 2H2O;
золотохлористо-
водородная кислота
3Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO+ 8H2O;
платинохлористо-
водородная кислота
Ag + HNO3 + 2HCl = H[AgCl2] + NO+ H2O;
сереброхлористо-
водородная кислота
3. Кислоты реагируют с основными (а) и амфотерными (б) оксидами с образованием соли и воды:
а) MgO + H2SO4 = MgSO4 + H2O
б) Al2O3 + 6HCl = 2AlCl3 + 3H2O
4. Кислоты вступают в реакции обмена с солями, если образующаяся соль относится к нерастворимым веществам (а) или образующаяся кислота - к нерастворимым (б), слабым или непрочным кислотам (в)
а) AgNO3 + HCl = AgCl + HNO3
б) Na2SiO3 + H2SO4 = H2SiO3 + Na2SO4
в) Na2CO3 + 2HCl = 2NaCl + H2CO3


H2O CO2
5. Кислоты взаимодействуют с не металлами.
С кислотами-окислителями взаимодействуют углерод, сера, фосфор и др. (они выступают в роли восстановителя)
S + 2H2SO4 (конц) = 3SO2 + 2H2O
С + 2H2SO4 (конц) = СO2 + 2SO2 + 2H2O
3P + 5HNO3 + 2H2O = 3H3PO4 + 5NO
S + 2HNO3 = H2SO4 + 2NO
B + 3HNO3 (конц) = H3BO3 + 3NO2
Кремний с кислотами не взаимодействует ; подобно благородным металлам он растворяется в смеси концентрированных кислот (азотной и плавиковой):
3Si + 4HNO3 + 18HF = 3H2[SiF6] + 4NO + 8H2O
-
Индикатор
рН
Окраска
Метиловый оранжевый
3,1 – 4,0
красная – оранжево-желтая
Метиловый красный
4,2 – 6,4
красная – синяя
Фенолфталеин
8,2 – 10,0
нет – пурпурная

 кислоты
кислоты