
- •1 Оптическое излучение. Диапазон оптических волн.
- •2 Энергетические параметры оптического излучения
- •3 Световые параметры оптического излучения
- •4 Гипотеза планка квантовая теория света
- •5 Фотон энергия фотона
- •6 Масса фотона
- •7 Импульс фотона
- •8 Теория Бора о строении атома водорода. (постулаты Бора)
- •9 Гипотеза де Бройля. (волны де Бройля)
- •10 Особенности описания поведения микрочастиц (Волновой пакет).
- •11 Соотношения неопределенностей Гейзенберга
- •12 Волновая функция.
- •13 Уравнение Шредингера, его особенности
- •14 Амплитудная волновая функция. Амплитудное уравнение Шредингера.
- •15 Главное квантовое число
- •16 Орбитальное квантовое число
- •17 Магнитное квантовое число
- •18 Спиновое квантовое число
- •19 Принцип Паули
- •20 Квантовые переходы
- •22 Спонтанные квантовые переходы
- •23 Вынужденные квантовые переходы
- •24 Коэффициент Эйнштейна для вынужденных квантовых переходов
- •25 Оптические спектры
- •26 Ширина спектральной линии
- •27 Причины, приводящие к уширению спектральных линий
- •28 Спектр испускания и спектр поглощения
19 Принцип Паули
Применительно к системе электронов в атоме принцип Паули можно записать следующим образом:
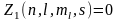 или 1, (28)
или 1, (28)
где  - число электронов находящихся в
состоянии, описываемом набором квантовых
чисел
- число электронов находящихся в
состоянии, описываемом набором квантовых
чисел
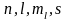 .
.
Пользуясь
принципом Паули, можно найти максимальное
число электронов в атоме, имеющих
заданные значения трех ( ),
двух (
),
двух (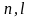 )
и одного (
)
квантовых чисел.
)
и одного (
)
квантовых чисел.
Найдем
максимальное число
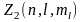 электронов, находящихся в состояниях,
определяемых набором трех квантовых
чисел (
),
т.е. отличающихся лишь ориентацией
спинов электронов. Так как число
может принимать лишь два значения, т.е.
электронов, находящихся в состояниях,
определяемых набором трех квантовых
чисел (
),
т.е. отличающихся лишь ориентацией
спинов электронов. Так как число
может принимать лишь два значения, т.е.
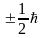 ,
то имеем
,
то имеем
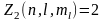 (29)
(29)
Вычислим
далее максимальное число электронов
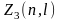 ,
находящихся в состояниях, определяемых
двумя квантовыми числами:
и
.
Так как при заданном числовом значении
вектор орбитального момента количества
движения
,
находящихся в состояниях, определяемых
двумя квантовыми числами:
и
.
Так как при заданном числовом значении
вектор орбитального момента количества
движения
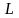 может иметь (
может иметь ( )
различных ориентаций в пространстве,
то число электронов равно
)
различных ориентаций в пространстве,
то число электронов равно
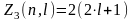 . (30)
. (30)
Значения для разных приведены в таблице 1.
Таблица 1
-
Значения орбитального
квантового числа
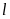
0
1
2
3
4
Символ соответствующего
состояния электронов
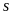
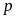
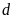
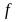

Максимальное число электронов

2
6
10
14
18
Наконец,
найдем, пользуясь принципом Паули,
максимальное число
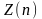 электронов, находящихся в состояниях,
определяемых значением
главного квантового числа (или кратность
вырождения). Так как
при заданном
изменяется от 0 до
электронов, находящихся в состояниях,
определяемых значением
главного квантового числа (или кратность
вырождения). Так как
при заданном
изменяется от 0 до
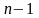 ,
то суммируя
по
от 0 до
,
то суммируя
по
от 0 до
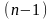 ,
получим
,
получим
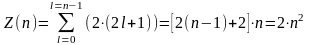 (31)
(31)
В таблице 2, составленной на основе предыдущих формул, приведены максимальные числа электронов, обладающих в атоме заданными значениями квантовых чисел.
Таблица 2
-
Заданные квантовые
числа
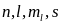
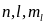
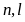

Максимальное число
электронов
1
2
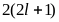
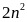
В таблице 3 приведены максимальные числа электронов, находящихся в состояниях, характеризуемых данными значениями и .
Таблица 3
-
Слой
Число электронов в состояниях
Максимальное число
электронов
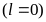
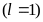
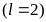

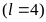
K
2
-
-
-
-
2
L
2
6
-
-
-
8
M
2
6
10
-
-
18
N
2
6
10
14
-
32
O
2
6
10
14
18
50
Принцип Паули сыграл выдающуюся роль в развитии современной атомной и ядерной физики. Так, например, удалось теоретически обосновать периодическую систему элементов Менделеева. Без принципа Паули невозможно было бы создать квантовые статистики и современную теорию твердых тел.
