
1.2.2 Растворы электролитов в случае электролитных растворов интерес представляют расчетные методы определения плотности смешанных растворов электролитов.
Расчеты
проводят по формуле, выведенной Г.И.
Микулиным, в соответствии с которой
плотность смешанного раствора электролитов
определяется через кажущиеся молярные
объемы
![]() электролитов
в смеси как сумма:
электролитов
в смеси как сумма:
 (11)
(11)
где ρ0 – плотность растворителя, Мi – молярная масса i-го электролита, сi – концентрация i-го электролита в смешанном растворе,
Для практического применения эту формулу удобно представить в виде
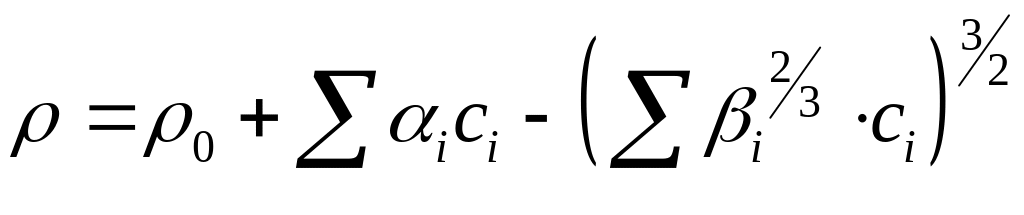 (12)
(12)
где
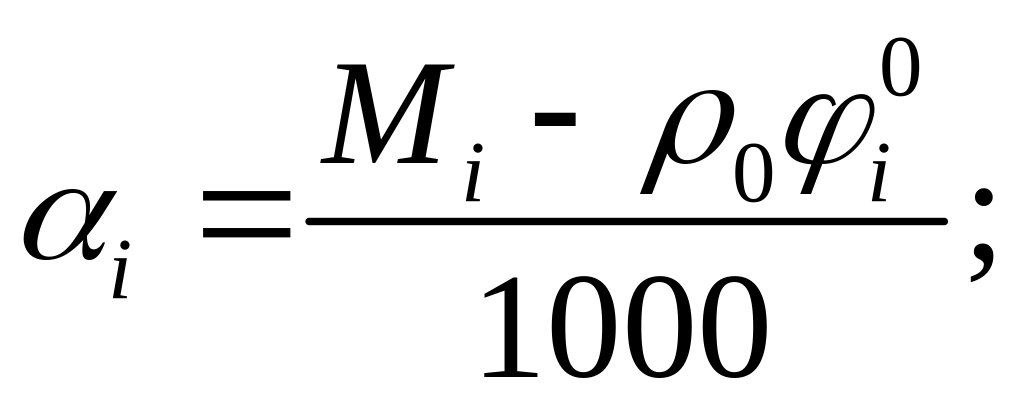
![]() .
.
Значения
констант
![]() и
и
![]() индивидуальны
для каждого электролита в данном
растворителе при данной температуре и
не зависят от присутствия других солей.
Поэтому значения этих параметров
находят из концентрационной зависимости
кажущегося молярного объема
индивидуальны
для каждого электролита в данном
растворителе при данной температуре и
не зависят от присутствия других солей.
Поэтому значения этих параметров
находят из концентрационной зависимости
кажущегося молярного объема
![]() i-го
электролита в его бинарном растворе
(имеется в виду раствор электролита в
данном растворителе), описываемой
уравнением Мэссона в виде
i-го
электролита в его бинарном растворе
(имеется в виду раствор электролита в
данном растворителе), описываемой
уравнением Мэссона в виде
![]() (13)
(13)
Значения рассчитывают по соотношению
![]() ,
(14)
,
(14)
где
V
– объем раствора;
![]() - молярный объем растворителя,
- молярный объем растворителя,
![]() и
и
![]() - числа молей растворителя и соли в
растворе.
- числа молей растворителя и соли в
растворе.
ЗАДАНИЕ 2
По данным о плотности водных растворов некоторых солей при 20 оС, приведенным в таблице 2, рассчитать плотность растворов двух солей следующего состава: А (8%) + В (16%).
А B
Вариант №1 NaCl + KCl;
Вариант №2 NaCl + LiCl;
Вариант №3 NaCl + NH4Cl;
А B
Вариант №7 KCl + NH4Cl;
Вариант №8 КCl + NaNO3;
Вариант №9 KCl + KNO3;
Вариант №4 NaCl + NaNO3;
Вариант №5 NaCl + KNO3;
Вариант №6 КCl + LiCl;
Вариант №10 LiCl + NH4Cl;
Вариант №11 LiCl + NaNO3;
Вариант №12 LiCl + КNO3.
1) Выразить состав растворов в шкале моляростей, мольдм–3;
2) рассчитать значения кажущихся мольных объемов φi солей в их индивидуальных растворах, см. ур. 14);
3)
построить зависимость
![]() и определить коэффициенты уравнения
Мэссона (ур. 13);
и определить коэффициенты уравнения
Мэссона (ур. 13);
4) рассчитать коэффициенты α и β.
5) по формуле (12) рассчитать плотность смешанного раствора. Плотность воды при 20 оС принять равной 1 г см–3. Качественный и количественный состав смешанного электролита указывает преподаватель.
Таблица 2. Значения плотности водных растворов солей при 20 оС (1 г/см3 ).
Масс.доля,% |
NaCl |
KCl |
LiCl |
NH4Cl |
NaNO3 |
KNO3 |
1 |
1,0053 |
1,0045 |
1,0041 |
1,0013 |
1,0049 |
1,0046 |
4 |
1,0268 |
1,0239 |
1,0215 |
1,0107 |
1,0254 |
1,0234 |
8 |
1,0559 |
1,0500 |
1,0444 |
1,0227 |
1,0532 |
1,0494 |
12 |
1,0857 |
1,0768 |
1,0675 |
1,0344 |
1,0819 |
1,0762 |
16 |
1,1162 |
1,1043 |
1,0910 |
1,0457 |
1,1118 |
1,1030 |
20 |
1,1478 |
1,1323 |
1,0150 |
1,0567 |
1,1426 |
1,1326 |
22 |
1,1640 |
1,1474 |
- |
- |
- |
- |
24 |
1,1804 |
1,1623 |
1,1399 |
- |
1,1752 |
1,1623 |
26 |
1,1972 |
- |
- |
1,0726 |
- |
- |
28 |
- |
- |
1,1658 |
- |
1,2085 |
- |
ЛИТЕРАТУРА
Фиалков Ю.Я., Житомирский А.Н., Тарасенко Ю.А. Физическая химия неводных растворов. – Л.: Химия, 1973. – 376 с.
Вопросы физической химии растворов электролитов. Под ред. Г.И. Микулина. – Л.: Химия, 1968. – 420 с.
