
- •Содержание
- •ВВедение
- •Техника безопасности
- •Работа 1 Техника лабораторных работ
- •Работа 2 методы очистки веществ
- •Перекристаллизация
- •Возгонка
- •Перегонка
- •Очистка газов
- •Экспериментальная часть
- •Вопросы к допуску
- •Работа 3 Определение эквивалента простых и сложных веществ
- •Вопросы к защите
- •Работа 4 определение атомных и молярных масс
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 5 классы неорганических соединений и периодическая система элементов. Типы химических реакций
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 6 Комплексные соединения
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 7
- •Теплоты химических процессов
- •Рассчитывают стандартную теплоту реакции на основе следствий из закона Гесса.
- •Опыт1. Определение теплоты гидратации карбоната натрия
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 8 скорость химических реакций. Химическое равновесие. Катализ
- •Опыт1. Зависимость скорости реакции от концентрации реагирующих веществ
- •Опыт 2. Зависимость скорости реакции от температуры
- •Опыт 3. Гомогенный катализ
- •Опыт 4. Скорость гетерогенных химических реакций
- •Опыт 5. Смещение химического равновесия при изменении концентрации реагирующих веществ
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 9 Приготовление растворов заданной концентрации
- •Способы выражения количественного состава растворов
- •Приготовление растворов с заданной массовой долей вещества а) из твердого вещества и воды
- •Б) из концентрированного раствора и воды
- •В) Смешивание двух растворов с различной массовой долей вещества
- •2. Приготовление растворов определенной молярной и молярной концентраций эквивалента. А) из твердого вещества и воды.
- •Б) из концентрированного раствора и воды
- •Вопросы к допуску
- •Вопросы к защите
- •Работа 10 Реакции в растворах электролитов
- •Вопросы допуска
- •Вопросы к защите
- •Вопросы допуска
- •Вопросы к защите
- •Вопросы допуска
- •Вопросы к защите
- •Литература
Вопросы к защите
1. Каким из приведенных методов можно определить химический эквивалент золота, которое непосредственно с водородом и кислородом не соединяется и не вытесняет водород из кислот.
а) метод вытеснения водорода; б) метод прямого определения;
в) аналитический метод; г) электрохимический метод.
2. Молярная масса эквивалента азота (г/моль) в соединении NO2 равна:
а) 4,66; б) 7; в) 3,5; г) 6.
3. Молярная масса эквивалента азота в соединении NхOу равна 2,8 г/моль. Определите это соединение:
а) N2O; б) NO; в) N2O3; г) NO2; д) N2O5.
4. Молярная масса эквивалента гидроксида висмута (г/моль) в реакции Bi(OH)3 + HNO3 = Bi(OH)2NO3 + H2O. равна
а)259,98; б) 129,99; в) 86,66 г.
5. Молярная масса эквивалента фосфорной кислоты (г/моль) в реакции H3PO4 + Ca(OH)2 = CaHPO4 + 2H2O.равна:
а) 49; б) 98; в) 32,67.
6. Молярная масса эквивалента соли NaHSO4 в следующей реакции равна:
NaHSO4 + BaCl2 = BaSO4 + NaCl + HCl.
а) 0,5-, б) 0,25-, в) 1-, г) 2- молярных масс.
7. 0,05 г металла вытесняют из кислоты 28 мл водорода (н.у.). Чему равна молярная масса эквивалента металла (г/моль)?
а) 5; б) 1; в) 15; г) 20; д) 25.
8. Сколько оксида получится при окислении 3 г металла, молярная масса эквивалента которого равна 12 г/моль?
а) 3; б) 6; в) 5; г) 10; д) 12.
9. Какой объем займёт (при н.у.) 1 моль эквивалента кислорода
а) 5,6 л; б) 2,8 л; в) 44,8 л; г) 22,4 л.
10. Какой объем займёт (при н.у.) 1 моль эквивалента водорода:
а)11,2л б)22,4 в)44,8 г)20л
Работа 4 определение атомных и молярных масс
Чтобы определить молекулярную массу вещества обычно находят численно равную ей молярную массу вещества в г/моль.
Масса молекул, выраженная в атомных единицах массы, называется относительной молекулярной массой. Атомная единица массы – это 1/12 часть массы атома самого легкого природного изотопа углерода 12С. Молярная масса это масса одного моль вещества. Моль-это количество вещества, в котором содержится столько же структурных единиц, сколько их содержится в 0,012 кг изотопа углерода 12с.
Экспериментальное определение молярной массы газообразных веществ основано на применении закона Авогадро и следствий из него. Молярная масса может быть определена даже и в том случае, если состав исследуемого соединения неизвестен.
Используют следующие методы:
1. Определение молярной массы газообразных веществ на основании молярного объема
2. Определение молярной массы газа по относительной плотности (по водороду или воздуху)
3.Определение молярной массы по его весу и объему.
Опыт. Определение молярной массы углекислого газа
Углекислый газ получите, используя прибор из аппарата Киппа (1), двух промывных склянок (2, 3) и плоскодонной колбы (4). (см рис).
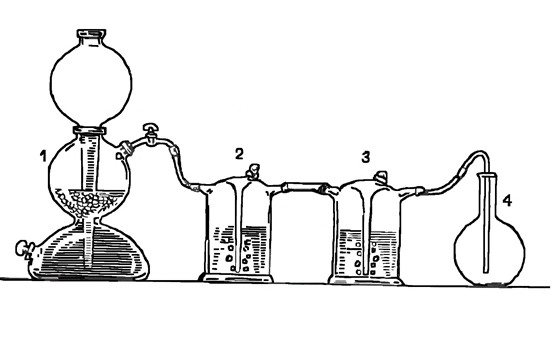
Рис. Прибор для определения молярной массы углекислого газа
Для определения молярной массы углекислого газа возьмите сухую плоскодонную колбу ёмкостью 250 мл с хорошо пригнанной резиновой пробкой. При помощи карандаша по стеклу сделайте отметку на стёклышке колбы в том месте, где кончается пробка. Взвесьте с точностью до 0,01 г колбу с пробкой. При заполнении колбы углекислым газом газоотводную трубку аппарата Кипа опустите до дна колбы. Когда колба заполнится углекислым газом (как это можно проверить?), медленно (почему?) выньте газоотводную трубку, закройте колбу пробкой и взвесьте. Заполнение колбы углекислым газом произведите несколько раз, до тех пор, пока не будет достигнута постоянная масса. Определите объём колбы, наполнив её водой до метки. Отметьте температуру и давление.
Экспериментальные данные
Масса колбы с воздухом – m1, г
Масса колбы с углекислым газом – m2, г
Атмосферное давление (по барометру) – Р, мм.рт.ст.
Температура – t, C
Объём колбы при условиях опыта – V1, мл
Порядок расчёта
Объём воздуха в колбе при н.у. – V0, мл
Масса воздуха в объёме колбы – m3, г
(масса 22,4 л воздуха при н.у. равна 29 г)
Масса пустой колбы (стекло и пробка) – m4, г
Масса углекислого газа в объёме колбы – m5, г
Относительная плотность углекислого газа по воздуху – DВ(CO2)
Молярная масса углекислого газа –M(CO2)
(рассчитать по уравнению Менделеева-Клапейрона или по относительной плотности по воздуху, или используя следствие из закона Авогадро)
Абсолютная и относительная ошибки опыта – г/моль; %
