
- •Структура объектов системы нефтепроводного транспорта
- •1. Классификация магистральных нефтепроводов и нефтепродуктопроводов
- •2. Состав сооружений магистральных нефтепроводов и нефтепродуктопроводов
- •Физико-технические свойства нефтей и их поготовка к транспорту
- •3.Состав нефтей и их классификация
- •4. Физико-химические свойства нефтей
- •5. Подготовка нефти к транспорту
- •6. Прием-сдача нефтей определенного качества
- •Насосы для перекачки нефтЕй и нефтепродуктов
- •7. Нефтяные центробежные насосы
- •8. Принцип действия центробежного насоса
- •9. Гидравлические q-h зарактеристики центробежных насосов. Измененение насосных характеристик
- •11. Изменение насосных характеристик
- •12. Привод насоса. Выбор привода
- •13. Теоретический напор, мощность и к.П.Д центробежных насосов, коэффициент быстроходности цбн (основные рабочие параметры)
- •14. Расчет характеристик цбн в зависимости от плотности и вязкости перекачиваемой нефти
- •15. Пересчет характеристик цбн при изменении числа оборотов
- •16. Регулирование подачи цбн
- •17. Работа цбн в группе
- •18. Определение мощности насосов для перекачки нефти
- •Технологический расчет магистральных трубопроводов при стационарном режиме перекачки
- •19. Закон Паскаля
- •20. Уравнение Дарси-Вейсбаха
- •21. Уравнение Бернулли. Определение полного напора в различных сечениях трубопровода
- •22. Исходные данные для технологического расчета
- •23. Расчет параметров транспортируемых нефтей
- •24. Определение коэффициента гидравлического сопротивления внутренней поверхности трубопровода
- •25. Гидравлический уклон. Определение полных потерь давления в трубопроводе
- •26. Уравнение баланса напоров в рельефном трубопроводе
- •27. Потери напора в трубопроводе с лупингами и вставками
- •28. Определение расчетной длины нефтепровода. Перевальная точка
- •29. Характеристики трубопровода, насоса, насосной станции
- •30. Совмещенная характеристика «трубопровод-насос». Рабочая точка
- •31. Подбор насосно-силового оборудования
- •32. Определение необходимого числа насосных станций
- •33. Расстановка нефтеперекачивающих станций по трассе нефтепровода
- •34. Расчет нефтепровода при заданном положении перекачивающих станций
- •35. Расчет коротких трубопроводов
- •36. Изменение подпора перед станциями при изменении вязкости нефти
- •37. Режим работы нефтепровода при отключении нефтеперекачивающих станций
- •38. Нефтепроводы со сбросами и подкачками
- •39. Методы увеличения пропускной способности нефтепровода
- •40. Методы снижения гидравлических потерь
- •42. Регулирование режимов работы трубопроводов изменением параметров трубопроводов дросселированием, байпасированием
- •43. Соотношение диаметров трубопроводов, давления и пропускной способности
- •44. Определение экономически наивыгоднейшего диаметра трубопровода
- •Основные требования к проектированию магистральных нефтепроводов
- •45. Расстояния между трубопроводами при подземной прокладке
- •46. Требования к расстановке запорной арматуры на магистральном нефтепроводе
- •47. Нормативная методика расчета трубопроводов на прочность
- •48. Основные нагрузки и воздействия на нефтепровод
- •49. Расчет толщины стенки трубопровода
- •50. Требования к трубам и марки сталей струб, применяемых при строительстве магистральных нефтепроводов
- •51. Требования к фасонным изделиям и соединительным деталям, применяемым на магистральных нефтепроводах
- •Противокоррозионная защита нефтепроводов и резервуаров
- •52. Классификация коррозионных процессов
- •53. Основные сведения об электрических процессах на поверхности трубопровода, находящегося в почве
- •54. Защитные покрытия нефтепроводов
- •55. Электрохимическая защита нефтепроводов от коррозии
- •56. Расчет длины защищаемого участка при катодной защите мн
- •57. Методы определения состояния коррозионной защиты нефтепроводов
- •58. Противокоррозионная защита резервуаров
- •Эксплуатация линейной части магистральных нефтепроводов
- •59. Утечки нефти из трубопровода и причины их возникновения
- •60. Расчет утечек нефти через отверстия в трубопроводе
- •61. Методы обнаружения утечек нефти из трубопровода
- •62. Определение места утечки по диспетчерским данным
- •63. Истечение нефтепродукта через отверстия в трубопроводах
- •64. Расчет утечек нефтепродукта через отверстия в трубопроводе (см. П.60 Расчет утечек нефти через отверстия в трубопроводе)
- •65. Планирование и расчеты периодических очисток нефтепровода от парафина
- •66. Внеплановая очистка нефтепровода от парафина и водяных скоплений
- •Технологические расчеты нефтепроводов при нустановившихся режимах
- •67. Инерционные свойства потока нефти
- •68. Гидравлический удар в нефтепроводах. Принципы расчета гидравлического удара
- •Перекачка нефтей с аномальными свойствами
- •69. Основные способы перекачки высоковязких и высокозастывающих нефтей и нефтепродуктов
- •70. Реологические свойства нефтей
- •71. Гидротранспорт вязких нефтей и нефтепродуктов
- •72. Перекачка термообработанных нефтей и нефтепродуктов
- •73. Перекачка нефтей с присадками
- •74. Перекачка предварительно подогретых нефтей и нефтепродуктов
- •75. Использование антитурбулентных присадок к нефтепродуктам для снижения потерь напора на трение
- •76. Зависимости основных параметров нефти от концентрации разбавителя
- •77. Вычисление давления насыщенных паров смеси
- •78. Вычисление гидравлических потерь при перекачке с разбавителем
- •79. Гидравлическая характеристика трубопровода при перекачке разбавленной нефти
- •Применение противотурбулентных присадок в трубопроводном транспорте нефти и нефтепродуктов
- •80. Эффект Томса
- •81.Применение противотурбулентных присадок на отечественных нефтепроводах
- •82. Технология ввода присадки в поток в трубопровод
- •83. Механизм действия малых полимерных добавок на поток в трубопроводе
- •107. Классификация нефтебаз
- •108. Номенклатура и основные эксплуатационные характеристики нефтепродуктов, с которыми оперируют нефтебазы
- •109. Физико-химические свойства нефтепродуктов
- •110. Операции, проводимые на нефтебазах
- •111. Объекты нефтебаз и их размещение
- •112. Определение объема резервуарного парка нефтебазы
- •113. Коэффициент оборачиваемости резервуаров
- •114. Резервуары нефтебаз и перекачивающих станций
- •115. Типы резервуаров и их конструкции
- •116. Оптимальные размеры вертикальных стальных резервуаров
- •117. Потери нефти и нефтепродуктов
- •118. Классификация потерь нефти и нефтепродуктов
- •119. Упрощенная теория потерь нефтепродуктов от испарения
- •120. Мероприятия по сокращению потерь от испарения
- •121. Современные средства сокращения потерь бензинов от испарения
53. Основные сведения об электрических процессах на поверхности трубопровода, находящегося в почве
Согласно теорий электрохимической коррозии разрушение металла обусловлено работой множества короткозамкнутых гальванических элементов, образующихся вследствие неоднородности среды и металла. При работе коррозийного элемента уменьшается разность начальных потенциалов, что сопровождается уменьшением коррозионного тока. Этот процесс называется поляризацией. Различают анодную и катодную поляризацию. При анодной поляризации в случае усиленного растворения металла ионы металла медленнее переходят в раствор, чем электроны отводятся в катодную область, и у поверхности электрода накапливаются положительные ионы металла, потенциал анода смещается в сторону положительных значений. Катодная поляризация сопровождается смещением потенциала электрода в отрицательную сторону и вызывается в основном малой скоростью электрохимической реакции соединения деполяризаторов с электронами. Участки, на которых растворяется металл, называются анодными, на них ион-атомы железа переходят в раствор, а на катодных - ток выходит в грунт. Электрохимические процессы на аноде и катоде различны, но взаимосвязаны, и, как правило, самостоятельно не протекают. Такая связанная система называется коррозионным микроэлементом. На анодных участках осуществляется окисление с образованием ионов металла Fe2+ а на катодных под влиянием кислорода образуется гидроокись (в результате кислородной деполяризации).
O2+2H2O+4e=4(OH-) (1)
Ионы железа и гидроксила взаимодействуют и образуют нерастворимый осадок Fe(ОН)2, который разлагается на окись железа и воду:
Fe(ОН)2 —> Fe2O3 + Н2О. (2)
Высвобождающиеся при окислении электроны от анодного участка по металлу изделия протекают к катоду и участвуют в реакции восстановления, рис. 1.
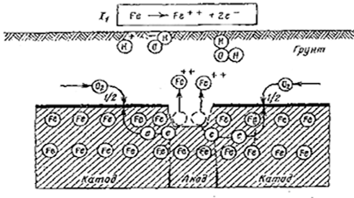
Рис. 1. Гальванический коррозионный элемент. Схема взаимодействия стали и почвенного электролита
В некоторых случаях возможны сложные процессы коррозии при одновременном воздействии двух или более факторов. К ним относятся коррозия под напряжением, щелевая, коррозионная эрозия, коррозионная кавитация. Скорость коррозионных процессов зависит от многих факторов, связанных как со свойствами, составом и строением металлического материала, так и со свойствами среды и внешними воздействиями. Для стальных трубопроводов, уложенных в грунт, скорость разрушения зависит во многом от коррозионности грунта, в частности, от типа грунта, состава и концентрации веществ, содержания влаги, проникновения воздуха в грунт, структуры грунта, температуры и удельного сопротивления грунта, наличия в грунте бактерий, активизирующих коррозионные процессы. Оценивается коррозионная активность грунта по величине его удельного электросопротивления (чем меньше , тем выше степень коррозии). Важной характеристикой грунта является и водородный показатель рН среды (увеличение скорости коррозии при уменьшении рН).
На интенсивность коррозии оказывает влияние неоднородность металла, механические напряжения, температуры и т.д. Неоднородность металла приводит к появлению коррозионных микроэлементов (микропар) в местах соприкосновения грунтов, или в месте изменения физических свойств грунта. Коррозия может произойти и при образовании микропары из-за наличия макровключений – окалины, царапины, вмятины, наклепа, поперечных продольных сварных швов макроструктурной неоднородности физико-химических свойств почв, (например, при неоднородном поступлении кислорода к поверхности трубопровода, расположенном под полотном дороги). Существенное влияние на скорость коррозии оказывает жизнедеятельность анаэробных бактерий, особенно в почвах, содержащих большее количество сульфатных солей. В этом случае происходит образование серной кислоты и усиление коррозионных процессов.
