
- •Практичне заняття № 8
- •До виконавчих структур належать:
- •Кінцевим наслідком нормальної функції системи виділення є підтримка гомеостазу.
- •Мал. 1. Будова нирки: 1 — капсула; 2 — чашечка; 3 — кіркова речовина; 4 — піраміди мозкової речовини; 5 — сечовід; 6 —ниркова миска; 7 — нирковий нерв; 8 — артерія; 9 — вена
- •Мал. 2. Будова нефрона (короткого - кіркового):
- •Мал. 4. Будова фільтраційної мембрани ниркового тільця:
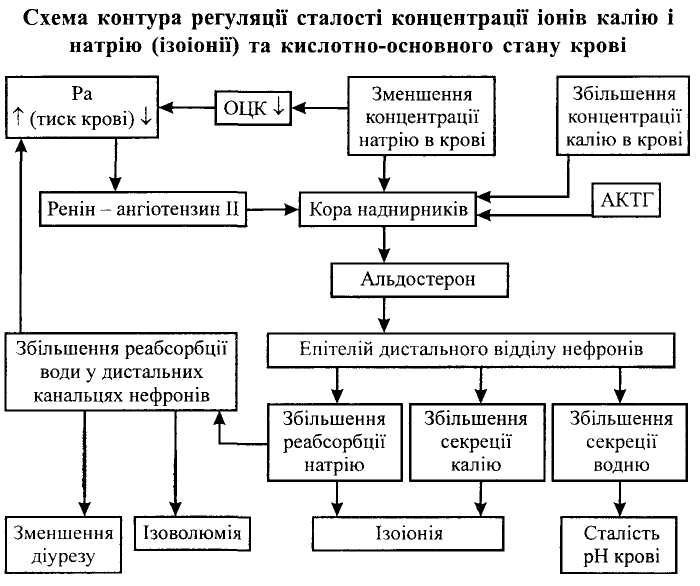
- •• Участь нирок у підтримці сталості концентрації іонів (ізоіонії) та об'єму циркулюючої крові (ізоволюмії)
• Участь нирок у підтримці сталості концентрації іонів (ізоіонії) та об'єму циркулюючої крові (ізоволюмії)
Регуляція сталості концентрації іонів натрію і калію у внутрішньому середовищі здійснюється завдяки гормону кори наднирників альдостерону, який збільшує реабсорбцію натрію у дистальному відділі нефрона й одночасно збільшує секрецію іонів калію, а також іонів водню в умовах ацидозу.
Передсердний натрійуретичний пептид синтезується, зберігається й вивільнюється з кардіоміоцитів передсердь. Він збільшує виділення натрію з сечею (натрійурез), наслідком чого зменшення концентрації натрію в плазмі і збільшення діурезу, що призводить до зменшення об'єму циркулюючої крові.
Секрецію альдостерону клубочковою зоною кори наднирників стимулюють такі чинники.
Ангіотензин II. Утворення ангіотензину II відбувається завдяки секреції ферменту реніну юкстагломерулярними клітинами (ЮГК), які розташовані переважно у аферентній артеріолі і виконують функцію також механорецепторів: при зниженні кров'яного тиску в судині. Ренін перетворює ангіотензиноген плазми в ангіотензин І, останній перетворюється в ангіотензин II під впливом ангіотензинперетворюючого ферменту (АПФ), що продукується ендотелієм легеневих і ниркових капілярів.
Зменшення концентрації іонів натрію або збільшення концентрації іонів калію в плазмі безпосередньо стимулюють секрецію альдостерону корою наднирників.
А
 дренокортикотропін
(АКТГ) — гормон
аденогіпофіза, концентрація якого
збільшується при неспецифічній адаптації
організму до дії стресових факторів,
що призводить до збільшення об'єму
циркулюючої крові (ОЦК) завдяки збільшенню
реабсорбції води за осмотичним градієнтом
при збільшенні реабсорбції іонів натрію
під впливом альдостерону.
дренокортикотропін
(АКТГ) — гормон
аденогіпофіза, концентрація якого
збільшується при неспецифічній адаптації
організму до дії стресових факторів,
що призводить до збільшення об'єму
циркулюючої крові (ОЦК) завдяки збільшенню
реабсорбції води за осмотичним градієнтом
при збільшенні реабсорбції іонів натрію
під впливом альдостерону.
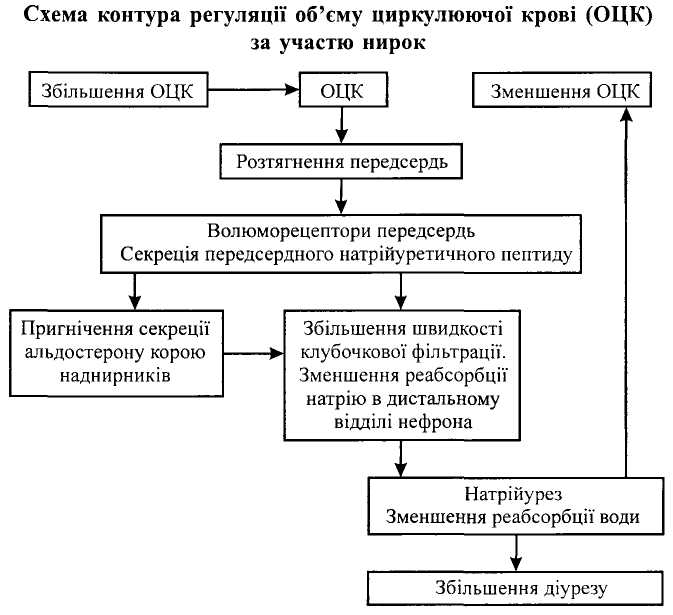
Секрецію передсердного натрійуретичного пептиду стимулюють такі чинники.
- Розтягнення передсердь внаслідок гіперволюмії (збільшення об'єму циркулюючої крові) завдяки підвищенню тиску крові в них
Передсердний натрійуретичний пептид збільшує натрійурез двома шляхами: а) збільшенням швидкості клубочкової фільтрації; б) пригніченням реабсорбції натрію в дистальному відділі нефрона. Наслідком останнього є зменшення реабсорбції води в дистальному відділі нефрона, збільшення діурезу та зменшення об'єму циркулюючої крові.
Регульованим параметром є об'єм циркулюючої крові (ОЦК), а слідкуючою ланкою контура регуляції є волюморецептори передсердь, завдяки чому з передсердь вивільнюється передсердний натрійуретичний пептид, завдяки якому відновлюється ОЦК.
Нирки крім своєї головної функції, що полягає у виведенні з крові продуктів обміну речовин, насамперед азотовмісних, а також деяких токсичних і сторонніх речовин екзогенного походження, виконують інші функції — гомеостатичні, які спрямовані на підтримання сталості внутрішнього середовища організму. До них належать осмо- та волюморегуляція, регуляція сольового складу і кислотно-основного стану крові й рідин тіла, регуляція артеріального тиску, а також внутрішньосекреторна та метаболічна функції тощо. Механізми більшості названих функцій було розглянуто вище (див. "Сечоутворення"). Тут ми детальніше зупинимося на їх ролі та значенні для організму в цілому.
Осмо- і волюморегуляторна функції. У процесі сечоутворення в канальцях нефрона відбувається інтенсивна реабсорбція води, об'єм якої залежить від ступеня гідратації організму. Звідси випливає, що нирки є основним органом осморегуляції.
Осморегуляція — це комплекс реакцій, що підтримують сталість осмотичного тиску внутрішнього (рідкого) середовища організму. Хоча основна роль у цих процесах належить ниркам, проте вони не можуть цілком забезпечити осморегуляцію. Нирки добре справляються з виведенням з організму зайвої води (коли працюють в режимі діурезу). Проте за нестачі води вони можуть лише економніше виводити воду з організму і навіть в режимі максимального антидіурезу продовжують виділяти воду.
Волюморегуляція. Регуляція об'єму позаклітинної рідини здійснюється, як правило, одночасно з регуляцією осмотичного тиску цієї рідини за тими самими механізмами. Гіпергідратація організму, спричинена водним навантаженням, супроводжується як зниженням осмотичного тиску крові й тканинної рідини, так і збільшенням їх об'єму. Такі зрушення усуваються зменшенням секреції вазопресину і посиленим виведенням води нирками.
За добу людина може випити залежно від умов і стану організму від 1 до 3 —5 л води і більше. Попри іноді величезні перевантаження водою, об'єм крові в організмі залишається сталим. Це пояснюється наявністю низки механізмів, що його контролюють. В основі ланцюга реакцій, що підтримують ці механізми, лежить чітка залежність: збільшення об'єму води в організмі спричинює її частковий перехід у кров і відповідно короткочасне збільшення її об'єму. А це, у свою чергу, зумовлює зростання систолічного об'єму крові і, як результат, підвищення артеріального тиску. Далі вмикаються різні ефекторні механізми, спрямовані на компенсацію порушення.
Барорецептори, які подразнюються в разі підвищення артеріального тиску, надсилають імпульси не тільки до судинорухового центру довгастого мозку, а й до гіпоталамуса. Там вони гальмують вироблення нейронами надзорового і пришлуночкового ядер вазопресину (антидіуретичного гормону), що, у свою чергу, зменшує факультативну реабсорбцію і збільшує виведення води з організму.
Волюморецептори, що знаходяться у стінках кровоносних судин і передсердь, також беруть участь у регуляції об'єму крові, їх подразнення у разі підвищеного тиску крові у венах, легеневій артерії, передсердях спричинює рефлекторне розширення периферичних судин і насамперед артеріол. Останнє зумовлює підвищення тиску в ниркових клубочках, збільшення фільтрації сечі і, як наслідок, зменшення об'єму крові.
Розтягання стінок передсердь при підвищенні артеріального тиску спричинює вироблення їх клітинами передсердного натрійуретичного фактора (атріопептину). Цей гормон у 5—10 разів посилює виведення нирками натрію й води з організму, відповідно зменшуючи об'єм крові. У регуляції об'єму позаклітинної рідини, в тому числі крові, беруть участь також ангіотензин-ІІ, альдостерон та деякі інші гормони.
Регуляція йонного складу крові. Відкриття натріорецепторів, які специфічно реагують на зміну концентрації лише йонів натрію, довело факт існування системи регуляції йонного складу крові і позаклітинної рідини. Ниркам у цій системі відводиться роль головного виконавчого органа. Затримуючи певні йони шляхом їх реабсорбції або посилюючи їх виведення з організму шляхом секреції, нирки відіграють головну роль в підтриманні йонного гомеостазу. Ця функція нирок контролюється переважно гуморальним шляхом. Найбільший і специфічний вплив на йонний склад крові і тканинної рідини чинять альдостерон, атріопептин та деякі інші гормони.
Альдостерон, гормон кори надниркових залоз, посилює реабсорбцію Na+ разом з С1- і секрецію К+. В результаті вміст і концентрація Na+ в плазмі крові зростають, а К+, навпаки, знижуються. Атріопептин, на відміну від альдостерону, гальмує реабсорбцію Na+ канальцями нефрона, посилюючи його виведення з організму. Це, у свою чергу, спричинює повніше виведення нирками аніонів (С1- і НСО3-) і води.
Паратирин (паратгормон), що синтезується і виділяється в кров прищитоподібною залозою, регулює рівень кальцію в крові, посилюючи його реабсорбцію в ниркових канальцях і кишках. Одночасно паратирин контролює рівень фосфатів, збільшуючи їх екскрецію нирками. Протилежний вплив на обмін кальцію здійснює гормон парафолікулярних ендокриноцитів (С-клітин) щитоподібної залози кальцитонін. Проте він діє позанирковим шляхом — знижує вміст Са2+ в крові за рахунок депонування його в кістках.
Регуляція кислотно-основного стану. Нирки відіграють чи не головну роль (після буферних систем крові) у підтриманні сталості реакції (рН) крові. Незважаючи на велику різноманітність харчових речовин, що споживаються і окиснюються в організмі, а також функціональних станів організму, рН крові і тканинної рідини залишається сталим, перебуваючи у дуже вузькому діапазоні — 7,35 — 7,4. Сталість цього показника забезпечується не тільки буферними системами власне крові, а й роботою нирок і легень, які виводять з організму зайві кислоти та луги. Про це яскраво свідчить широкий діапазон значень рН сечі — від 4,5 до 8, тобто концентрація Н+ в сечі може змінюватись у 1000 разів. Це залежить як від властивостей їжі, так і від рівня фізичного навантаження і стану дихальної системи, порушення якого можуть супроводжуватись респіраторним ацидозом або алкалозом.
Механізм секреції Н+ в канальцях нефрона описано вище. Подальші реакції, що відбуваються з Н+ в канальцях, такі: в міру зростання концентрації Н+ в канальцевій сечі він вступає в реакцію з натрію гідрогенкарбонатом, унаслідок чого утворюється карбонатна кислота і Na+:
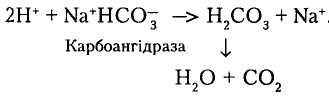
Новоутворені молекули води й вуглекислого газу видаляються через нирки і легені. Одночасно в канальцях нирок відбувається реакція водню з аміаком, який постійно утворюється в нефронах і дифундує в канальцеву сечу. Утворений при цьому йон амонію NH4+ зв'язується із С1- (див. мал. 6, б): і
![]()
Завдяки цьому концентрація NH3 і Н+ у канальцевій сечі зменшується, що сприяє подальшій дифузії новоутворених аміаку та Н+ в каналець, а також зменшенню кислотності сечі.
Метаболічна функція нирок полягає в перетворенні зайвих і відпрацьованих органічних сполук на такі речовини, які організм може використовувати в подальших процесах життєдіяльності.
Зокрема, нирки відіграють важливу роль у процесах глюконеогенезу — синтезу глюкози з органічних кислот. Якщо за нормальних умов кількість утворюваної в нирках глюкози приблизно дорівнює тій її кількості, що споживається ниркою для власних потреб, то під час голодування організму майже половина глюкози крові надходить у кров із нирок. Хоча основним депо глюкози і відповідно її джерелом в організмі є печінка, проте при перерахунку на одиницю маси цих органів нирки виробляють глюкози більше, ніж печінка.
У нирках відбувається також обмін ліпідів. Деяка частина вільних жирних кислот, що потрапили до канальцевої рідини шляхом секреції, в кірковій речовині нирки окиснюється, а виділена енергія витрачається на потреби органа. Решта жирних кислот перетворюється на жири і фосфоліпіди і в такому вигляді надходить у кров.
Крізь стінку клубочкових капілярів у порожнину капсули проникають переважно низькомолекулярні білки й пептиди. Певна частина їх реабсорбується у проксимальних канальцях, а решта розщеплюється в клітинах канальцевого епітелію до амінокислот, які знову повертаються у кров.
З одного боку, нирки таким чином виводять з організму метаболізовані й денатуровані білки, їх фрагменти, які є шлаками, що "засмічують" кров, а крім того, звільняють організм від зайвої кількості пептидних гормонів. З іншого боку, повертаючи у кров амінокислоти, нирки підтримують їх концентрацію в крові на сталому рівні.
Внутрішньосекреторна функція нирок. Нирки виробляють низку фізіологічно активних речовин, які впливають на функцію як власне нирок, так і інших органів та систем організму.
Еритропоетин — гормон глікопротеїдної природи, який стимулює вироблення еритроцитів кістковим мозком. Близько 90% еритропоетину утворюється в нирках. Стимулом для синтезу цього гормону є гіпоксична кров.
Ренін є пусковим компонентом ренінангіотензинової системи (РАС). Ця речовина хоч і виробляється спеціалізованими клітинами юкстагломерулярного комплексу і виділяється безпосередньо в кров, проте не є гормоном у повному розумінні. Ренін — це фермент, високоактивна протеаза, яка, діючи на білок плазми крові ангіотензиноген, започатковує утворення гормону ангіотензину-ІІ і виділення гормону надниркових залоз альдостерону. Перший є надзвичайно активним судинозвужувачем, а другий — регулятором обміну натрію і калію в організмі.
Кальциферол (віт. D) також не є гормоном, проте за фізіологічною дією він нагадує гормони. Тільки в нирках відбувається перетворення однієї з форм кальциферолу (віт. D3) на активну його форму — 1,25-дигідроксихолекальциферол, гормональна активність якого майже в 1000 разів вища, ніж усіх його попередників. Утворення холекальциферолу відбувається в клітинах проксимальних канальців нефрона за наявності паратирину. Дія холекальциферолу полягає в посиленні транспорту кальцію в кишках, а також у стимуляції остеобластів кісткової тканини, що відкладають кальцій у кістках.
Регуляція артеріального тиску. Нирки відіграють важливу роль у регуляції артеріального тиску, діючи як безпосередньо через зміни об'єму крові, так і гуморально — шляхом виділення гормонів, що впливають на судинний тонус.
Пряма дія. Підвищення артеріального тиску часто супроводжується посиленим сечовиділенням — пресорний діурез. Його механізм полягає ось у чому: підвищення артеріального тиску спричинює зростання кровотоку в судинному пучку (прямих судинах) мозкової речовини нирки, що збільшує "вимивання" натрію та сечовини з тканинної рідини нирки, знижуючи її осмолярність. Внаслідок цього зменшується реабсорбція води в збірних трубочках, збільшується кількість виділюваної нирками сечі, а об'єм крові та артеріальний тиск відповідно зменшуються. Зниження артеріального тиску, навпаки, зменшуючи кровотік у прямих судинах мозкової речовини, підвищує осмолярність її тканинної рідини і реабсорбцію води в збірних трубочках. В результаті до кровоносних судин повертається більше води і артеріальний тиск зростає.
Гуморальна дія. За допомогою РАС нирки активно підтримують об'єм крові та артеріальний тиск на сталому рівні. Крім того, вони виробляють фізіологічні речовини, що знижують артеріальний тиск. До судинорозширювальних речовин, виділюваних нирками, належать простагландини, кініни, а також нещодавно відкритий депресорний ліпід нирок.
Непряма дія. Під впливом низки гормонів нирки регулюють сольовий склад позаклітинної рідини. Будь-яка зміна співвідношення між Na+, K+ та Са2+ впливає на скоротливість міокарда, тонус кровоносних судин, що, у свою чергу, позначається на рівні артеріального тиску.
РЕГУЛЯЦІЯ ФУНКЦІЇ НИРОК
Регуляція водно-сольового обміну, в якому головна роль належить ниркам, спрямована на підтримання таких важливих гомеостатичних показників, як осмотичний тиск рідин внутрішнього середовища організму, співвідношення між К+ і Na+ в них, а також об'єму цих рідин в організмі. У процесі життєдіяльності згадані показники залежать від багатьох чинників, тому зрозуміло, що стабілізація їх повинна підтримуватись ефективними і точними регуляторними механізмами.
Нирки дуже чітко реагують на зміни кількості води в організмі — гіпер- та дегідратацію — відповідно збільшенням чи зменшенням кількості виділюваної сечі. Такі факти є переконливим доказом наявності ефективної системи регуляції сечоутворення. А оскільки відомо, що денервована нирка реагує на зміни водного режиму організму такими самими зрушеннями діурезу, як і інтактна, то уявлення про гуморальну регуляцію діяльності нирок виникло першим і стало загальновизнаним.
ГУМОРАЛЬНА РЕГУЛЯЦІЯ
Серед гуморальних чинників регуляції функції нирок слід виділити насамперед вазопресин, а також альдостерон, ренін-ангіотензинову систему та ін.
Вазопресин (антидіуретичний гормон, АДГ) — це гормон нейрогіпофіза. Він синтезується нейронами (нейросекреція) надзорового і пришлуночкового ядер гіпоталамуса, аксонами цих нейронів за допомогою білка-носія нейрофізину переноситься до задньої частки гіпофіза і вже звідти виділяється в кров. Механізм дії вазопресину полягає в активації гіалуронідази, яка, розщеплюючи гіалуронові комплекси міжклітинної речовини у стінках дистальних канальців та збірних трубочках, збільшує їхню проникність. Унаслідок цього значна кількість води виходить з кінцевих відділів нефрона в гіперосмотичну тканинну рідину нирки, а звідти у кров. Таким чином виконується режим антидіурезу і запобігається втрата води організмом.
Важливо зазначити, що в нормі вазопресин постійно виділяється в кров, підтримуючи певний рівень антидіурезу. Завдяки цьому внаслідок реабсорбції води з кожних 25—30 мл сечі, що надходять щохвилини до кінцевих відділів нефрона, до ниркової миски потрапляє всього 1 —1,2 мл кінцевої сечі. Хоча вазопресин діє лише на кінцеву частину нефрона і забезпечує реабсорбцію близько 20% води з канальців, важливість та ефективність його дії ілюструється такими фактами: у разі максимальної активізації антидіурезу добовий об'єм сечі зменшується до 300 — 500 мл, а за відсутності вазопресину в крові (гіпергідратація або патологія гіпоталамо-гіпофізарної системи) він досягає 8—10 л. Звичайно така поліурія супроводжується полідипсією — різким зростанням об'єму випитої рідини.
Стимулом для виділення в кров вазопресину є підвищення осмотичного тиску тканинної рідини і крові. Ця зміна сприймається центральними осморецепторами — нейронами надзорового і пришлуночкового ядер. Вони ж продукують вазопресин, а при збудженні посилають імпульси до гіпофіза щодо виділення гормону в кров. На вироблення і виділення нейронами цих ядер гормону впливають також периферичні осморецептори і натріорецептори, розміщені майже в усіх органах і тканинах. Їх подразнення підвищеною осмолярністю тканинної рідини діє, як і подразнення центральних осморецепторів, стимулюючи виділення вазопресину, який вмикає механізм максимальної економії води, при цьому зменшується її виведення з організму за рахунок посилення реабсорбції в нирках.
Звичайно, відновити в такий спосіб потрібний об'єм води і нормальний осмотичний тиск не можна. Цю функцію бере на себе розміщений у гіпоталамусі центр спраги, збудження якого зумовлює відповідне відчуття і поведінку, спрямовану на пошук і пиття води.
Протилежним до дії осморецепторів чином впливають на виділення вазопресину волюмо- і барорецептори кровоносної системи. Їх подразнення у разі збільшення об'єму крові чи підвищення артеріального тиску гальмує нейрони супраоптичного ядра і зменшує виділення гормону в кров. Реабсорбція води в канальцях нефрона та збірних трубочках зменшується, більше води виділяється нирками і відповідно зменшується об'єм крові в судинах, знижується артеріальний тиск.
Крім того, вазопресин звужує кровоносні судини. Зменшення його концентрації в крові призводить до розширення судин і зниження підвищеного артеріального тиску. За нормального артеріального тиску вазопресин на судини не впливає, оскільки ця його дія гальмується барорецепторними рефлексами.
Альдостерон, гормон кіркової речовини надниркових залоз, належить до групи мінералокортикоїдів, регулює виділення Na+ і К+ із сечею.
Виходячи з того, що в сечі міститься натрію менше, ніж у плазмі крові (табл. 1), можна зробити висновок, що в канальцевій системі нефрона цей йон реабсорбується, а не секретується. Основну роль у цьому процесі відіграють проксимальні канальці і петлі нефрона, на частку яких припадає 92% реабсорбованого натрію. Причому ці відділи нефрона постійно повертають більшу частину натрію назад у плазму крові. Що стосується решти (8%) натрію, то його реабсорбція цілком контролюється альдостероном. Якщо цього гормону немає, майже весь натрій, що залишився в канальцевій сечі, виводиться з організму. Це становить близько 20 г за добу. А за високого вмісту гормону в крові у дистальних відділах нефрона реабсорбується практично весь натрій сечі, виводитись з організму при цьому може всього 0,1 г натрію за добу.
Механізм дії альдостерону полягає у його проникненні в ядро епітеліальної клітини канальців нефрона, активації там ДНК-РНК-систем і синтезі клітиною білків — переносників йонів натрію.
Незважаючи на те що альдостерон здатний посилювати реабсорбцію натрію і збільшувати таким чином його кількість в організмі, концентрація Na+ у тканинній рідині й у крові практично не змінюється. Це пов'язано з тим, що одночасно з активною реабсорбцією Na+ збільшується пасивний перехід води з канальців в інтерстиціальну тканину нирки і в результаті зростає об'єм тканинної рідини і крові. Як наслідок, зростає артеріальний тиск, збільшується клубочкова фільтрація води і Na+, і все повертається до початкового стану. Складається враження, що дія альдостерону на регуляцію виділення нирками Na+ і води неефективна. Проте за дефіциту альдостерону організм втрачає натрій, хлор і воду, зменшується об'єм тканинної рідини, крові, через кілька днів може наступити смерть. Крім того, в тих відділах нефрона, на які впливає альдостерон, відбувається секреція К+, а ці два процеси взаємно пов'язані єдиним робочим механізмом — Na+-, К+-АТФ-азою, тобто альдостерон одночасно активізує обидва процеси.
Виділення альдостерону клубочковою зоною кори надниркових залоз здійснюється під безпосереднім впливом на її клітини низки чинників крові, насамперед концентрації калію. Її збільшення посилює синтез гормону і виділення його в кров, що, у свою чергу, спричинює збільшення секреції калію, виведення його з організму із сечею і одночасне зростання реабсорбції натрію й води та котранспорту інших йонів та речовин. Отже, альдостерон, діючи через нирки, регулює концентрацію електролітів у позаклітинній рідині, її об'єм та об'єм крові, артеріальний тиск, швидкість клубочкової фільтрації тощо.
Ренін-ангіотензинова система (РАС). Головним діючим чинником РАС є ангіо-тензин-ІІ. Ланцюг реакцій утворення ангіотензину-ІІ починається в юкстагломерулярному комплексі, клітини якого виробляють протеолітичний фермент ренін. Цей фермент розщеплює один з глобулінів плазми крові ангіотензиноген з утворенням ангіотензину-І. Останній під впливом ангіотензинперетворювального ферменту переходить у октапептид ангіотензин-П. Ангіотензин-П є одним з найпотужніших судинозвужувачів, свій вплив на функцію нирок здійснює через їхню судинну систему. Звужуючи кровоносні судини нирок і зменшуючи таким чином кірковий кровотік, ангіотензин-ІІ зменшує фільтрацію первинної сечі, одночасно збільшуючи реабсорбцію води і натрію. Крім того, цей пептид стимулює і виділення альдостерону, вплив якого на функцію нирок також полягає в посиленні реабсорбції натрію і води.
Стимулом для збільшеного виділення нирками реніну і запуску РАС є зниження артеріального тиску і погіршення ниркового кровопостачання. Так само активізується РАС подразненням симпатичних нервів або деяких ділянок гіпоталамуса. Як результат розвивається досить тривале підвищення артеріального тиску за рахунок двох різних механізмів. Перший з них, швидкий і короткотривалий (хвилини), зумовлений прямим судинозвужувальним впливом ангіотензину-П, а другий, повільний і довготривалий (години), пов'язаний зі зменшенням виведення нирками води й натрію і відповідним збільшенням об'єму тканинної рідини і крові.
Надмірна і тривала активізація РАС може призвести до розвитку ниркової форми артеріальної гіпертензії, яка усувається хірургічним шляхом — розширенням ниркової артерії, що забезпечує поліпшення кровопостачання нирок, або фармакологічним способом — введенням у кров антитіл до реніну чи до ангіотензинперетворювального ферменту.
Атріопептин. У стінках передсердь є клітини, які під впливом розтягання їх кров'ю виробляють специфічну речовину — передсердний натрійуретичний пептид, або атріопептин. Цей гормон, гальмуючи реабсорбцію Na+ у разі розтягання передсердь збільшеним об'ємом крові, посилює його виділення разом з водою та іншими йонами. Це єдиний гормон, що гальмує реабсорбцію Na+, хоча його дія спрямована не на мінеральний обмін, а на регуляцію об'єму циркулюючої крові.
НЕРВОВА РЕГУЛЯЦІЯ
Нирки як вісцеральний орган отримують подвійну — симпатичну і парасимпатичну — іннервацію.
Симпатична іннервація. Симпатичні нервові волокна відходять від 6-го грудного — 2-го поперекового сегментів спинного мозку і йдуть до нирок у складі черевних нервів. Перерізання ниркових гілок симпатичних нервів ніяк не позначається на функції та кровопостачанні нирок, проте подразнення цих нервів спричинює різке зменшення ниркового кровотоку і клубочкової фільтрації аж до повної зупинки обох процесів. Ці факти свідчать про те, що ниркові гілки симпатичних нервів тонічно не активні, але при збудженні відповідних центрів можуть звужувати судини нирок, головним чином приноспі клубочкові артеріоли кіркової речовини, зменшуючи й навіть припиняючи кровотік у нирках і зупиняючи таким чином утворення сечі. Подібне явище може відбуватися внаслідок стресу, больового подразнення, надмірного емоційного напруження тощо.
Пізнішими дослідженнями було встановлено, що симпатичні адренергічні нервові волокна шляхом активації аденілатциклази клітин канальцевого епітелію посилюють реабсорбцію Na+ і котранспорт інших йонів. Вони також впливають на функцію юкстагломерулярного комплексу, збільшуючи вироблення реніну.
Парасимпатична іннервація нирок здійснюється блукаючими нервами, гілки яких входять до нирок у складі ниркових нервів. Подразнення блукаючого нерва спричиняло як збільшення, так і зменшення діурезу і зміни швидкості екскреції Na+. Ці ефекти пов'язували головним чином зі змінами артеріального тиску, зумовленими подразненням блукаючих нервів. Тому більшість фахівців схиляються до думки, що ці нерви не чинять прямого впливу на функцію нирок. Проте останнім часом з'явились відомості про збільшення реабсорбції глюкози і секреції деяких органічних кислот під впливом парасимпатичної іннервації.
САМОРЕГУЛЯЦІЯ НИРОК
Відомо, що швидкість клубочкової фільтрації значною мірою залежить від швидкості кровотоку в нирках, зокрема від тиску крові в капілярах клубочків. Усі ці показники є досить сталими, незважаючи на значні коливання артеріального тиску — від 80 до 160 мм рт. ст. Оскільки ні симпатична, ні парасимпатична нервова система за умов спокою не впливає на внутрішньониркові судини, залишається припустити існування механізмів саморегуляції ниркового кровотоку і клубочкової фільтрації.
Провідну роль у процесах саморегуляції в нирках відводять юкстагломерулярному комплексу, зокрема щільній плямі. Слід нагадати, що щільна пляма — це видозмінені епітеліальні клітини дистального звивистого канальця нефрона (мал. 3). Вони реагують на зміни сольового складу вторинної сечі виробленням реніну та інших речовин, що впливають на судини клубочка. Розрізняють два механізми саморегуляції.
Механізм, що спричинює розширення приносної клубочкової (аферентної) артеріоли. Якщо з якихось причин, найчастіше внаслідок зниження артеріального тиску, клубочкова фільтрація зменшується, а реабсорбція солей не залежить від фільтрації, то це автоматично спричинює зменшення концентрації Na+ і СІ- в сечі дистального звивистого канальця і вироблення клітинами щільної плями речовин, що розширюють приносну клубочкову артеріолу. Швидкість кровотоку і фільтрація у клубочку зростають, повертаючись до початкового рівня.
Механізм, що спричинює звуження виносної клубочкової (еферентної) артеріоли. Така сама причина — зниження концентрації Na+ і СІ- в дистальному звивистому канальці, що сталося внаслідок зменшення кровотоку і фільтрації в клубочку, — через клітини щільної плями стимулює міоїдні ендокриноцити (юкстагломерулоцити) клубочкових артеріол до секреції реніну. Під впливом реніну в крові утворюється судиноактивний гормон ангіотензин-ІІ, який спричинює звуження виносної клубочкової артеріоли, внаслідок чого підвищується тиск крові в капілярах клубочка і відновлюється нормальна клубочкова фільтрація.
Обидва саморегуляторні механізми працюють за принципом негативного зворотного зв'язку і в разі збільшення клубочкової фільтрації гальмують свою активність.
СЕЧОВИПУСКАННЯ
БУДОВА СЕЧОВОГО МІХУРА
Зі збірних трубочок, що відкриваються на вершині пірамід, кінцева сеча надходить до ниркової миски, а звідти за допомогою скорочень гладкої мускулатури її стінок та перистальтичних рухів двох сечоводів — до сечового міхура.
Сечовий міхур є порожнистим органом, тонка стінка якого складається з трьох оболонок: слизової, м'язової і сполучнотканинної — серозної. Функція сечового міхура полягає в збиранні, накопиченні й виведенні сечі з організму. Місткість міхура дорослої людини становить 400 — 500 мл. М'язовий шар стінки сечового міхура складається з кільцевих і поздовжніх гладком'язових волокон, які у ділянці шийки і біля виходу утворюють м'яз — випорожнювач міхура. Від нижньої звуженої частини сечового міхура відходить сечівник з двома сфінктерами: внутрішнім, гладком'язовим, і зовнішнім, утвореним посмугованими м'язами.
Мал. 9. Іннервація сечового
міхура і сечівника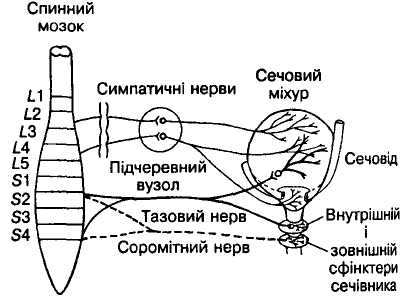
ІННЕРВАЦІЯ СЕЧОВОГО МІХУРА
Сечовий міхур і його сфінктери, на відміну від інших органів, отримують потрійну іннервацію: парасимпатичну, симпатичну і соматичну (мал. 9).
Парасимпатична іннервація. Пре-гангліонарні парасимпатичні волокна виходять із 2 — 4-го крижових сегментів спинного мозку і в складі тазового нерва підходять до сечового міхура. В його стінці розміщені тіла післявузлових нейронів, короткі аксони яких безпосередньо іннервують м'язові волокна стінки сечового міхура, м'яз — випорожнювач міхура і внутрішній замикач (сфінктер) сечівника. М'язові волокна цього сфінктера і нижньої частини м'яза — випорожнювача міхура розміщені таким чином, що, коли під час збудження парасимпатичних нервів м'яз скорочується, внутрішній сфінктер сечівника автоматично розкривається і відбувається сечовипускання.
Симпатична іннервація сечового міхура представлена післявузловими волокнами у складі підчеревного нерва, що відходить від однойменного нервового вузла, а останній отримує передвузлові волокна переважно від 2 —4-го поперекових сегментів спинного мозку. Донедавна вважали, що симпатичні нерви діють протилежно до парасимпатичних: закривають внутрішній сфінктер сечівника і розслаблюють м'яз -випорожнювач міхура, що сприяє наповненню сечового міхура. Проте, за останніми даними, ці функції здійснюються переважно міхуровим нутрощевим (вісцеральним) сплетенням після припинення збудження парасимпатичної іннервації. За симпатичними нервами залишається лише підтримання регуляції тонусу кровоносних судин сечового міхура.
Соматична іннервація представлена аксонами мотонейронів 2 — 4-го крижових сегментів спинного мозку, які в складі соромітного нерва підходять виключно до зовнішнього сфінктера сечівника. За допомогою цих волокон зовнішній сфінктер сечівника довільно відкривається і закривається, тобто здійснюється довільний контроль сечовипускання.
До складу перелічених нервів крім рухових входять також чутливі волокна, які несуть до ЦНС сигнали від механорецепторів стінки сечового міхура і сечівника. Ці аферентні сигнали відіграють головну роль у регуляції сечовипускання.
РЕФЛЕКТОРНА РЕГУЛЯЦІЯ СЕЧОВИПУСКАННЯ
У міру надходження сечі до міхура він розтягується, однак тиск у ньому і напруження його стінки змінюються мало, аж поки об'єм сечі в міхурі не досягне певного критичного рівня — близько 400 мл. При цьому напруження стінки і тиск у міхурі різко зростають і починається рефлекторне сечовипускання. Цей рефлекс виникає у відповідь на подразнення численних рецепторів розтягання у стінці сечового міхура. Імпульси від цих рецепторів через аферентні волокна тазового нерва надходять до крижових сегментів спинного мозку, де вони перемикаються на парасимпатичні нейрони. Аксони цих нейронів передають збудження до сечового міхура, чим викликають скорочення м'язів стінки міхура і розслаблення внутрішнього сфінктера сечівника.
Слід зазначити, що у людини міхурові рецептори подразнюються і спричинюють позиви до сечовипускання значно раніше — при наповненні міхура до 150 — 200 мл, а об'єм сечі 300 мл спричинює посилену імпульсацію до центра і викликає ритмічні скорочення стінки міхура, які через 20 — 40 с затухають і при подальшому збільшенні об'єму сечі в міхурі відновлюються. Гальмування рефлексу відбувається через вставні нейрони (нейрони Реншо), які здійснюють зворотне гальмування передвузлових парасимпатичних рухових нейронів спинного мозку.
Людина відчуває періодичні зростаючої сили позиви, які легко гальмуються вольовим зусиллям. І лише коли імпульсація з механорецепторів сечового міхура досягне критичної сили, відбувається гальмування крижових спинномозкових мотонейронів і розкриття зовнішнього сфінктера сечівника — починається сечовипускання. Цей процес триває до повного випорожнення сечового міхура завдяки рефлекторному подовженню процесу імпульсами з механорецепторів сечівника, подразнюваних струменем сечі, що витікає.
Замикання рефлексу сечовипускання відбувається на рівні спинного мозку. У молодих і дорослих організмів цей рефлекс замикається на рівні моста головного мозку і латентний період становить 80 — 120 мс. У людини, починаючи з трирічного віку, рефлекс сечовипускання контролюється вищими відділами ЦНС, зокрема корою великого мозку. Гальмуючи цей рефлекс, центри кори забезпечують довільну затримку сечовипускання, поки не з'являться певні умови для його реалізації. В останньому випадку вищі центри можуть посилювати рефлекс шляхом полегшення його замикання на крижовому рівні й гальмування мотонейронів, що іннервують зовнішній сфінктер сечівника.
