
- •III. Сопряженные системы с замкнутой цепью
- •1. Строение бензола
- •Современная теория строения бензола
- •Понятие ароматичности
- •Изомерия производных бензола
- •Полизамещенные производные бензола
- •2. Общий механизм реакций электрофильного замещения в
- •3. Влияние природы заместителей на направление реакций электрофильного замещения в бензольном кольце Ориентация замещения
- •Электроноакцепторные заместители
- •4. Ароматичность гетероциклических соединений
- •5. Основные термины.
- •6. Эталонное решение задач
- •Решение
- •Эталонное решение задач второго типа
- •Решение
- •Решение
- •Пространственное строение органических
- •Виды изомерии
- •Классификация изомеров.
- •2. Конформационная изомерия
- •Конформации циклических соединений
- •2. Конфигурационная изомерия
- •Проекционные формулы э. Фишера
- •Правила пользования проекционными формулами Фишера
- •4. Пространственное строение молекул и их биологическая активность
- •5. Основные термины.
- •6. Эталонное решение задач эталонное решение задач первого типа
- •Решение.
- •Эталонное решение задач второго типа
- •V. Углеводороды
- •Классификация углеводородов Углеводороды
- •1. Алканы Химические свойства (Sr-реакции)
- •Радикальное замещение у sp3 -гибридизованного атома углерода (sr - реакции)
- •Галогенирование высших алканов
- •Реакции окисления
- •2. Химические свойства циклоалканов
- •3. Электрофильное присоединение к алкенам и циклоалкенам (ае - реакции)
- •Какие экспериментальные данные могут служить доказательством такого механизма?
- •Присоединение водородсодержащих соединений к несимметричным алкенам
- •Реакции электрофильного присоединения против правила Марковникова
- •4. Электрофильное присоединение к диеновым
- •Реакции присоединения к 1,3 – бутадиену
- •Радикальное присоединение и электрофильное
- •5.1 Реакции присоединения (аr - реакции)
- •5.2 Реакции электрофильного замещения (se - реакции)
- •Химические свойства толуола
- •Нафталин в живом организме
- •6. Основные термины
- •7. Эталонное решение задач
- •Решение
- •1. Напишите реакции взаимодействия хлора с пропеном:
- •Решение
- •2. Присоедините бромоводород к следующим алкенам:
- •Решение
- •Решение
- •Решение
- •Эталонное решение задач третьего типа
- •Решение
- •Решение
- •Решение
- •Решение
- •Литература
- •Дополнительная.
Изомерия производных бензола
Так как в бензольном кольце электронная плотность выровнена и все атомы углерода равноценны, монозамещенные производные бензола изомеров не имеют.

Структуры I, II, III и IV не являются изомерами. Все эти соединения - бромбензол.
Двузамещенные производные бензола могут существовать в трех изомерных формах.
1. Два заместителя расположены у соседних атомов углерода бензольного кольца. В этом случае говорят, что заместители находятся в орто-положении относительно друг друга.

Все эти соединения имеют одно общее название -
1,2 –диметилбензол (орто-ксилол).
Поскольку кольцо симметрично, все изображенные выше наборы орто-положений равноценны.
2. Два заместителя в бензольном кольце разделены одним атомом углерода. Такие изомеры называют мета-изомерами.

Все эти производные бензола имеют одно общее название -
1,3–динитробензол (мета-динитробензол). Так как кольцо симметрично, все наборы мета-положений равноценны.
3. Два заместителя в бензольном кольце разделены двумя атомами углерода. Такие изомеры называют пара - изомерами.
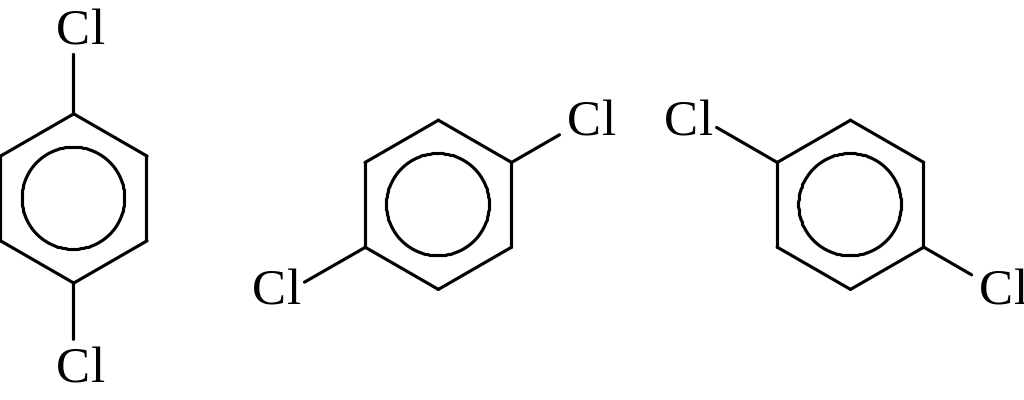
Эти производные бензола имеют одно общее название - 1,4-дихлорбензол (пара-дихлорбензол).
Вследствие симметричности кольца все три набора пара - положений равноценны.
Таким образом, в бензольном кольце по отношению к уже имеющемуся заместителю существует два орто-положения, два мета- положения и одно пара -положение
Обозначим Х любой заместитель в бензольном кольце, и рассмотрим, какие атомы углерода кольца можно рассматривать как орто-, мета- и пара- положения по отношению к этому заместителю, стоящему у разных атомов углерода.

Полизамещенные производные бензола
Если в бензольном кольце имеются три или более заместителей, их положение в кольце следует обозначать только с помощью цифр. Например,

1,2,4 - трибромбензол 1,3,5 - триметилбензол
2. Общий механизм реакций электрофильного замещения в
ароматическом ряду
Ароматический характер бензола диктует свои условия: реакции будут протекать достаточно легко, если не затрагивать стабильную ароматическую систему. Следовательно, это должны быть реакции замещения по связи С-Н. Учитывая нуклеофильный характер кольца, атакующим реагентом должен быть электрофил.
Здесь мы не будем
разбирать конкретные реакции
электрофильного замещения в ароматическом
ряду, а рассмотрим общую картину
механизма этого процесса, применяя
символ
![]() для обозначения
любой электрофильной частицы, атакующей
бензольное кольцо. (Подробно
эти реакции будут рассмотрены в главе
«Углеводороды»).
для обозначения
любой электрофильной частицы, атакующей
бензольное кольцо. (Подробно
эти реакции будут рассмотрены в главе
«Углеводороды»).
Все реакции в ароматическом ряду протекают по одному и тому же пути, и начинаются они с атаки электрофильной частицей ароматической -электронной системы.
В результате образуется -комплекс, в котором электрофил связывается с молекулой бензола за счёт всех его -электронов. Затем электрофильная частица вытягивает из ароматической шестёрки пару электронов, за счёт которой и образует σ-связь с кольцом, атом углерода при этом становится sp3-гибридизованным. Образуется σ-комплекс, в котором остальные четыре -электрона располагаются в две сопряжённые двойные связи, а атомы углерода остаются sp2-гибридизованными. Находящийся рядом с местом атаки положительный центр не остаётся безучастным к соседней системе π-электронов, и фактически -электроны "растекаются" по всем пяти атомам углерода. За счёт такой делокализации происходит стабилизация -комплекса, в котором положительный заряд рассредоточен почти по всему кольцу. Затем от sp3-гибридизованного атома углерода отщепляется протон, а электронная пара, за счёт которой он был привязан к бензольному кольцу, вливается в состав вновь образующейся ароматической шестерки электронов.

-комплекс σ-комплекс стабилизированный продукт
σ- комплекс SЕ -реакции
Е![]() -
электрофил
-
электрофил
По этому механизму протекают все процессы электрофильного замещения в бензольном кольце. Эти реакции подробно мы рассмотрим в главе "Свойства углеводородов".
