
- •III. Сопряженные системы с замкнутой цепью
- •1. Строение бензола
- •Современная теория строения бензола
- •Понятие ароматичности
- •Изомерия производных бензола
- •Полизамещенные производные бензола
- •2. Общий механизм реакций электрофильного замещения в
- •3. Влияние природы заместителей на направление реакций электрофильного замещения в бензольном кольце Ориентация замещения
- •Электроноакцепторные заместители
- •4. Ароматичность гетероциклических соединений
- •5. Основные термины.
- •6. Эталонное решение задач
- •Решение
- •Эталонное решение задач второго типа
- •Решение
- •Решение
- •Пространственное строение органических
- •Виды изомерии
- •Классификация изомеров.
- •2. Конформационная изомерия
- •Конформации циклических соединений
- •2. Конфигурационная изомерия
- •Проекционные формулы э. Фишера
- •Правила пользования проекционными формулами Фишера
- •4. Пространственное строение молекул и их биологическая активность
- •5. Основные термины.
- •6. Эталонное решение задач эталонное решение задач первого типа
- •Решение.
- •Эталонное решение задач второго типа
- •V. Углеводороды
- •Классификация углеводородов Углеводороды
- •1. Алканы Химические свойства (Sr-реакции)
- •Радикальное замещение у sp3 -гибридизованного атома углерода (sr - реакции)
- •Галогенирование высших алканов
- •Реакции окисления
- •2. Химические свойства циклоалканов
- •3. Электрофильное присоединение к алкенам и циклоалкенам (ае - реакции)
- •Какие экспериментальные данные могут служить доказательством такого механизма?
- •Присоединение водородсодержащих соединений к несимметричным алкенам
- •Реакции электрофильного присоединения против правила Марковникова
- •4. Электрофильное присоединение к диеновым
- •Реакции присоединения к 1,3 – бутадиену
- •Радикальное присоединение и электрофильное
- •5.1 Реакции присоединения (аr - реакции)
- •5.2 Реакции электрофильного замещения (se - реакции)
- •Химические свойства толуола
- •Нафталин в живом организме
- •6. Основные термины
- •7. Эталонное решение задач
- •Решение
- •1. Напишите реакции взаимодействия хлора с пропеном:
- •Решение
- •2. Присоедините бромоводород к следующим алкенам:
- •Решение
- •Решение
- •Решение
- •Эталонное решение задач третьего типа
- •Решение
- •Решение
- •Решение
- •Решение
- •Литература
- •Дополнительная.
Химические свойства толуола
.
Для толуола возможны 2 типа реакций:
1) SR - реакции по метильному радикалу,
2) SE -реакции по связи С – Н бензольного кольца.
Характер разрыва связей в реагенте определит тип реакций толуола (SR или SE).
1) Связь в реагенте разрывается гомолитически, образуется радикал, который не может атаковать связь С - Н бензольного кольца, так как эта связь легко разрывается при атаке электрофилом (редко нуклеофилом). Радикал может разрушить ароматическую шестёрку электронов и образовать производные циклогексана, но
этот процесс требует затраты большого количества энергии. Поэтому образовавшийся радикал будет атаковать связь С - Н метильной группы, образуя, в качестве промежуточной частицы, устойчивый бензильный радикал.
(Следует отметить, что алкильные группы, связанные с бензольным кольцом, несколько более реакционноспособны, чем алкильные группы, связанные с углеродным скелетом алканов.)
Рассмотрим реакцию взаимодействия толуола с хлором на свету.

Механизм этого
процесса: в молекуле хлора связь
разрывается гомолитически.
![]()
(реакция «а»)
Радикал хлора атакует метильную группу толуола, образуя устойчивый бензильный радикал.

(реакция «б») бензильный радикал.
Бензильный радикал, устойчив за счёт сопряжения неспаренного электрона с π-системой бензольного кольца.
Этот радикал далее взаимодействует с новой молекулой хлора. В молекуле хлора связь снова разрывается гомолитически; в результате этого процесса образуется бензилхлорид и появляется новый радикал хлора, который далее вновь вступает в реакцию с толуолом (реакция «б»).

бензилхлорид
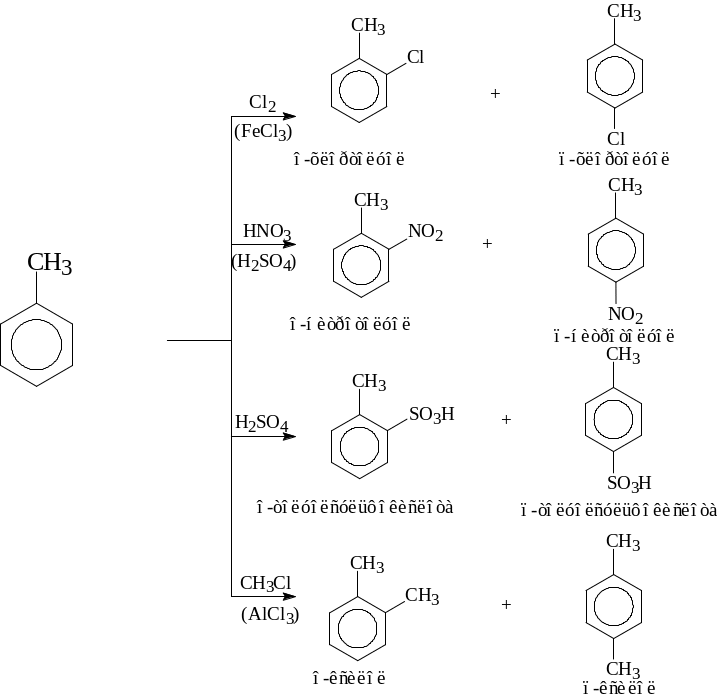
2) Связь в реагенте разрывается гетеролитически, образуются электрофил и нуклеофил. Для толуола характерны реакции электрофильного замещения. За счёт электронодонорного эффекта метильной группы, SE реакции протекают в достаточно мягких условиях, реагент, замещая атомы водорода бензольного кольца, вступает в орто- и пара- положения по отношению к метильной группе.
Следующая схема
иллюстрирует наиболее характерные для
толуола реакции электрофильного
замещения.
Нафталин в живом организме
Структурными фрагментами биологически активных веществ часто являются конденсированные углеводороды и их производные. Окружающая среда буквально "заражена" углеводородами. Источниками углеводородов в биосфере могут быть нефтяные озёра, газы, выделяющиеся в пещерах, шахтах и трещинах земной коры, разлагающиеся остатки животных и растений.
Способность животных метаболизировать некоторые углеводороды при введении их в организм в больших количествах навела некоторых учёных на мысль, что царство животных подвергалось действию этих углеводородов в течение многих тысяч лет. Характерным примером такого биологического процесса является способность крыс и кроликов превращать
нафталин в транс-1,2-дигидро-1,2-дигидроксинафталин.
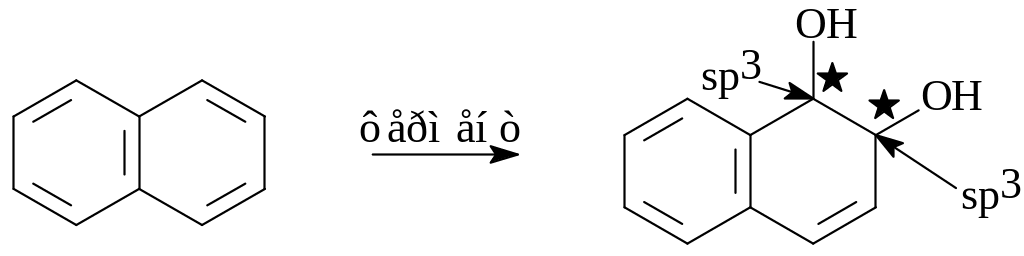
![]() отмечены хиральные
атомы углерода.
отмечены хиральные
атомы углерода.
Транс-1,2-дигидро-1,2-дигидроксинафталин может существо-вать в виде право- и лево- вращающих энантиомеров. Здесь хочется отметить такой любопытный штрих из области стереохимической специфичности действия ферментов: крысы образуют левовращаю-щий изомер, а кролики - правовращающий.
До недавнего времени ароматические углеводороды представляли интерес для биохимиков и фармакологов как потенциально канцерогенные вещества. Теперь, однако, оказалось, что ароматические углеводороды сами часто вовсе не являются канцерогенами. Существует предположение, что многие из этих углеводородов, попадая в организм, превращаются в эпоксиды.

1,2- эпоксинафталин
Именно эти эпоксиды либо сами вызывают рак, либо являются предшественниками действительных канцерогенов.
Благодаря многим интересным открытиям в этой области, химия эпоксидов ароматических углеводородов представляет большой интерес для исследователей, занимающихся поисками лекарств от рака.
