
- •Глава 1. Моющие средства
- •1.1. Краткая историческая справка.
- •1.2. Классификация
- •Глава 2. Поверхностно-активные вещества.
- •2.1. Строение молекул
- •2.4. Биохимическая разлагаемость пав
- •Глава 3. Косметико-гигиенические моющие средства.
- •3.1. Классификация
- •3.1.2. Мыло и моющие средства
- •3.1.3. Зубная паста
- •Глава 4. Синтетические моющие средства. 4.1 .Классификация
- •4.2. Основные компоненты и их назначение
- •4.3. Экологическая безопасность
- •Глава 5. Получение и анализ мыла
- •5.1. Производство мыла
- •5.2. Экспериментальная часть Реактивы, материалы и оборудование.
- •Методика проведения работы.
- •Вопросы на защиту:
- •Информация для лаборантов. Реактивы
- •Посуда, материалы
- •Оборудование
5.2. Экспериментальная часть Реактивы, материалы и оборудование.
Реактивы:
Известь гашеная Са(ОН)2,
Посуда:
конические колбы на 100 см3,
цилиндр мерный на 500 см3, либо мерная колба на 500 см3,
пипетки на 10 и 20 мл
бюретки
воронки для фильтрования
Материалы: фильтровальная бумага.
Оборудование: весы.
Методика проведения работы.
Цель работы: 1.1. Получениемыла из кулинарного маргарина.
1.2 Определение содержания жирных кислот в мыле.
1.3.Определение средней молекулярной массы жирной кислоты, полученной в работе (п. 1.2).
Реактивы: кулинарный маргарин, гидрооксид натрия, этанол, насыщенный раствор хлорида натрия, серная кислота, индикаторы:
метилоранжевый,фенолфталеин, дистиллированная вода.
Оборудование: фарфоровый стакан на 150 мл, колба на 100 мл, стеклянные палочки, химические весы, бюретка для титрования, фильтровальная бумага, электроплитка, штатив.
Ход работы
1.1.1. 6 г кулинарного маргарина расплавила в фарфоровом стакане.
Готовый спиртовой раствор NaOH добавила при перемешивании к расплавленному маргарину.
Полученный раствор кипятила в течение 15 мин. После кипячения добавила при помешивании 15 мл насыщенного раствора хлорида натрия и охладила на ледяной бане.
1.1.4. Извлекла образовавшийся на поверхности стакана слой мыла, высушила его и взвесила.
Массы мыла равна 6, 56 г. Масса полученного мыла из 6 г кулинарного маргарина превышает 100 %, т.к. мыло не очищено от глицерина и хлорида натрия.
5 г полученного мыла поместила в стакан емкостью 100 мл и добавила 50 мл дистиллированной воды, а затем нагрела на электроплитке до полного растворения мыла.
Добавила к полученному раствору 10 мл серной кислоты и продолжила нагревание до образования на поверхности раствора маслянистого слоя.
Охладила стакан с раствором, а затем слила оставшуюся жидкость; образовавшуюся в стакане жирную кислоту промыла горячей водой и нейтрализовала метилоранжевым.
Перенесла на фильтровальную бумагу жирную кислоту, высушила ее и взвесила.
Масса полученной жирной кислоты равна 3, 92 г.
1.3.1. Взяла навеску жирной кислоты 0, 72 г и растворила ее в этиловом спирте 96 % концентрации.
1.3.2. Добавила в раствор 2 капли фенолфталеина и оттитровала его 0, 1 молярным раствором NaOH до появления бледно-розового цвета.
Средняя молекулярная
масса полученной жирной кислоты равна
317 г/моль.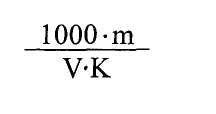
Вывод: следует указать значения всех определенных в ходе выполнения работы показателей жесткости и степень умягчения воды.
Вопросы на защиту:
1) Какие требования предъявляются к воде, используемой на технические нужды и для целей питьевого водоснабжения?
2). Что такое жесткость воды?
3) Каковы источники попадания солей жесткости в воду?
4) Дайте понятия общей, постоянной и временной жесткости.
5) Назовите методы умягчения воды. Какие принципы лежат в основе этих методов?
6) Напишите химические реакции, лежащие в основе известково-солевого метода умягчения воды.
7) Назовите принципы определения общей жесткости, карбонатной жесткости, количества ионов кальция и магния в воде.
7) Что такое металлоиндикатор? Принцип его использования.
