
- •Основные понятия и определения.
- •Механизм образования прочности формовочных и стержневых смесей.
- •Оценка максимальной прочности смесей при растяжении.
- •Предел прочности смеси с учетом сил адгезии и когезии.
- •Проникновение жидкого металла в поры формы.
- •1) Прогрев литейной формы теплом отливки.
- •2) Капиллярное проникновение металла
- •3) Влияние внешнего давления на глубину проникновения металла в поры формы.
- •Окисление поверхности отливок в среде кислорода.
- •Адсорбция кислорода на поверхности твердого металла.
- •Окисление поверхности отливки в газовой атмосфере формы.
- •Зависимость константы равновесия от температуры.
- •Карбидообразование в поверхностном слое отливки.
- •Механизм образования пригара при литье в песчано-глинистых формах.
- •Литейные процессы и особенности перехода метала из жидкого состояния в твердое.
- •Характеристика строения тела отливки, его неоднородности и дефектов.
- •Кристаллическое строение отливки
- •Неоднородность химического состава отливки
- •Воздействие примесей.
- •Неметаллические включения.
- •Усадочная пористость.
- •Усадочная раковина.
- •Усадочные деформации.
- •Трещины.
- •Временные и остаточные напряжения.
- •Технологии производства отливок.
- •Способы извлечения моделей из полуформ.
- •Ручная формовка в опоках.
- •Специальные виды формовки.
- •Ручная формовка.
- •Формовка по неразъемной модели.
- •Формовка с перекидным болваном.
- •Подготовка мягкой постели
- •Подготовка твердой постели.
- •Сушка форм и стержней.
- •Изготовление форм и стержней из химически твердеющей смеси.
- •Машинное изготовление форм.
- •Литье: виды
- •Требования предъявляемые к литейным сплавам.
- •Классификация сплавов.
- •Строение сплавов и понятие о диаграммах состояния.
- •Понятие о диаграммах состояния.
- •Испытание на сжатие и на изгиб.
- •Диаграмма состояния Fe – c.
- •Стали конструкционные нелегированные и легированные.
- •Чугуны серые, ковки и легированные.
- •Литейные сплавы цветных металлов.
- •Алюминиевые сплавы.
- •Магниевые сплавы.
- •Тугоплавкие сплавы.
- •Титановые сплавы.
- •Никелевые и кобальтовые сплавы.
- •Чушковые чугуны.
- •Металлолом.
- •Ваграночное топливо.
- •Расчет шихты.
- •Шихтовые материалы для получения цветных сплавов.
- •Неметаллическая шихта.
- •Методика расчет шихты.
- •Состав огнеупорных материалов для футеровки индукционных печей при кислом процессе.
- •Защитные и огнеупорные покрытия форм и стержней.
- •Формовочные материалы и смеси.
- •Формовочные пески.
- •Свойства формовочных песков, методы их определения, влияние свойств песков на качество формовочных и стержневых смесей.
- •Связующие материалы.
- •Огнеупорная глина
- •Виды формовочных глин по минеральному составу
- •Классификация глин по термической устойчивости
- •Свойства формовочных глин, методы их определения, влияние свойств глин на качество формованных и стержневых материалов.
- •Органические связующие
- •Неорганические связующие материалы.
- •Формовочные и стержневые смеси.
Окисление поверхности отливок в среде кислорода.
Чистота поверхности отливки в значительно мере определяет физико - механические свойства отливок. Литейная корочки, которая часто снимается при механической обработке, обладает повышенной прочностью, хорошей износостойкостью, высокой коррозионной стойкостью. Окислы снижают эти положительные свойства поверхности отливки.
Металл или сплав взаимодействуют с кислородом на границе раздела конденсированных фаз (твердое тело – газ или жидкость - газ). Реакции протекают на поверхности раздела фаз, очень чувствительны даже к незначительным дефектам, будь они химического или кристаллографического происхождения. Чистота металла оказывает основное влияние на протекание поверхностных реакций. Ничтожные количества примесей в металле, сконцентрированные на поверхностном слое (поверхностные активные вещества) могут вызвать селективное окисление. Кроме того, физические свойства окислов, их коэффициент диффузии изменяются даже от следов примесей. А это может в значительной степени изменить ход реакции взаимодействия металла с кислородом.
Адсорбция кислорода на поверхности твердого металла.
Прежде всего, разберемся, что такое адсорбция. Тела с большей поверхностью способны поглощать различные газы и их смеси. Поглощение веществ может происходить не только из газовой смеси, но и из растворов. Явление поглощения газов, паров и поверхностных веществ твердыми телами или жидкостями называют сорбцией. Различают абсорбцию – объемное поглощение жидкостью или твердым телом, химосорбцию – поглощение с образованием химического соединения, адсорбцию – поглощение поверхности твердого тела или поглощение на границе жидкость – жидкость и жидкость – газ (пар) и капиллярную конденсацию – образование жидкой фазы в порах и капиллярах поглотителях. Газ или растворенное вещество называют в этом случае адсорбаитом, а поглощающее вещество – адсорбентом. Количество адсорбированного вещества обычно выражают его содержание в молях в 1 м2 поверхностного слоя. Если величина адсорбирующей поверхности известна, то количество адсорбированного вещества относят к 1 грамму адсорбента.
Литейные процессы часто сопровождаются явлением поглощения поверхностью твердых тел различных веществ из жидкой или газообразной фазы. Например, окисление является сложным гетерогенным процессом, протекающим через ряд стадий диффузионного и кинетического характера:
- подвод кислорода к поверхности металла;
- адсорбция молекул кислорода на поверхности;
- диссоциация молекул кислорода на атомы;
- поглощение атомов кислорода конденсированной фазой (растворение или химическая реакция);
- диффузия продуктов реакции в объеме или поверхностном слое конденсированной фазы (рост окалины).
В зависимости от изменения внешних условий процесс окисления может быть прерван на любой стадии и направлен по необходимому пути.
Адсорбция является обратимым процессом. Согласно Ленглиору, изотерма адсорбции описывается формулой:
Θ=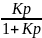
Константа равновесия процесса адсорбции
Кр=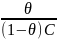 ,
,
где с – коэффициент активности свободных молекул при условии, что активность заполненных и незаполненных центров адсорбции одинакова.
Значения Кр, следовательно ∆Gадс зависят от коэффициента заполненности поверхности θ.
Если между адсорбированными частицами существуют силы взаимного притяжения, то с увеличением θ возрастают Кр и ∣∆Gадс∣ и наоборот, если адсорбирование частицы взаимно отталкиваются, то с увеличением θ уменьшается Кр и ∣∆Gадс∣. Опыт показывает, что с увеличением θ на никеле константа равновесия адсорбции возрастает, а на серебре и платине – уменьшается. При низких температурах возможно существованием физической и химической адсорбции кислорода на поверхности металла.
Количественная адсорбция характеризуется теплотой адсорбции, которая зависит от коэффициента заполненности поверхности θ.
Как правило, с увеличением θ теплота адсорбции уменьшается. В справочниках обычно приводят значения теплоты адсорбции при наиболее низкой степени заполненности поверхности. Значение теплот адсорбции на начальном её этапе всегда больше теплот образования соответствующих окислов. Кроме того, энергетически более выгодна связь металл – кислород адсорбированный, чем связь металл – кислород в окисле.
Таким образом, взаимодействие металла с кислородом начинается с адсорбции кислорода. Атомы металла, находящиеся на поверхности, стремятся соединиться с атомами кислорода и образовать пленку, внутренняя поверхность которой состоит из атомов металла, внешняя – из атомов кислорода.
Атомы кислорода на поверхности металла можно рассматривать как двумерный газ, который может диффузировать как по границам зерен металла, так и по всему объему. По данным Таммона, энергия поверхностной (граничной) диффузии меньше объемной.
∆Gдиф.гр<∆Gдиф.об.
Под действием концентрационных сил атомы кислорода проникают внутрь металла. Изменение температуры в различной мере влияет на изменение коэффициентов поверхности и объемной диффузии.
Из уравнения изобары процесса
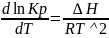
Можно сделать вывод, что при низких температурах преобладает граничная диффузия кислорода, а при высоких – объемная.
При диффузии кислорода по объему металла атомы металла и кислорода перестаиваются так, что бы пространственное распределение этих двух видов атомов было очень близким к тому, которое имеется в окисле. Такая перестройка требует значительной энергии активации. Хемосорбированный кислород и кислород окисла не всегда имеют четкое различие. Хемосорбированный кислород изменяет физические и химические свойства металлов. Например, поверхностная пленка кислорода может вызвать значительный рост коэффициента упрочнения металла при одновременном увеличении хрупкости, увеличении угла смачивания металла окислами (как свойствами, так и окислами других металлов), повышение химической стойкости металла в различных средах.
