
- •Тема 1.1 Теплопровідність ................................................................................................. 6
- •Тема 2.1 Термодинаміка та її метод. Основні параметри стану робочого тіла ........ 15
- •Тема 2.5 Термодинамічні процеси …………………………………………….……….. 23
- •1 Загальна частина
- •1.1 Мета і задачі дисципліни. Структурні модулі
- •1.2 Перелік рекомендованої літератури
- •2 Викладення теоретичного матеріалу
- •Розділ 1 основи теорії теплопередачі
- •Тема 1.1 Теплопровідність
- •Тема 1.2 Конвекційний теплообмін
- •Тема 1.3 Теплообмін випромінюванням
- •Тема 1.4 Теплопередача
- •Розділ 2 технічна термодинаміка
- •Тема 2.1 Термодинаміка та її метод. Основні параметри стану робочого тіла
- •Тема 2.2 Поняття про термодинамічні процеси. Закони ідеального газу.
- •Тема 2.3 Теплоємність. Визначення кількості теплоти
- •Тема 2.4 Перший закон термодинаміки. Ентальпія.
- •Тема 2.5 Термодинамічні процеси
- •Тема 2.7 Реальні гази. Водяна пара
- •Тема 2.8 Вологе повітря
Тема 2.7 Реальні гази. Водяна пара
План
Водяна пара, області застосування.
Водяна пара, основні поняття і визначення.
Процес пароутворення при постійному тиску. - діаграма водяної пари.
Таблиці термодинамічних властивостей води і водяної пари.
5 Визначення термодинамічних параметрів води і водяної пари.
1 Водяна пара як робоче тіло і теплоносій отримала широке застосування в теплотехні-ці. Це пояснюється тим, що вода є дуже поширеною речовиною в природі і, по-друге, вода і водяна пара мають відносно добрі термодинамічні властивості і не впливають шкідливо на метал і живий організм.
Як теплоносій водяна пара широко застосовується в технологічних процесах ба-гатьох галузей народного господарства: енергетики хімічної технології, машинобуду-вання тощо. Наприклад,
в системах опалення і вентиляції житлових і виробничих будинків;
в системах забезпечення мікроклімату приміщень і споруд захищеного грунту, овоче- і фруктосховищ;
в процесах кормоприготування, пастеризації, пропарювання грунту тощо.
Водяна пара застосовується в різних станах у дуже широкому діапазоні тисків і температур і часто переходить в рідкий стан – конденсується. В цих умовах не можна знехтувати силами взаємодії, отже, до водяної пари не можна застосовувати закони ідеальних газів і рівняння Мендєлеєва – Клапейрона.
2 Розділення речовини на газ і пару умовне, бо між ними не існує будь – якої межі.
Парою називається всякий реальний газ, котрий в умовах його застосування здатний переходити в рідину. Всякий реальний газ, який в звичайних умовах його застосуван-ня не переходить в рідкий стан, зберігає назву газу.
Процес переходу рідини в пару називається пароутворенням. Цей процес може проходити шляхом випаровування і кипіння. При випаровуванні утворення пари від-бувається тільки з вільної поверхні рідини. Цей процес протікає при будь – яких тем-пературах рідини і може супроводжуватися зниженням її температури.
Бурхливий
процес пароутворення, який супроводжується
виникненням бульбо-чок пари по всьому
об’єму
рідини, називається кипінням.
Кипіння рідини відбуваєть-ся при
постійному тиску і при відповідній йому
постійній температурі, яка називається
температурою
кипіння або
температурою
насичення і
позначається
![]() .
Для всіх рі-дин температура кипіння
підвищується
з збільшенням тиску, залежність між
ними знаходиться з досліду і в загальному
випадку виражається рівнянням
.
Для всіх рі-дин температура кипіння
підвищується
з збільшенням тиску, залежність між
ними знаходиться з досліду і в загальному
випадку виражається рівнянням
![]() .
Для різ-них рідин і води є велика кількість
емпіричних рівнянь, які дозволяють
приблизно встановити залежність
.
В якості прикладу можна навести рівняння
Руша, яке має вигляд:
.
Для різ-них рідин і води є велика кількість
емпіричних рівнянь, які дозволяють
приблизно встановити залежність
.
В якості прикладу можна навести рівняння
Руша, яке має вигляд:
![]() ,
(2.86)
,
(2.86)
де
Р – абсолютний тиск,
![]() .
.
Для
точного визначення температури кипіння
необхідно користуватися таблицями. Всі
параметри киплячої рідини позначаються
відповідною буквою зі штрихом, наприк-лад:
питомий об’єм
![]() ,
ентальпія
,
ентальпія
![]() ,
ентропія
,
ентропія
![]() тощо.
тощо.
Насиченою парою називається пара, яка знаходиться в динамічній рівновазі зі своєю рідиною. Це означає, що в закритій посудині кількість молекул пари, які над-ходять в простір над киплячою рідиною, дорівнює кількості молекул, котрі поверта-ються знову в рідину. Така рухома рівновага обмовлена хаотичністю руху молекул і силами взаємодії пари і рідиною поблизу її поверхні.
Якщо
при
до киплячої рідини підвести
необхідну
кількість теплоти для випаровування
всієї рідини, то в момент зникнення
останніх крапель рідини (води) отримують
суху
насичену пару при
температурі кипіння
.
Ця пара є нестійким ста-ном й отримується
в парогенераторах як миттєвий стан при
переході в перегріту пару. Стан сухої
насиченої пари визначається одним
параметром: тиском або температурою
насичення
.
Всі параметри сухої насиченої пари
позначаються відповідними буквами з
двома штрихами: питомий об’єм
![]() , ентальпія
, ентальпія
![]() , ентропія
, ентропія
![]() тощо.
тощо.
При кипінні рідини разом із бульбочками пари виносяться дрібні частки вологи. Отримана суміш пари і рідини називається вологою насиченою парою, причому част-ки рідини рівномірно поширені по всьому об’єму пари.
Стан
вологої насиченої пари визначається
тиском
і
степеню сухості
![]() або температурою кипіння
і
степеню сухості
.
Степеню
сухості
називається
масова частка сухої пари, яка міститься
в вологій парі:
або температурою кипіння
і
степеню сухості
.
Степеню
сухості
називається
масова частка сухої пари, яка міститься
в вологій парі:
![]() ,
(2.87)
,
(2.87)
де
![]() і
і
![]() - відповідно маса сухої пари і рідини,
котрі знаходяться в 1 кг суміші;
- відповідно маса сухої пари і рідини,
котрі знаходяться в 1 кг суміші;
![]() - маса
1 кг вологої пари.
- маса
1 кг вологої пари.
Вологість
насиченої пари в парових котлах повинна
бути в межах 1-3 %, тобто її степінь сухості
![]() %.
%.
Для
сухої пари
![]() ,
для киплячої рідини
,
для киплячої рідини
![]() .
Масова частка рідини, котра міс-титься
в вологій парі, називається степеню
вологості і
позначається
.
Масова частка рідини, котра міс-титься
в вологій парі, називається степеню
вологості і
позначається
![]() .
Всі пара-метри вологої пари (крім тиску
і температури) позначаються відповідною
буквою з індексом
,
наприклад: питомий об’єм
.
Всі пара-метри вологої пари (крім тиску
і температури) позначаються відповідною
буквою з індексом
,
наприклад: питомий об’єм
![]() ,
ентальпія
,
ентальпія
![]() ,
ентропія
,
ентропія
![]() тощо.
тощо.
Перегрітою називається пара, яка при однаковому тиску з насиченою, має більш високу температуру, чим температура кипіння . Стан перегрітої пари визначається будь – якими двома параметрами, найбільш часто – тиском і температурою. Процес переходу насиченої пари в рідину називається конденсацією. Цей процес є зворотним процесу пароутворення і також відбувається при і відповідній йому постійній температурі, рівній температурі кипіння при тому ж тиску.
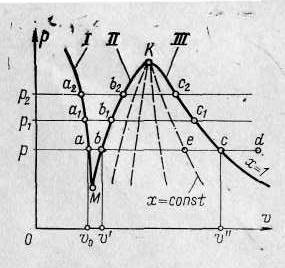
3 На рисунку 2.15 зображена - діаграма водяної пари, на котрій показана залеж-ність зміни питомого об’єму води і пари від тиску.
Отримання
пари в парогенераторах відбувається
при
.
Розглянемо про-цес отримання пари при
деякому постійному тиску
.
Нехай при даному тиску
1
кг води з температурою
![]() займає об’єм
займає об’єм
![]() .
Стан її на діаграмі зображено точкою
.
Стан її на діаграмі зображено точкою
![]() .
При підведенні теплоти вода нагрівається
і її температура підвищується до тих
пір, по-ки вона не досягне температури
кипіння
,
котра відповідає тиску
.
При нагріванні об’єм
води збільшується від
до
.
Стан киплячої рідини позначено на
діаграмі точкою
.
При підведенні теплоти вода нагрівається
і її температура підвищується до тих
пір, по-ки вона не досягне температури
кипіння
,
котра відповідає тиску
.
При нагріванні об’єм
води збільшується від
до
.
Стан киплячої рідини позначено на
діаграмі точкою
![]() .
Відрізок
.
Відрізок
![]() характеризує процес перетворення 1 кг
холодної води в киплячу.
характеризує процес перетворення 1 кг
холодної води в киплячу.
При подальшому підведенні теплоти кипляча вода поступово переходить в пару. В той момент, коли випариться вся рідина, буде отримана суха насичена пара, об’єм її буде в багато разів більше (при низьких тисках) об’єму киплячої води . Стан
 сухої
насиченої пари на діаграмі зображено
сухої
насиченої пари на діаграмі зображено
точкою
![]() .
Процес пароутворення
.
Процес пароутворення
![]() відбува-
відбува-
ється
не тільки при
,
але й при
![]() ,
,
тому цей процес ізобарно - ізотермічний. Якщо
до сухої насиченої пари стану підводити теп-
лоту при тому ж тиску , то вона перетворю-
ється в перегріту пару. Стан її на діаграмі
зображено точкою . Між точками і знахо-
диться суміш сухої на сиченої пари і води,
тобто волога насичена пара, довільний стан її
на
діаграмі зображено точкою
![]() .
.
Рисунок 2.15 - - діаграма водяної
пари
При
більш високому тиску
![]() процес отримання пари відбувається
аналогічно. Але через те що
процес отримання пари відбувається
аналогічно. Але через те що
![]() ,
то питомий об’єм
води
незначно
зменшується і стан її зобра-
,
то питомий об’єм
води
незначно
зменшується і стан її зобра-
жується
точкою
![]() ,
яка розташована лівіше точки
.
Навпаки, питомий об’єм киплячої води
,
яка розташована лівіше точки
.
Навпаки, питомий об’єм киплячої води
![]() буде збільшуватися, бо з підвищенням
тиску підвищується температура кипін-ня
.
Цей стан зображується точкою
буде збільшуватися, бо з підвищенням
тиску підвищується температура кипін-ня
.
Цей стан зображується точкою
![]() ,
розташованою правіше точки
.
При тиску
об’єм
сухої пари
зменшується і зображується точкою
,
розташованою правіше точки
.
При тиску
об’єм
сухої пари
зменшується і зображується точкою
![]() ,
котра буде лівіше точки
.
,
котра буде лівіше точки
.
Якщо
з’єднати
точки
![]() ,
які визначають характерні стани води
і пари при різ-них тисках, то на
- діаграмі отримують три основні лінії:
І, ІІ і ІІІ.
,
які визначають характерні стани води
і пари при різ-них тисках, то на
- діаграмі отримують три основні лінії:
І, ІІ і ІІІ.
Лінія
І визначає стан води при температурі
і різних тисках. З діаграми вид-но, що з
підвищенням тиску питомий об’єм
води
зменшується.
Одначе внаслідок ма-лого стиснення води
залежність
від
незначна і нею звичайно знехтують. Тому
при будь – яких тисках приймають
![]() .
.
Лінія
ІІ визначає стан киплячої рідини (
)
і показує, що об’єм
![]() з підвищен-ням тиску підвищується. Ця
лінія називається нижньою
пограничною кривою,
зліва від неї знаходиться некипляча
рідина, справа – область вологої
насиченої пари.
з підвищен-ням тиску підвищується. Ця
лінія називається нижньою
пограничною кривою,
зліва від неї знаходиться некипляча
рідина, справа – область вологої
насиченої пари.
Лінія ІІІ характеризує стан сухої насиченої пари ( ) при різних тисках і на- зивається верхньою пограничною кривою, зліва від неї знаходиться область вологої пари, а справа – область перегрітої пари. З діаграми видно, що об’єм пари буде тим менше, чим більше його тиск.
З
підвищенням тиску різниця (![]() )
зменшується, лінії ІІ і ІІІ зближуються
і при деякому тиску вони перетинаються
в точці К, яка називається критичною.
Таким чином, точка К визначає критичний
стан води і водяної пари і всі параметри
в цьому стані називаються критичними.
Критичний стан будь – якої речовини
характеризуєть-ся тим, що різниця між
рідиною і парою щезає. Критичні параметри
для води мають наступні значення:
)
зменшується, лінії ІІ і ІІІ зближуються
і при деякому тиску вони перетинаються
в точці К, яка називається критичною.
Таким чином, точка К визначає критичний
стан води і водяної пари і всі параметри
в цьому стані називаються критичними.
Критичний стан будь – якої речовини
характеризуєть-ся тим, що різниця між
рідиною і парою щезає. Критичні параметри
для води мають наступні значення:
![]() ,
,
![]() ,
,
![]() .
.
При
зменшенні тиску лінії І і ІІ зближуються
і при деякому тиску перетинають-ся в
точці М, котра називається потрійною
точкою. Кожна
речовина в цій точці зна-ходиться в
трьох станах: твердому, рідкому і
газоподібному. В потрійній точці кожна
речовина має певні параметри, наприклад
для води:
![]() ,
,
![]() .
.
В області
вологої пари наносяться лінії постійної
сухості
![]() ,
котрі на діаграмі зображені пунктирними
кривими, що виходять з критичної точки
К.
,
котрі на діаграмі зображені пунктирними
кривими, що виходять з критичної точки
К.
4 Всі розрахунки процесів з водою і водяною парою проводяться за допомогою спеці-альних таблиць термодинамічних властивостей води і водяної пари.
В наш час в країнах колишнього СРСР прийняті єдині таблиці (автори С.Л. Рів-
кін або М.П. Вукалович). При складанні цих таблиць були враховані всі найновіші експериментальні і теоретичні дослідження термодинамічних властивостей води і во- дяної пари. В таблицях приведені термодинамічні властивості води і водяної пари в інтервалі тисків до 100 МПа і температур – до 800 . Параметри киплячої рідини і су-хої насиченої пари виділені в окремі таблиці, де ці параметри приведені в залежності або від тисків, або від температур. Користуючись цими таблицями, можна легко знай-ти по заданих температурі або тиску насичення необхідні для розрахунку величини.
Для знаходження цих величин при проміжних значеннях тисків або температур (яких немає в таблицях) користуються методом лінійної інтерполяції. Параметри воло-гої пари при відомій степені сухості розраховуються по наведених раніше рівняннях. При цьому величини, які входять в формули, приймаються по таблицях сухої насиче-ної пари і киплячої рідини.
Таблиці параметрів для некиплячої рідини і перегрітої пари також виділені особливо. Дані для води розташовані вище жирної лінії, а для перегрітої пари – нижче цієї лінії. В області тисків вище критичних, де немає видимої різниці між водою і дуже щільною перегрітою парою, лінія розділу відсутня.
5 При термодинамічних дослідженнях прийнято вважати, що при і будь – якому тиску ентальпія, ентропія і внутрішня енергія рідини дорівнюють нулю, тобто
![]() ,
,
![]() ,
,
![]() .
.
В
ізобарному процесі
(рисунок
19) на підігрівання 1 кг рідини від
до
витрачається
теплота
![]() ,
яку називають теплотою
рідини.
Вона дорівнює:
,
яку називають теплотою
рідини.
Вона дорівнює:
![]() ,
(2.88)
,
(2.88)
де - масова теплоємність рідини.
По І закону ТД теплота рідини витрачається на зміну внутрішньої енергії і на роботу розширення, тому
![]() (2.89)
(2.89)
Оскільки об’єм рідини змінюється незначно, то в цьому процесі переважна частина теплоти рідини витрачається на зміну внутрішньої енергії.
Основні
параметри киплячої рідини (точка
)
![]() ,
,
,
,
![]() знаходять з таблиць по заданому тиску
або по температурі насичення. Внутрішня
енергія киплячої рідини ви-значається
по формулі
знаходять з таблиць по заданому тиску
або по температурі насичення. Внутрішня
енергія киплячої рідини ви-значається
по формулі
![]() ,
(2.90)
,
(2.90)
з рівняння (108) ( )
![]() ,
(2.91)
,
(2.91)
отже, для одного і того ж стану можна написати:
![]() ,
(2.92)
,
(2.92)
звідки
![]() .
(2.93)
.
(2.93)
Таким
чином, теплота киплячої рідини більше
теплоти рідини на величину
![]() .
Цей висновок відноситься до будь –
якого стану води і пари. При низьких
тисках вели-чиною
знехтують та ентальпію в будь – якому
стані води і пари прирівнюють до теплоти.
.
Цей висновок відноситься до будь –
якого стану води і пари. При низьких
тисках вели-чиною
знехтують та ентальпію в будь – якому
стані води і пари прирівнюють до теплоти.
В
ізобарному процесі
![]() (рисунок 2.15) кипляча рідина при постійній
темпера-турі
переходить
в пару.
(рисунок 2.15) кипляча рідина при постійній
темпера-турі
переходить
в пару.
Кількість
теплоти, яка підводиться до 1 кг киплячої
рідини при
для пе-ретворення її в суху насичену
пару, називається теплотою
пароутворення і
познача-ється буквою
![]() .
При будь – яких тисках нижче критичного
більша частина теплоти па-роутворення
витрачається на зміну внутрішньої
потенційної енергії і менша – на ро-боту
розширення. Тоді рівняння І закону ТД
можна виразити в наступному вигляді:
.
При будь – яких тисках нижче критичного
більша частина теплоти па-роутворення
витрачається на зміну внутрішньої
потенційної енергії і менша – на ро-боту
розширення. Тоді рівняння І закону ТД
можна виразити в наступному вигляді:
![]() (2.94)
(2.94)
Ентальпія сухої насиченої пари визначається по формулі
![]() (2.95)
(2.95)
Внутрішня енергія сухої насиченої пари розраховується по відомому рівнянню
![]() (2.96)
(2.96)
Волога
насичена пара є сумішшю киплячої води
і сухої насиченої пари. Її тем-пература
дорівнює температурі кипіння рідини
при
даному тиску. Питомий об’єм вологої
пари дорівнює сумі питомих об’ємів
кг
сухої пари і (![]() )
кг води
)
кг води
![]() (2.97)
(2.97)
Звідси можна отримати рівняння
![]() ,
(2.98)
,
(2.98)
яке застосовують для точного визначення . Ентальпія та ентропія вологої пари визна-чаються за аналогією з рівнянням (116), а саме
![]() ,
(2.99)
,
(2.99)
![]() (2.100)
(2.100)
Внутрішня енергія вологої пари знаходиться з рівняння
![]() (2.101)
(2.101)
Властивості
перегрітої пари сильно відрізняються
від властивостей насиченої. При даному
тиску перегріта пара може мати будь –
яку температуру вище температури
насичення
,
а її об’єм
![]() при одному ж і тому тиску завжди буде
більше об’єму
сухої насиченої пари
.
при одному ж і тому тиску завжди буде
більше об’єму
сухої насиченої пари
.
Чим вище температура перегрітої пари і чим нижче її тиск, тем менше відхиля-ється перегріта пара від властивостей ідеального газу. При високих тисках і темпера-турах, близьких до стану насичення, перегріта пара буде значно відхиляться від Влас-тивостей ідеального газу. Одначе у всіх випадках перегріта пара не підпорядковується рівнянню . Для перегрітої пари різними дослідниками були запропоновані емпіричні рівняння стану, які дозволяють знаходити значення її основних параметрів та інші фізичні величини.
Внутрішня енергія перегрітої пари в даному стані визначається по відомому рівнянню
![]() (2.102)
(2.102)
В
ізобарному процесі
![]() (рисунок 2.15) відбувається перегрівання
пари, при цьому температура пари
становиться більше температури кипіння
.
(рисунок 2.15) відбувається перегрівання
пари, при цьому температура пари
становиться більше температури кипіння
.
Кількість
теплоти, яка підводиться до 1 кг сухої
насиченої пари при перетворен-ні її в
перегріту, називається теплотою
перегрівання і
позначається
![]() .
Ця теплота підраховується по рівнянню
.
Ця теплота підраховується по рівнянню
![]() ,
(2.103)
,
(2.103)
де
![]() і
і
![]() - відповідно ентальпія і температура
перегрітої пари;
- відповідно ентальпія і температура
перегрітої пари;
![]() - середня
- середня
масова ізобарна теплоємність перегрітої пари.
Лекція 11
