
- •Тема 1 Теорія хімічної будови органічних речовин о.М.Бутлерова.
- •Тема 2 Вуглеводні.
- •I. Ізомерія та номенклатура
- •Iiі .Методи добування
- •IV. Розрахункові задачі
- •V. Генетичний зв’язок між класами сполук
- •I. Ізомерія та номенклатура.
- •II. Хімічні властивості
- •III. Методи добування
- •IV. Розрахункові задачі
- •V. Генетичний зв’язок.
- •II. Хімічні властивості
- •IV. Розрахункові задачі
- •V. Генетичний зв'язок
I. Ізомерія та номенклатура
1. Назвіть наступні сполуки за міжнародною номенклатурою
а) СНз-СН-СН-СН2-СН-СНз в) СН3- СН2 - С(СН3)2 – С2Н5
׀ ׀ ׀ СН3
СНз СНз C2Н5 ׀
б) (СН3-СН2 )2 С(СН3)2 г) С3Н7- СН2 – СН –СН3
2. Напишіть структурні формули речовин:
а) 2-метил- 1,1 -дихлоропропан; б) 2,3,4,5-тетраметилгептан;
в) З-етил -2,2-диметилгексан; г) 2,2,3-триметилбутан.
3. Які алкани не мають ізомерів ?
ІІ. Хімічні властивості
1. Покажіть по стадіям механізм фотохімічного хлорування н- гексану з утворенням 2-хлоргексану.
2. Напишіть рівняння реакцій:
а) нітрування бутану;
б) дегідрогенциклізації гексану;
в) ізомеризації н-пентану;
г) горіння ізобутану;
д) термічного крекінгу октану;
Iiі .Методи добування
1. Яким чином алкани одержують з ненасичених вуглеводнів? Назвіть ці процеси. Наведіть приклади.
2. Які галогенопохідні необхідно використати для синтезу:
а) н- гексану; б) 3,3,4,4-тетраметилгексану.
IV. Розрахункові задачі
1. Визначте молекулярну формулу алкану, якщо відомо, що при повному спалюванні 0,1 моль його утворилось 13,44 л Карбон (IV) оксиду .
2. Скільки літрів кисню потрібно (н.у.) для повного згорання 28 л метану? Розрахуйте масу кислої солі, що утвориться внаслідок пропускання вуглекислого газу, який при цьому виділяється, через розчин гашеного вапна.
V. Генетичний зв’язок між класами сполук
Al4C3 → CH4 → CH3Cl → CH2Cl2 → CHCl3 → CCl4
Будова та фізичні властивості алкенів.
Основні терміни та поняття:
Будова алкенів:
один подвійний зв'язок, що є поєднанням одного σ- та одного π– зв’язку,
атом Карбону знаходиться в стані sp2 – гібридизації,
валентний кут 120⁰,
просторова будова: площинна;
довжини зв’язків : С – С 0,134 нм
№ 17
Виберіть формулу, що правильно відображає взаємне розташування в просторі атомів в молекулі етилену:
![]()
![]()
![]()
![]()
![]()
Вкажіть сполуки, в молекулах яких містяться одинарні та подвійні зв’язки:
А. алкани; Б. алкіни; В. циклоалкани; Г. алкени.
Подвійний зв’язок є поєднанням . . .
А. двох σ- зв’язків; Б. двох π- зв’язків; В. одного σ- зв’язку та одного π- зв’язку; Г. йонного зв’язку та ковалентного зв’язку.
Вкажіть невірне твердження про етилен:
А. валентні кути в молекулі етилену по 1200;
Б. всі атоми, що утворюють молекулу лежать в одній площині;
В. енергія розриву С-С - зв’язку в молекулі етилену рівна 348 кДж/моль. Енергія розриву подвійного зв’язку в молекулі етилену рівна 3482=696 кДж/моль;
Г. орбіталі, що утворюють - зв’язок негібридні і не лежать в площині молекули.
1 2 3 4
Вкажіть гібридизації атомів Карбону в молекулі алкену: СН2=СН – СН2 –СН3
А.1 та 4 – sp2, 2 та 3 – sp3 ; Б. 3 та 4 – sp3, 1 та 2 – sp2 ; В. 1 та 4 – sp3, 2 та 3 – sp ; Г. 1 та 4 – не гібридизовані, 2 та 3 – sp2.
Алкени(етиленові вуглеводні, олефіни). Гомологічний ряд. Номенклатура. Ізомерія.
Основні терміни та поняття:
Аліл – ненасичений радикал СН2=СН- СН2 –
Вініл – найпростіший ненасичений одновалентний радикал СН2 = СН –
№ 18
Виберіть формулу радикалу вінілу:
А. СН2=СН-СН2- Б. –С3Н6
В.![]() Г.
СН2=СН
–
Г.
СН2=СН
–
Виберіть формула речовини, що має таке ж значення масової частки Карбону, що і в етилені:
А.
С6Н6
Б.
![]()
В. С2Н2 Г. СН2=СН-СН=СН2
Вкажіть структурну формулу 2,3-диметилбут-1-ену:
А. СН2 = СН – С(СН3)3; Б. СН3 – СН= С(СН3) – СН2 – СН3;
В. СН3 –СН – С=СН2; Г. СН2 = С – СН(СН3) – СН2 – СН3
| | |
СН3 СН3 СН3
Виберіть формулу речовини, що має геометричні ізомери:
А. СН3СН=С(СН3)(C2Н5); Б. пент -1-ен;
В. СН3СН=С(СН3)2; Г. СН2=С(С2Н5)СН3.
Назвіть наступні алкени за міжнародною номенклатурою:
А. H C2H5 Б. CH2 = C - CH - CH - CH3
\ / | | |
C = C CH3 CH3 CH3
/ \
C3H7 H
В. CH3 – CH2 – C – CH – CH – CH3 Г. CH3
|| | | \
CH2 CH3 C3H7 CH – CH – C – CH2 – CH2 – CH3
/ | ||
CH3 CH3 CH2
Д.
![]() Е.
Е.
![]()
Напишіть структурні формули наступних алкенів:
А. транс-3,4-диетилгепт-3-ен; Б. 2,3-дибромогекс-1-ен;
В. 2,3-диметилбут-1-ен; Г. 2,3,4,4-тетраметилпент-2-ен;
Д. 2-етил-окт-1-ен; Е. (цис)- 3-йодо – 4 – метилгепт-3-ен.
Вкажіть, які з речовин ізомерні між собою.
Напишіть структурні формули всіх речовин з молекулярною формулою C4H8 та назвіть їх.
Напишіть формули геометричних ізомерів наступних сполук:
А. С2Н5 – СН=СНСН2СН3; Б. BrСН=СН(СН2)3СН3.
Хімічні властивості алкенів. Добування.
Основні терміни та поняття:
Гетеролітичний розрив - розрив ковалентного зв’язку, внаслідок якого утворюються йони.
Гідрування (гідрогенізація) – реакція приєднання водню до молекули органічної сполуки.
Дегідрування – реакція відщеплення водню.
Гідратація - реакція приєднання води до молекули ненасиченої речовини.
Дегідратація – реакція відщеплення води від речовини.
Дегалогенування – реакція відщеплення галогенів.
Дегідрогалогенування - реакція відщеплення галогеноводнів.
Полімеризація – це хімічна реакція сполучення однакових молекул мономеру, що призводить до утворення макромолекул з великою молекулярною масою.
Правило Зайцева – при відщепленні галогеноводнів від галогеналканів чи води від спирту атом Гідрогену відщеплюється від менш гідрогенізованого атома Карбону.
Правило Марковникова – при приєднанні полярного реагенту (ННаl, НОН) до несиметричного алкену атом Гідрогену приєднується до найбільш гідрогенізованого атома Карбону, що зв’язаний подвійним зв’взком.
Реакція Є.Є. Вагнера –окислення алкенів КМnО4 в нейтральному або слабо лужному середовищі до двохатомних спиртів (гліколей).
 І
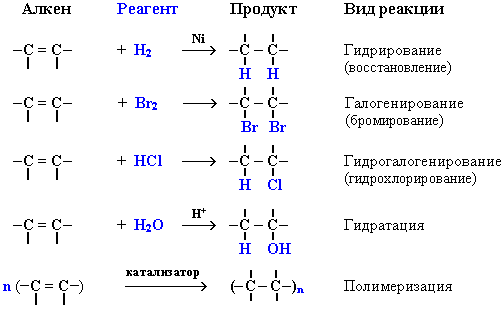
Приєднання
І
Приєднання
Гідрування (відновлення)
Галогенування (бромування)
Гідрогалогенування (гідрохлорування)
Гідратація
Полімеризація

![]()
ІІ
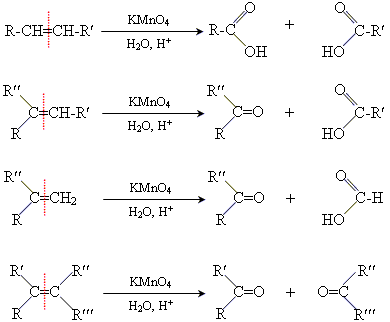
Окислення
№ 19
Вкажіть формулу речовини, з якою не ваємодіють етиленові вуглеводні:
А. водень; Б. кисень; В. азот; Г. хлор.
Вкажіть реагент, що використовують для ідентифікації алкенів:
А. Br2 (H2O); Б. H2O (H+); В. HBr; Г.Cl2.
Вкажіть, які твердження вірні:
Як насичені , так і ненасичені вуглеволні реагують з бромною водою.
2. Як насичені , так і ненасичені вуглеволні реагують з киснем.
А. вірно тільки 1; Б. вірно тільки 2;
В. обидва твердження вірні; Г. обидва твердження невірні.
Вкажіть продукт взаємодії бут-1-ену з хлором:
А. 1,2-дихлоробутен; Б. 1,1-дихлоробутан;
В. 2-хлоробут-1-ен; Г. 1,2-дихлоробутан.
Вкажіть продукт, що переважно утворюється при взаємодії 2-метилбут-1-ену з водою:
А. 2 –метилбутан-1-ол; Б. 2 –метилбутан-2-ол;
В. 2 –метилбутанон; Г. пентан-2-ол.
Вкажіть продукт приєднання НСl до 2-метилпропену у відповідності до правила Марковникова:
А. 2-хлоро-2-метилпропан; Б. 1-хлоро-2-метилпропан;
В. 2-хлоро-2-метилпропен; Г. 1-хлоро-2-метилпропен.
Вкажіть умову, що сприяє збільшення виходу етилену реакцією гідрування етину:
С2Н2
+ Н2
![]() СН2=СН2
+ Q.
СН2=СН2
+ Q.
А. використання більш активного каталізатора;
Б. підвищення температури;
В. «отруєння» каталізатора – платини;
Г. підвищення тиску.
Вкажіть продукт реакції Вагнера Є.Є. алкену
 :
:
А.![]() Б.
Б.
![]()
В.
![]() Г.
СО2
и Н2О
.
Г.
СО2
и Н2О
.
Вкажіть реагент, що необхідний для проведення наступної реакції:
![]()
А. HBr; Б. CH3COOH; В. H2SO4; Г. HCl.
Вкажіть речовину Х в ланцюжку перетворень:
![]()
А. пропан; Б. пропен;
В. 1-хлоропропан; Г. циклопропан.
Вкажіть продукт,який переважно утворюється при дегідратації спирту (СН3)3С-ОН:
А.
![]() Б.
Б.
![]()
В.
![]() Г.
Г.
![]()
Домашнє залікове завдання № 3
“Розв’язування розрахункових задач на виведення формули речовини
за рівнянням хімічної реакції ”
Яка маса брому може прореагувати з 7 г етиленового вуглеводню, густина якого за киснем 1,75.
На повне гідрування 0,7 г етиленового вуглеводню витрачено 0,224 л водню (н.у.). Обчисліть молярну масу та напишіть структурну формулу цієї сполуки, що має нормальну будову.
Етиленовий вуглеводень, маса якого 7 г, реагує з 20 г брому. При окисленні його водним розчином КМnО4, утворюється симетричний двохатомний спирт. Знайдіть формулу вуглеводню.
Встановіть формулу гомологу етилену, 0,42 г якого повністю знебарвлює 16 г 10%-го розчину брому в хлороформі.
Встановіть формулу алкену, якщо відомо, що він має цис- транс ізомери, а 5,6 г його при приєднанні води утворює 7,4 г спирту.
Скільки літрів (н.у.) пропену вступає в реакцію з хлороводнем, якщо при цьому утворюється 1,6 г суміші, в якій масова частка 2- хлоропропану – 90%, а 1- хлоропропану – 10%.
Домашнє залікове завдання № 4 «Алкени»
