
- •Тема 1 Теорія хімічної будови органічних речовин о.М.Бутлерова.
- •Тема 2 Вуглеводні.
- •I. Ізомерія та номенклатура
- •Iiі .Методи добування
- •IV. Розрахункові задачі
- •V. Генетичний зв’язок між класами сполук
- •I. Ізомерія та номенклатура.
- •II. Хімічні властивості
- •III. Методи добування
- •IV. Розрахункові задачі
- •V. Генетичний зв’язок.
- •II. Хімічні властивості
- •IV. Розрахункові задачі
- •V. Генетичний зв'язок
Тема 2 Вуглеводні.
Алкани. Гомологічний ряд. Номенклатура. Ізомерія.
Основні терміни та поняття:
«Парафіни» означає «мала хімічна спорідненість», або, інакше, «низька реакційна здатність».
Гомологи - речовини з однаковим якісним складом, подібні за будовою і хімічними властивостям, а за кількісним складом вони відрізняються один від одного на групу -СН2- - гомологічну різницю. Конформери (просторові поворотні ізомери)це геометричні форми молекули, що перетворюються одна водну за рахунок обертання фрагментів молекули навколо σ – зв’язків без зміни валентних кутів та довжин зв’язку.
Конформація – явище, що обумовлене вільним обертання груп атомів навколо σ – зв’язків, як навколо осей, внаслідок чого групи атомів в молекулі приймають різне просторове положення.
Номенклатура – частина мови науки, що є системою правил, які дозволяють дати кожній сполуці однозначну назву.
Цифри положення замісників |
|
Префікс число замісників |
|
Назва замісників ( за алфавітом) |
|
Корінь – довжина основного ланцюга |
Суфікс – -ан -ен -ін |
Суфікс старшої функціональної групи |
2,3 - ди метил(-СН3) – бут ан ова кислота
1 2 3 4 три етил (-С2Н5)
СН3 – СН – СН – СН3 тетра пропіл(-С3Н7)
| | ізопропіл (-СН(СН3)2)
СН3 СН3
№ 10
Виберіть суфікс, притаманний назвам гомологів метану:
А. -он; Б. -eн; В. -ан; Г. -ин.
Виберіть ознаку, притаманну членам одного гомологічного ряду: А. однаковий якісний склад; Б. однаковий кількісний склад;
В. однакова молекулярна маса; Г . однакова густина за повітрям.
Вкажіть речовину, що не входить до гомологічного ряду алканів:
А.
С6Н12
Б. С40Н82
В.
![]() Г.
Г.
![]()
Виберіть назву речовини CHBr2–CHBr–CHBr–CHBr2:
А. 1,1,2,3,4,4-гексабромбутан; Б. 1,2,3,4-гексабромбутан;
В. 1,2,3,4-гексабромбутан; Г. 1,2,3,4-бромпропан.
Вкажіть, які сполуки є Ізомерами:
А. 3-метилпентан та 3-етилпентан;
Б. 3-метилгексан та 2,3-диметилпентан;
В. 2,2,3-триметилбутан та 3-метил-3-етилпентан;
Г. 2-метил-3-етилгексан та 2,3 -диметилгексан;
Вкажіть назву вуглеводневих радикалів:
1) –СН2 – СН – СН3 2) – СН2 – СН2 – СН3 3) – С(СН3)3
|
СН3
А. 1 - втор-бутил; 2 - ізопропіл; 3 - трет-бутил.
Б. 1 - ізобутил; 2 - н-пропіл; 3 - трет-бутил.
В. 1 - трет-бутил; 2 - н-бутил; 3 - втор-бутил
Виберіть формулу молекули, що містить в своєму складі найбільше число третинних атомів Карбону:
А.![]() Б.
Б.
![]() В.
В.
 Г.
Г.
![]()
Вкажіть число ізомерних дибромопохідних пропану:
А. три; Б. чотири; В. п’ять; Г. шість.
Вкажіть формулу алкану, якщо його відносна молекулярна маса дорівнює 86:
А. гексан; Б. пентан; В. бутан; Г. етан.
Визначте молекулярну формулу алкану, масова частка Карбону в якому становить 81,82 %:
А. С2Н6; Б. С7Н16; В. С3Н8; Г. С4Н10.
№ 11 Назвіть речовини. Знайдіть гомологи і ізомери.
А Б.
В.
Б.
В.![]() Г.
Г.
Д. Е.
Е. Ж.
Ж.
№ 12 За назвами речовин написати їхні скорочені структурні формули.
А. 2,2-диметилбутану; Б. 2,2,3-трибромлпентану; В. 2-хлорбутану; Г. 2,2,3,3-тетраметилгексану.
Будова та фізичні властивості алканів.
Основні терміни та поняття:
Хімічний зв’язок, що утворюється за рахунок спільних електронних пар, шляхом узагальнення пари електронів двома атомами, називається ковалентним зв’язком.
Енергія зв’язку кДж/моль –це енергія, що виділяється при утворенні молекул із одиноких атомів.
Довжина хімічного зв’язку d, Ǻ = відстань між центрами ядер атомів в молекулі, йоні або кристалі, коли енергія системи, що утворилась min.
Під насиченістю розуміють здатність атомів брати участь в утворенні обмеженої кількості ковалентних зв’язків.
Напрямленість ковалентного зв’язку визначається взаємним розташуванням електронних орбіта лей, що беруть участь при утворенні зв’язку.
σ-зв’язок – зв’язок, що виникає при перекриванні АО вздовж лінії, що з’єднує ядра атомів, називається.
Гібридизація – процес змішування різних, але близьких за енергією орбіта лей даного атома, з виникненням такої ж кількості нових гібридних орбіта лей, однакових за енергією та формою. Гібридизація відбувається при утворенні ковалентного зв’язку та вигідна в енергетичному плані.
Будова алканів:
прості (одинарні σ – зв’язки,
атом Карбону знаходиться в стані sp3 – гібридизації,
валентний кут 109⁰28΄,
просторова будова: метан – тетраедрична, вищі алкани зигзагоподібна,
довжини зв’язків : С – С 0,154 нм, С – Н 0,109 нм.
№ 13
Вкажіть форму молекули метану:
А. тетраедрична; Б. плоска;
В. лінійна; Г. інша.
Вкажіть характер хімічного зв’язку між атомом Карбону та чотирма атомами Гідрогену :
А. подвійні; Б. потрійні;
В. одинарні; Г. донорно - акцепторні.
Вкажіть кількість ковалентних зв’язків між атомами Карбону в молекулі етану:
А. 2; Б. 3; В. 1; Г. 8.
Виберіть, перекривання яких орбіталей утворюється C – C зв’язок в молекулі етану:
А. s – sp3; Б. s – p ; В. sp3 – sp3; Г. p – sp3.
Вкажіть довжину Карбон – Карбонового зв’язку в молекулі пропану:
А. 0,154 нм; Б. 0, 140 нм; В. 0,134 нм; Г. 0, 120 нм.
Вкажіть помилкову характеристику будови молекул та загальних властивостей алканів:
А. в утворенні хімічних зв’язків у кожного атома Карбону беруть участь чотири sp3-гібридні орбіталі, кут між якими 1090 28’, карбоновий ланцюг не лінійний, а набуває іншу форму;
Б. С-С зв’язок в молекулах алканів –це - зв’язок , що здатний обертатися відносно лінії, що сполучає центри атомів Карбону, тому для алканів не характерна геометрична ізомерія;
В. С-Н зв’язок в молекулах алканів міцний, енергія С-Н зв’язку складає 412 кДж/моль, це в значному ступені визначає достатню інертність алканів;
Г. валентна орбіталь атома Карбону – це результат гібридизації 1s і 2p орбіталей атома Карбону.
Виберіть найбільш імовірний механізм розриву ковалентного зв’язку в молекулах алканів:
А. СН3-СН2:СН2-СН3 ; Б. (СH3)2HCH;
В. CH3-CH2-H2C:H ; Г. CH3-H2C:H.
Вкажіть невірну характеристику алканів:
А. характерно малоактивні;
Б. легко змішуються (рідкі та тверді) з водою та іншими полярними розчинниками;
В . рідкі алкани добрі розчинники для жирів та жирних масел;
Г. це вуглеводні з малополярними молекулами.
Вкажіть алкан, що найлегше переходить у рідкий стан:
А. пропан; Б. бутан ; В. етан; Г. метан.
Виберіть алкан із найнижчою температурою :
А. н- пентан; Б. н- бутан;
В. ізопентан; Г. неопентан.
№ 14
Аби видалити з тканини чи паперу парафінову пляму, треба пропрасувати її через кілька шарів пористого паперу, наприклад паперові серветки, гарячою праскою. Поясніть, на якій властивості парафіну ґрунтується цей спосіб вибавляння плями.
Хімічні властивості алканів. Добування.
Основні терміни та поняття:
Термін «парафіни» означає «мала хімічна спорідненість», або, інакше, «низька реакційна здатність».
Розривання ковалентного зв’язку, внаслідок якого утворюються частинки з неспареними електронами, називають гомолітичним.
Радикал - частинка (атом, група сполучених атомів, молекула), яка має неспарений електрон.
Реакцію, яка відбувається з утворенням активної частинки, здатної спричинити утворення інших таких частинок, називають ланцюговою.
Реакція Коновалова- реакція взаємодії з розведеною нітратною кислотою при нагріванні під тиском з утворенням нітропохідних алканів( заміщення атома Гідрогену на нітрогрупу – NO2).
Реакція дегідрування (дегідрогенізації) – каталітичне відщеплення водню від молекули органічних сполук.
Піроліз - розщеплення сполук під впливом нагрівання. У разі піролізу алканів під час переробки нафти вживають термін крекінг.
Синтез Фішера - Тропша:
![]()
Реакція Вюрца –взаємодія галогенопохідних алканів з металевим Na:
R –Cl + R΄ - Cl + 2 Na → R – R ΄ + R – R + R΄ - R΄ + 2 NaCl
Реакція ізомеризації – перетворення алкану в його ізомер з розгалуженою будовою(відбувається при нагріванні і в присутності каталізатора АlCl3)
Синтез – газ – суміш Карбон (ІІ) оксиду та водню, що одержують при конверсії метану з водяною парою або вуглекислим газом.
Алкани насичені вуглеводні загальною формулою СnH2n +2 , атоми Карбону яких зв’язані між собою простими ковалентними зв’язками,а інші валентності насичені атомами Гідрогену.
Будова |
Прогнозовані властивості |
атом С утворює прості (одинарні ) σ – зв’язки міцні насичений атом С max число зв’язків - 4 σ зв’язки слабополярні - гомолітичний розрив з утворенням радикалів |
хімічно неактивні (парафіни) – не взаємодіють з сильними Ох не здатні до приєднання. Характерна реакція заміщення механізм реакції - вільнорадикальний |
Хімічні властивості
nCO2 +
(n+1) H2O

 горіння
горіння
СnH2n+1Hal
+
HCl
 галогенування
галогенування
третинний > вторинний > первинний атом С
CnH2n+1NO2
+H2O

нітрування
CnH2n+1SO3H
+H2O
сульфування
СmH2m+2
+ CkH2k
крекінг алкан алкен
2СН4 = С2Н2 + 3Н2
-Н2 СnH2n C=C алкен
дегідрування СnH2n-2 С≡С алкін
СnH2n-6
![]() арени
арени
СnH2n+2
розгал. ланцюг
ізомеризація
[O]
часткове спирт 2CH4 + O2 -t, кат 2СН3ОН
окислення альдегід CH4 + [O] -t, кат НСНО
карбонова кислота CH4 + [O] -t, кат НСООН
2С4Н10 + 5O2 -t, кат 2СН3СООН + 2Н2О
№ 15
Метану характерні реакції:
А. обміну; Б. заміщення;
В. взаємодії з лугами; Г. нейтралізації.
При пропусканні газоподібних насичених вуглеводнів через бромну
воду та розчин перманганату калію рідина:
А. утворює осад; Б. змінює колір на синій;
В. знебарвлюється; Г. не змінює колір .
Хлорування метану відбувається:
А. за умови нагрівання;
Б. за умови освітлення ультрафіолетовим промінням;
В. на розсіяному сонячному світлі;
Г. у темряві.
Вкажіть реакцію, з якої починається процес хлорування :
А. СН3Сl + СlСН2Сl2 + НСl Б. СН4СН3 + Н
В. Сl2 2 Сl Г. СН4 + Сl СН3 + НСl
Виберіть практично нездійснену реакцію:
А.
СН4+
Сl2
![]() CН3Сl
+HCl
CН3Сl
+HCl
Б.
CH4
+ HNO3
![]() CH3NO2
+H2O
CH3NO2
+H2O
В.
CH4
+ 2H2O![]() CO2+4H2
CO2+4H2
Г.
CH4+I2![]() CH3I
+ HI
CH3I
+ HI
Вкажіть пару частинок, що найбільш вірогідніше утворяться при крекінгу н- бутану :
А. СН3 і СН2-СН2-СН3; Б. СН3-СН2 і СН3-СН2 ;
В. :СН3 і СН2-СН2-СН3; Г. СН3-СН2-СН2-СН2 і Н.
Вкажіть найбільш імовірний продукт реакції
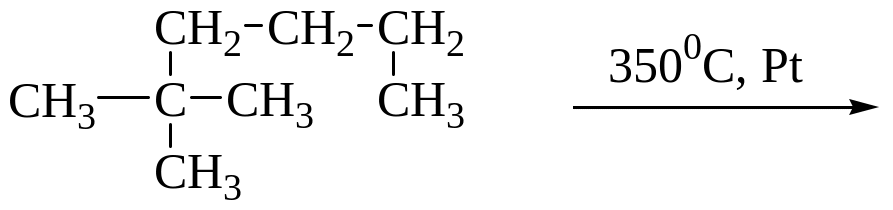 :
:
А. суміш ізомерів за положення подвійного зв’язку;
Б. алкани – ізомери за Карбоновим ланцюгом;
В. карбоциклічні вуглеводні – арени;
Г. алкани та алкени з більш короткими Карбоновими ланцюгами, ніж вихідна речовина;
Виберіть умови, що сприяють підвищенню виходу метану в реакції
Ni
 С(тв.)
+ 2Н2(г)
СН4(г)
+ 75кДж
С(тв.)
+ 2Н2(г)
СН4(г)
+ 75кДж
А. підвищення температури до 600 0С;
Б. підвищення тиску до 100 атм;
В. пониження тиску до 50 мм рт. ст. ;
Г. збільшення шару каталізатора.
Укажіть реакцію В’юрца:
А. С2Н5Cl + Cl2 →; Б. С2Н5Cl + Na→;
В. С2Н4Сl2 + Cl2→; Г. С2Н5Cl + О2→.
Вкажіть реакцію , в результаті якої не може утворитися метан:
А.
СН3COONa(тв.) +
NaOH(тв.)
![]()
Б. СаС2(тв.) + Н2О(ж)
В. С(тв) + Н2(г)
Г.
СО(г) + Н2(г)
![]()
![]()
№ 16
Горіння пропан – бутанової суміші можна продемонструвати на прикладі газової запальнички. Чому колір полум’я жовтий ?
Домашнє залікове завдання №1
“Розв’язування розрахункових задач на виведення формули речовини за масою, об’ємом та кількістю речовини – продуктів згоряння ”
Внаслідок спалювання вуглеводню кількістю речовини 0,5 моль утворилися Карбон (ІV) оксид і вода кількістю речовини по 1,5 моль. Відносна густина пари цієї речовини становить 21. Виведіть молекулярну формулу речовини.
Встановіть формулу речовини, якщо відомий її склад : С – 38,75%, Н – 9,68%, О – 51,51% (за масою). Відносна густина цієї сполуки за воднем становить 31.
Внаслідок спалювання органічної речовини масою 0,7 г утворилися Карбон (ІV) оксид і вода кількістю речовини по 0,05 моль кожна. Ця речовини масою 0,1 г займає об’єм 32 мл (н.у.). Виведіть формулу речовини.
Виведіть формулу речовини , якщо внаслідок спалювання її масою 1,5 г утворився Карбон (ІV) оксид масою 4,4 г і вода масою 2,7 г . Густина речовини за н.у. становить 1,34 г/л.
Відносна густина газоподібного галогенопохідного алкану за воднем становить 32,35. Виведіть формулу речовини, якщо при спалюванні її масою 6,45 г утворився вуглекислий газ об’ємом 4,48 л і хлороводень об’ємом 2,24 л ( н.у.) та вода.
Внаслідок спалювання органічної сполуки кількістю речовини 0,03 моль утворилися Карбон (ІV) оксид кількістю речовини 0,18 моль і вода кількістю речовини 0,15 моль. Відносна густина пари сполуки з воднем становить 41. Встановіть молекулярну формулу сполуки.
Виведіть формулу вуглеводню, що містить Карбон масовою часткою 93,75%, якщо відносна густина цієї сполуки за повітрям становить 4,41.
Внаслідок спалювання органічної сполуки масою 2,76 г утворилися Карбон (ІV) оксид масою 9,24 г і вода масою 2,16 г. Відносна густина цієї сполуки за воднем становить 46. Виведіть молекулярну формулу сполуки.
Виведіть молекулярну формулу речовини, масова частка Карбону в якій 64,8 %, Гідрогену – 13,5 %, Оксигену – 21,6 %. Відносна густина пари цієї речовини за повітрям становить 2,55.
Виведіть формулу насиченого вуглеводню , якщо відносна густина його за повітрям становить 4,414.
На спалювання 200 мл невідомої органічної речовини витратили 900 мл кисню. Утворилось 600 мл СО2 та 600 мл Н2О. Виміри об’ємів проводились за однакових умов. Визначте формулу речовини.
Який об’єм повітря потрібно використати для спалювання 30 мл пропану.
Домашнє залікове завдання № 2 «Алкани»
