
- •Лабораторная работа Определение спиртовой группы методом окисления.
- •Лабораторная работа Исследование оксигруппы (фенолов) бромид-броматным методом.
- •Лабораторная работа Определение альдегидной группы йодометрическим методом
- •Лабораторная работа Определение примесей в сульфокислотах титрометрическим методом с хлоридом бария
- •Лабораторная работа Определение нафтолов йодометрическим методом
- •Лабораторная работа Определение анилина методом диазотирования
- •Лабораторная работа Определение кислотного числа
- •Лабораторная работа Определение йодного числа
- •Лабораторная работа Определение числа омыления и эфирного числа
Лабораторная работа Определение числа омыления и эфирного числа
Цель работы.
Определение количества сложных эфиров в анализируемом масле, использовав число омыления как химический показатель.
Пояснения к работе.
Количественное определение сложных эфиров основано на реакции гидролитического расщепления (омыления).
В результате омыления образуется спирт и соль кислоты
O O
║ ║
R─ C─ C─R1 + KOH → R C OK + R1OH
По количеству щелочи, израсходованному на омыление, рассчитывают количество сложного эфира.
Число омыления (ч.о.) соответствует количеству миллиграммов едкого калия, необходимого для нейтрализации свободных кислот и омыления эфиров, содержащихся в 1 г анализируемого вещества.
Реакция омыления протекает в присутствии щелочи. Скорость омыления зависит от концентрации ионов OH- в растворе и от температуры. Наиболее часто омыление проводят при температуре кипящей водяной бани. Кроме того, скорость омыления эфиров зависит от природы эфира. В одних случаях реакция омыления протекает быстро, даже при обычной температуре, в других продолжается несколько часов. Сложные эфиры, растворимые в воде, сравнительно легко омыляются доже водным раствором щелочи, плохо растворимые эфиры – в спиртовой среде. Для омыления пользуются преимущественно спиртовым раствором KOH. Спиртовые растворы щелочей при хранении меняют свой титр, поэтому поправочный коэффициент для них определяют в каждом отдельном случае при помощи контрольного титрования.
Оборудование и реактивы.
Аналитические весы.
Обратный холодильник.
Электрическая плитка.
Водяная баня.
Бюретка.
Пипетки, 1-25 см3.
Гидроокись калия, 0,5 н. спиртовой раствор.
Соляная кислота, 0,5 н. раствор.
Фенолфталеин.
Работа в лаборатории.
Навеску вещества около 1-2 г, взятую с точностью до 0,0002 г, помещают в колбу емкостью 200-250 см3, добавляют 25 см3 0,5 н. раствора гидроксида калия. К колбе присоединяют обратный холодильник и погружают в водяную баню. Баню нагревают до кипения и выдерживают пробу в течение 1-1,5 ч, поддерживая легкое кипение смеси. Конец омыления определяют по образованию совершенно прозрачного и однородного раствора (отсутствие маслянистых капель). После прекращения нагревания к пробе прибавляют 1 см3 раствора фенолфталеина и титруют 0,5 н. раствором соляной кислоты до обесцвечивания.
Параллельно в тех же условиях нагревают 25 см3 0,5 н. спиртового раствора гидроксида калия и титруют 0,5 н. раствором соляной кислоты (холостая проба). Разность между количеством кислоты, израсходованной на титрование холостой и анализируемой проб, соответствует количеству гидроксида калия, затраченному на омыление эфиров и нейтрализацию свободных кислот, содержащихся в пробе.
Содержание отчета.
m1 – масса стекла + навеска, (г) =
m1 – масса пустого сткла, (г) =
mн1 – масса навески, (г) =
m2 – масса стекла + навеска, (г) =
m2 – масса пустого сткла, (г) =
mн2 – масса навески, (г) =
C – концентрация соляной кислоты (моль/дм3) =
– объем соляной кислоты, пошедший на титрование пробы, (см3) =
– объем соляной кислоты, пошедший на титрование пробы, (см3) =
Vхол – объем соляной кислоты, пошедший на титрование холостого хода, (см3) =
Содержание числа омыления определяют по формуле:
 M(KOH) =56
г/моль
M(KOH) =56
г/моль
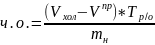 ,
мг/г
,
мг/г
ч.о.1=
ч.о.2=
 =
=
=
=
Погрешность методики ( )10%.
Расчет сходимости
d=( )
=
)
=
dk=0,1* =
ВОК сходимости пройден, если d<dk
Эфирное число соответствует количеству миллиграммов едкого калия, необходимого для омыления сложных эфиров, содержащихся, в 1 г исследуемого вещества.
Эфирное число определяют как разность между числом омыления и кислотным числом.
э.ч. = ч.о. к.ч., мг/г
э.ч. =
Выводы:
Контрольные вопросы.
Какая реакция лежит в основе определения сложных эфиров?
От каких параметров зависит скорость омыления?
Чем омыляются плохо растворимые в воде эфиры?
Какой индикатор применяется для определения Ч.О.?
По какому признаку судят о завершении омыления исследуемого вещества?
Литература.
К.и.Годовская. «Технический анализ». М., Высшая школа, 1972.
