
- •Лекция 1 «Хладагенты неорганического происхождения»
- •1 История развития
- •2 Требования, предъявляемые к хладагентам
- •3 Обозначение и классификация хладагентов
- •3.1 Хладагенты неорганического происхождения
- •3.1.1 Обозначение хладагентов
- •3.1.2 Теплофизические и химические свойства
- •4 Атомно-молекулярная теория
- •5 Газовые законы
- •5.1 Объединенное уравнение газовах законов. Газовая постоянная
- •5.2 Закон Дальтона. Парциальное давление
- •5.3 Закон Бойля-Мариотта. Сжижение газов. Критические давление, температура, объем
- •5.4 Уравнение Клапейрона-Менделеева
- •5.5 Уравнение Ван-дер-Ваальса
- •Лекция 2
- •1 Обозначение хладагентов
- •2 Основные химические свойства
- •3 Классификация хладагентов
- •Лекция 3 «Цепные реакции. Молекулярно-кинетическая теория. Физические принципы понижения температуры»
- •1 Цепные реакции
- •1.2 Линейная цепная реакция
- •1.3 Разветвленная цепная реакция.
- •1.4 Взрываемость и самовоспламенение
- •2 Молекулярно–кинетическая теория
- •3. Физические принципы понижения температуры
- •1) Дросселирование (эффект Джоуля-Томсона).
- •2) Расширение в вихревой трубе (эффект Ранка-Хильша).
- •3) Термоэлектрический эффект (эффект Пельтье).
- •4) Расширение с совершением полезной работы.
- •5) Электрокалорический эффект охлаждения (эк).
- •7) Намагничивание сверхпроводников.
- •8) Механокалорический эффект.
- •1 Парокомпрессионные холодильные машины
- •2 Теплоиспользующие холодильные машины
- •Лекция 4 «абсорбционные холодильные машины»
- •1 Абсорбция
- •3 Растворы
- •3.1 Общие свойства растворов
- •3.1.1 Классификация систем, состоящих из двух и более веществ
- •3.1.2 Способы выражения состава растворов
- •9 Коррозия металлов
- •9.1 Виды и типы коррозии
- •9.2 Способы защиты металлов от коррозии
- •9.2.1 Изолирование металлов от внешней среды
- •9.2.2 Изменение состава коррозионной среды
- •9.2.3 Рациональное конструирование
- •9.2.4 Электрохимические способы защиты от коррозии
- •Ингибиторы коррозиии
- •Глава 1. Ингибиторы коррозии на основе комплексов переходных металлов и азотсодержащих алифатических и ароматических соединений (обзор литературы)
- •Глава 1. Ингибиторы коррозии на основе комплексов переходных металлов и азотсодержащих алифатических и ароматических соединений (обзор литературы)
- •1.1. Ингибиторы коррозии для водных сред, содержащих кислород
- •1.2. Ингибиторы на основе азотсодержащих алифатических и ароматических соединений
- •1.3. Ингибиторы сероводородной коррозии
- •1.4. Ингибиторы углекислотной коррозии
- •1.5. Ингибиторы коррозии в нейтральных средах
- •Список использованной литературы
4 Атомно-молекулярная теория
В основе современных представлений о строении вещества лежит атомно-молекулярная теория.
Вещество – вид материи, обладающий при данных условиях определёнными физическими свойствами. Вещества состоят из атомов или молекул. Атом и молекула – это наименьшие частицы вещества. Так как атом и молекула являются крайне малыми частицами вещества (например, одна молекула аммиака имеет массу 2,83·10-23 г), на практике пользуются таким количеством вещества как моль.
Атом – электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов. Главной характеристикой атома является заряд ядра, равный числу протонов в атоме. В состав ядра любого атома, за исключением изотопа водорода 1Н, входят также нейтральные частицы нейтроны.
Элемент – разновидность атомов, имеющих одинаковый заряд ядра.
Изотоп – вид атомов, имеющих одинаковый заряд ядра, но разную массу. Наличие изотопов связано с различным содержанием нейтронов в атоме одного элемента. Изотопы по физическим константам и химическим свойствам отличаются незначительно. Исключение составляют изотопы водорода: протий (Н) – 1Н, дейтерий (D) – 2Н и тритий (Т) – 3Н. При переходе от протия к дейтерию и тритию атомная масса возрастает соответственно в два и три раза, что приводит к значительному различию в физических и химических свойствах данных изотопов.
Молекула – это наименьшая частица вещества, обладающая его химическими свойствами.
Моль – это количество вещества, содержащее 6,02·1023 (число Авогадро) атомов, молекул или др. структурных единиц. Например, один моль NН3 содержит 6,02·1023 молекул NН3. Мольная масса обозначается буквой М и например, для аммиака записывается следующим образом: М(NН3) = 17 г/моль.
Количество молей вещества обозначается n(х) и вычисляется по формуле
-
n(х) =
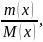 (1)
(1)
где
m(x)
– масса
вещества
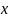 ,
,
М(х)
–
мольная масса вещества
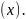
Например: если m(Н2SО4) = 9,8 г, то n(Н2SО4) = 9,8 ∕ 98 = 0,1 моль.
Закон Авогадро – в равных объемах любых газов при одинаковых условиях содержится одинаковое число газообразных частиц. Это связано с тем, что при обычных условиях в газах расстояния между отдельными молекулами настолько велики, что собственный размер молекул практически не влияет на общий объем газа. На практике широко применяется следствие из закона Авогадро – один моль любого газа при нормальных условиях (0 0С, 1 атм) занимает объем 22,4 л (мольный объем).
На примере молекулы углекислого газа (CO2) покажем связь между различными способами выражения количества вещества:
1моль CO2 содержит 6·1023 молекул CO2 , имеет массу 44 г и занимает объм 22,4л (н.у.).
5 Газовые законы
5.1 Объединенное уравнение газовах законов. Газовая постоянная
Состояние вещества в виде газа характеризуется определенными значениями: давления (Р), объема (V) и температуры(Т). Эти величины связаны между собой объединенным уравнением газовых законов:
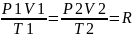
где, R – универсальная газовая постоянная.
В случае идеального газа, взятого при стандартных условиях, получаем:
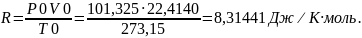
Универсальная газовая постоянная имеет физический смысл – это работа расширения одного моля газа на 1 градус при постоянном давлении.
