
- •1Часть іі. Углеводороды
- •6.1. Номенклатура неразветвленных (линейных) алканов.
- •6.2. Изомерия алканов
- •6.3. Названия алкильных радикалов
- •6.4. Номенклатура разветвленных алканов.
- •6 .5. Получение алканов.
- •6.6. Физические свойства алканов.
- •6.7. Химические свойства алканов.
- •6.8. Циклоалканы.
- •7.1. Гомологический ряд, номенклатура, изомерия.
- •7.2. Методы получения.
- •8.1. Классификация и номенклатура.
- •8.2. Методы синтеза.
- •8.3. Химические свойства.
- •9.1. Гомологический ряд алкинов. Номенклатура.
- •9.2. Методы получения алкинов.
- •9.3. Химические свойства ацетиленов.
- •10.1. Введение.
- •10.2. Понятие об ароматичности.
- •10.3. Одноядерные арены. Гомологический ряд бензола.
- •11.1. Полиядерные арены с изолированными бензольными ядрами.
- •11.2. Конденсированные ароматические соединения.
6 .5. Получение алканов.
6.5.1. Природные источники алканов.
Основные источники алканов – газ и нефть. Газ и нефть разделяют на фракции разгонкой: газ при пониженных температурах и давлении, нефть при нагревании.
6.5.2. Лабораторные методы получения.
6.5.2.1. Гидрирование непредельных углеводородов.
С
 Н2=СНR
+ H2
(Ni, Pt) CН3СН2R
Н2=СНR
+ H2
(Ni, Pt) CН3СН2R
6.5.2.2. Реакция Вюрца для первичных галогеналканов.
2 RCl + 2 Na 2 NaCl + RR
Это метод синтеза симметричных алканов. Из вторичных и третичных производных образуются главным образом алкены.
6.5.2.3. Восстановление иодистоводородной кислотой HJ
галогенпроизодных алканов, спиртов и т.д.
R Cl
+ 2 HI RН + НCl + I2
,
Cl
+ 2 HI RН + НCl + I2
,
R ОН + 2 HI RН + Н2О + I2 .
6.5.2.4. Сплавление солей карбоновых кислот со щелочью.
R
 COONa
+ NaOH
RH + Na2CO3
.
COONa
+ NaOH
RH + Na2CO3
.
6.5.2.5. Получение из магнийорганических соединений.
R Br + Mg (в эфире) RMgBr (+ H2O) RH + Mg(OH)Br
6.5.2.6. Метод Кольбе: электролиз водных солей карбоновых кислот.
На аноде анион карбоновой кислоты окисляется:
R COO е RCOO R + СО2 ;
Р екомбинация радикалов: R + R RR .
6.6. Физические свойства алканов.
Первые 4 членов гомологического ряда алканов при н.у. газы, С5 – С15 - жидкости, начиная с 16-го гомолога – твердые вещества. При увеличении молекулярной массы нормального алкана растет как его температура кипения, так и температура плавления. Причина – наличие дисперсионных сил, зависящих как от числа атомов в молекуле, так и от сближения этих атомов (от их упаковки). Поэтому нормальные алканы кипят при более высокой температуре, чем их разветвленные изомеры, поскольку в жидкости первые упакованы плотнее, чем вторые.
Алканы с очень длинной цепью, например, полиэтилен (продукт полимеризации этилена) с молекулярным весом 10 000 еще могут плавиться, но их кипение невозможно, поскольку это вещество разлагается, не переходя в пар при любом вакууме. Причина – дисперсионные взаимодействия в такой жидкости сильнее, чем связь СС.
6.7. Химические свойства алканов.
Алканы, как насыщенные углеводороды, не вступают в реакции присоединения. Они весьма инертны и не взаимодействуют при н.у. с кислотами, щелочами, окислителями и активными металлами, поскольку сами не полярные и содержат неполярные связи СС и малополярные связи СН. Поэтому их называют еще парафинами (лат. – parum afinitas – лишенные сродства).
 Связи
в парафинах трудно поляризуются,
образование из них ионов требует намного
больше энергии, чем образование радикалов.
Поэтому для алканов наиболее характерны
реакции по радикальному механизму.
Связи СН
прочнее связей СС,
однако они доступнее, вследствие чего
атом водорода в алканах может быть
оторван с образованием радикалов: R3C
: H R3C
+ H
.
Связи
в парафинах трудно поляризуются,
образование из них ионов требует намного
больше энергии, чем образование радикалов.
Поэтому для алканов наиболее характерны
реакции по радикальному механизму.
Связи СН
прочнее связей СС,
однако они доступнее, вследствие чего
атом водорода в алканах может быть
оторван с образованием радикалов: R3C
: H R3C
+ H
.
Прочность связи СН уменьшается в ряду: СН3Н СН3СН2Н (СН3)2СНН (СН3)3СН. Причем, увеличение стабильности образующихся из углеводородов радикалов имеет место в том же ряду:
Ряд СН3 СН3СН2 (СН3)2СН (СН3)3С
Число резонансных структур, опи- 1 4 7 10
сывающих строение радикалов.
Причиной стабилизации углеводородных радикалов, как уже упоминалось в лекции № 5, является гиперконьюгация соседних с радикальным центром водородных атомов, находящихся по отношению к нему в -положении. При этом для метильного радикала гиперконьюгация отсутствует ввиду его строения, тогда как для остальных она имеет место и усиливается по мере увеличения числа метильных групп, связанных с радикальным центром. Строение этильного радикала можно описать 4-ма резонансными структурами:
Д ля
изопропильного радикала таких структур
7, а для трет-бутильного их уже 10. Известно,
что чем больше резонансных структур,
тем стабильнее система, строение которой
они описывают.
ля
изопропильного радикала таких структур
7, а для трет-бутильного их уже 10. Известно,
что чем больше резонансных структур,
тем стабильнее система, строение которой
они описывают.
Таким образом, при радикальном замещении в первую очередь отрывается атом водорода от третичного углерода, т.е. реакционная способность алканов возрастает в том же ряду, что и стабильность образующихся из них радикалов.
Исходя из всего сказанного, можно сделать заключение, что для алканов характерны 2 типа химических реакций:
Замещение водорода по радикальному механизму SR ;
Расщепление молекул по связям СН и СС.
6.7.1. Реакции замещения.
6.7.1.1. Реакции галогенирования.
Э то реакции типа Х2 + RН RХ + НХ (SR) . Радикальный цепной
механизм хлорирования метана показан в разделе 5.5.1 в лекции № 5.
Реакционная способность галогенов в этих реакциях уменьшается в ряду:
F2 Cl2 Br2 I2 .
Реакции фторирования настолько экзотермичны, что идут со взрывом, образуя сажу (С) и НF. Однако, фторирование можно провести при низких температурах, например, разбавив F2 жидким азотом. .
Реакции хлорирования в темноте и при комнатной температуре не идут, однако, при освещении или при нагревании эти реакции идут очень бурно, ибо все стадии цепного радикального процесса (кроме инициирования) экзотермичны (механизм см. в лекции № 5). В метане все водороды легко можно заменить на хлор, т.е. получить СН3Cl, СН2Cl2, СНCl3 и СCl4 (хлористый метил, хлористый метилен, хлороформ и четыреххлористый углерод).
Реакции бромирования идут в 250 000 раз медленнее, чем хлорирования, поскольку стадия развития цепи Br + HR HBr + R здесь эндотермична (в отличие от хлорирования).
Реакции с I2 не идут по 2-м причинам: они очень медленны, а образующийся НJ восстанавливает продукты реакции до исходного алкана. Однако, иод производные алканов можно получить по реакции Финкельштейна в ацетоне, в котором NaI растворим, а NaCl нет, вследствие чего реакция и идет:
 RCl
+ NaI RI
+ NaCl .
RCl
+ NaI RI
+ NaCl .
Региоселективность при хлорировании и бромировании различна, как это следует из представленных в следующей таблице данных:
Х |
HR |
Контроль |
||
RСН2Н |
R2СНН |
R3СН |
||
Cl , 25 оС |
1 |
4 |
5 |
Кинетический при освещении |
Cl , 450 оС |
1 |
1 |
1 |
Термодинамический |
Br , 25 оС |
1 |
200 |
19 000 |
Кинетический при освещении и t |
Как видно, региоселективность хлорирования весьма незначительная, при высокой температуре исчезает, ибо при этом кинетический контроль реакции меняется на термодинамический. Что же касается бромирования, то здесь региоселективность весьма высокая.
Как уже отмечалось, причиной стабильности радикалов, которая растет в ряду RСН2 R2СН R3С, является гиперконьюгация, вследствие чего и снижается энергия активации (барьер, который нужно преодолеть) и возрастает скорость реакции. Однако, эта скорость различна в зависимости от структуры переходного состояния, о чем свидетельствует диаграмма зависимости свободной энергии от пути реакции, представленная на рис. 6.1.
Существует принцип Хеммонда, наглядно вытекающий из диаграммы на рис. 6.1 и утверждающий, что переходные состояния экзотермических реакций реагентоподобны (на координате реакции ближе к реагентам), для эндотермических – продуктоподобны (на координате реакции ближе к продуктам). Причем, чем экзотермичнее процесс, тем реагентоподобнее переходное состояние, и чем эндотермичнее процесс, тем продуктоподобнее переходное состояние.
Как видно из рис. 6.1, в соответствии с принципом Хеммонда переходное состояние экзотермической реакции с участием радикала хлора реагентоподобно (всего на 3% продвинуто к конечному радикальному состоянию), тогда как для эндотермической реакции с участием радикала брома – продуктоподобно (уже на 97% оно радикал). Поэтому гиперконьюгация в реакции хлорирования вносит малый вклад в стабилизацию переходного состояния и в изменении скорости отрыва водорода от разных положений мало отличаются, тогда как при бромировании, наоборот, гиперконьюгация вносит максимальный вклад в стабилизацию переходного состояния и скорости сильно отличаются.
Р ис.
6.1. Изменение свободной энергии по ходу
реакции радикального замещения.
ис.
6.1. Изменение свободной энергии по ходу
реакции радикального замещения.
6.7.1.2. Реакции нитрования и сульфирования алканов.
Концентрированные H2SO4 и HNO3 при н.у. с алканами не реагируют, а при нагревании окисляют. Однако и нитрование, и сульфирование можно провести в газообразных условиях или в парах.
6.7.1.2.1. Реакции нитрования (метод Коновалова).
 Используется
разбавленная азотная кислота при
нагревании, механизм SR,
имеет место региоселективность в ряду
RСН3
R2СН2
R3СН:
Используется
разбавленная азотная кислота при
нагревании, механизм SR,
имеет место региоселективность в ряду
RСН3
R2СН2
R3СН:
6.7.1.2.2. Реакции сульфохлорирования.
В промышленности проводят реакции алканов с SO2 и Cl2 в газовой фазе при облучении. Механизм подобен реакции хлорирования метана, однако, добавляется еще одна промежуточная стадия:
 h
h
Cl2 2 Cl
Атом Н при вторичном углероде реагирует быстрее, но при третичном углероде не реагирует совсем вследствие стерических препятствий (SO2 занимает большой объем). Образующиеся сульфохлориды подвергаются щелочному гидролизу:
RSO2Cl + 2NaOH NaCl + H2O + RSO2ONa
Такие соли сульфоновых кислот используются в качестве моющих средств и поверхностно активных веществ (ПАВ).
6.7.2. Реакции расщепления.
6.7.2.1. Каталитическое дегидрирование.
Это расщепление связи СН:
Cr2O3 /450 oC
С Н3СН2СН3
СН3СН=СН2
+ Н2
Н3СН2СН3
СН3СН=СН2
+ Н2
6.7.2.2. Окисление алканов.
Алканы сгорают на воздухе с образованием СО2 и Н2О и с выделением большого количества тепла, поэтому в быту и в промышленности эти реакции используются для получения тепла. Алканы – энергоносители, они широко используются как топливо для двигателей внутреннего сгорания (бензин, керосин, дизельное топливо). При низких температурах и при катализе в промышленности можно получать смесь разнообразных продуктов – кетонов, кислот, альдегидов. Это процессы радикальные, сложные, у нас нет времени на них останавливаться.
6.7.3. Крекинг алканов.
Крекинг – основной способ переработки нефти. Различают 2 процесса: некаталитический и каталитический.
6.7.3.1. Термический (некаталитический) крекинг
Процесс проводят при температуре выше 800 oC, процесс радикальный. Основная реакция – разрыв связи СС:
R
 CH2CH2
: CH2R
RCH2CH2
+ CH2R
RCH=CH2
+ RCH3
.
CH2CH2
: CH2R
RCH2CH2
+ CH2R
RCH=CH2
+ RCH3
.
Образующееся в результате этого процесса топливо имеет низкое качество: низкое октановое число и содержит нестабильные компоненты (алкены) в большом количестве. Поэтому для получения высококачественного бензина используют каталитический крекинг.
6.7.3.2. Каталитический крекинг.
Э тот
процесс протекает уже при температуре
450 - 550 oC
в присутствии электрофильных катализаторов
типа алюмосиликатов и кислот Льюиса
(AlCl3,
BF3 и
др.), Процесс ионный:
тот
процесс протекает уже при температуре
450 - 550 oC
в присутствии электрофильных катализаторов
типа алюмосиликатов и кислот Льюиса
(AlCl3,
BF3 и
др.), Процесс ионный:
Скажем, если R = CH3CH2CH2 , тогда:
П
 ри
изомеризации происходит гидридный
(Н:)
или метидный (СН3:)
перенос (1,2-сдвиг). Далее образовавшийся
карбокатион либо отрывает гидрид анион
от соседних молекул RH, либо присоединяется
по двойной связи:
ри
изомеризации происходит гидридный
(Н:)
или метидный (СН3:)
перенос (1,2-сдвиг). Далее образовавшийся
карбокатион либо отрывает гидрид анион
от соседних молекул RH, либо присоединяется
по двойной связи:
Обрыв цепи происходит за счет взаимодействия карбокатионов с алюминий гидрид анионом:
R + + HAlCl3 RH + AlCl3
В промышленности для каталитического крекинга применяют алюмосиликатные катализаторы, как естественные глины, так и искусственные кислые силикаты.
При крекинге, особенно в присутствии катализаторов, протекает также целый ряд вторичных процессов: дегидрирование до олефинов, полимеризация олефинов, алкилирование изоалканов олефинами, циклизация алканов до циклоалканов и дегирогенизация последних до ароматических соединений, коксование и другие. Состав продуктов крекинга в промышленности регулируют продолжительностью и температурой крекинга, а также применением высокого давления и различных катализаторов.
Часто крекинг-процесс комбинируют с риформингом, добавляя к силикатам в качестве катализаторов металлы (например Cr, Mo и другие). Риформинг это процесс циклизации алканов и превращения их в ароматические соединения.
Получаемые при помощи каталитического крекинга бензины являются высококачественными, ибо содержат мало алкенов и много разветвленных углеводородов с высоким октановым числом ( 95), обладающих высокими антидетонационными свойствами..
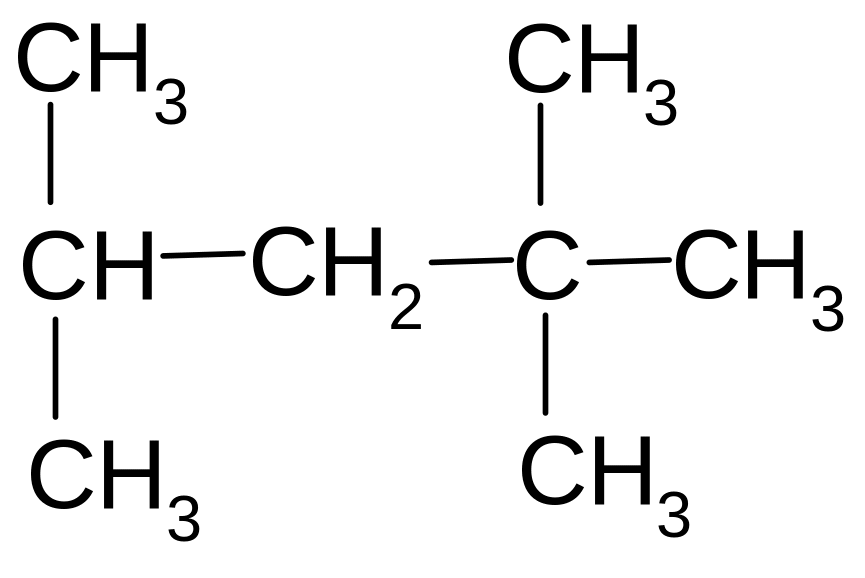 Октановое
число бензинов и индивидуальных
углеводородов определяют путем сравнения
их антидетонационных свойств с такими
же свойствами смеси нормального гептана
(октановое число 0, ибо он сильно
детонирует) с изооктаном
(2,2,4-триметилпентаном):
Октановое
число бензинов и индивидуальных
углеводородов определяют путем сравнения
их антидетонационных свойств с такими
же свойствами смеси нормального гептана
(октановое число 0, ибо он сильно
детонирует) с изооктаном
(2,2,4-триметилпентаном):
Октановое число изооктана принимается за 100, а его содержание в % в смеси с н-гептаном принимают за октановое число того углеводорода, анти детонационные свойства которого и исследуемой смеси одинаковы.
