
- •Республики беларусь Высшее учебное учреждение «Командно-инженерный институт»
- •Методические указания к решению задач и контрольные задания по разделу «Процессы горения. Опасные факторы пожара»
- •Введение
- •Общие методические указания
- •Рекомендуемый порядок действий при решении задач
- •Примеры решения задач
- •1. Материальный баланс процессов горения
- •1.1. Расчет количества воздуха, необходимого для горения веществ Расчетные формулы
- •Примеры
- •Объем воздуха, израсходованного на горение 1 м3 аммиака, определим по формуле (1.7):
- •1.2. Расчет объема и состава продуктов горения Расчетные формулы
- •Здесь – теоретический объем продуктов горения;
- •Состав продуктов горения, т.Е. Содержание I-го компонента (% об.), определяется по формуле:
- •Примеры
- •2. Тепловой баланс процессов горения
- •2.1. Расчет теплоты сгорания веществ Расчетные формулы
- •Примеры
- •2.2. Расчет температуры горения
- •Примеры
- •6 Моль, 3 моля, 26,32 моля, ,
- •Концентрационные пределы воспламенения
- •Примеры
- •4. Температурные параметры пожарной опасности веществ
- •4.1 Расчет температурных пределов воспламенения
- •Примеры.
- •4.2. Расчет температур вспышки и воспламенения
- •Примеры
- •4.3. Расчет температуры самовоспламенения
- •Расчет температуры потухания
- •Примеры
- •4.5. Температура и давление взрыва при взрыве паровоздушных смесей
- •Примеры
- •Перечень контрольных задач
- •Приложение
- •Энтальпия (теплосодержание) газов при постоянном давлении
- •Энтальпия (теплосодержание) газов при постоянном давлении
- •Теплота образования и сгорания некоторых веществ
- •Показатели пожарной опасности некоторых газов
- •Показатели пожарной опасности некоторых жидкостей
- •Величины параметров k и l для вычисления
- •Давление насыщенных паров некоторых веществ, гПа
- •Продолжение таблицы 7
- •Температура самовоспламенения (к) некоторых предельных углеводородов
- •Температура самовоспламенения (к) некоторых предельных одноатомных спиртов в зависимости от средней длины углеродной цепи
- •Значение параметров для расчета минимальной флегматизирующей
- •Внутренняя энергия газов
- •Литература
- •Содержание
4. Температурные параметры пожарной опасности веществ
4.1 Расчет температурных пределов воспламенения
Существует несколько полуэмпирических методов расчета ТПВ, однако они мало отличаются друг от друга по точности.
Температурные пределы воспламенения жидкостей рассчитываются по температуре кипения:
![]() (4.1)
(4.1)
где
![]() нижний
(верхний) температурный предел
воспламенения, оС;
нижний
(верхний) температурный предел
воспламенения, оС;
![]() температура
кипения, оС;
температура
кипения, оС;
k, l – константы для определенных групп (гомологических рядов) жидкостей.
Их значения приведены в табл. 6 приложения.
Для индивидуальных жидких веществ температурные пределы воспламенения можно определить по формуле:
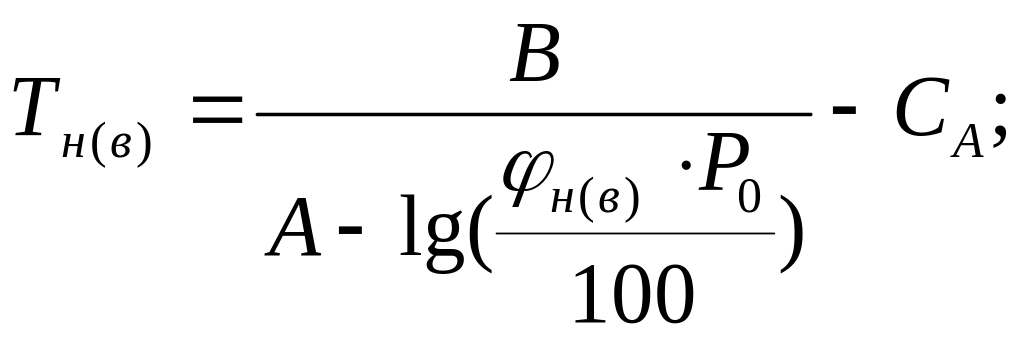 (4.2)
(4.2)
где А, В, СА - константы уравнения Антуана;
Ро – атмосферное давление, кПа;
![]() соответственно
нижний (верхний) концентрационные
пределы воспламенения.
соответственно
нижний (верхний) концентрационные
пределы воспламенения.
В случаях, не предусмотренных выше, нижний концентрационный предел воспламенения может быть определен по значению температуры вспышки:
![]() (4.3)
(4.3)
где
С – константа, равная 2, если для расчета
используем значение
![]() в закрытом тигле, и равная 8, если для
решения используют значение
в открытом тигле.
в закрытом тигле, и равная 8, если для
решения используют значение
в открытом тигле.
Значения могут быть взяты из справочной литературы или определены одним из расчетных методов.
Температурные пределы воспламенения могут быть определены по известным значениям концентрационных пределов:
![]() , (4.4)
, (4.4)
где
![]() давление насыщенного пара, соответствующее
нижнему (верхнему) концентрационному
пределу воспламенения;
давление насыщенного пара, соответствующее
нижнему (верхнему) концентрационному
пределу воспламенения;
нижний (верхний) концентрационный предел воспламенения;
![]() атмосферное
давление.
атмосферное
давление.
По таблице 7 приложения определяем температуру вещества, при которой достигается данное давление. Она будет являться соответственно нижним (верхним) пределом воспламенения.
Примеры.
Пример 1. Определить ТПВ метилового спирта, если температура его кипения равна 65 оС.
Решение.
Расчет проводим по формуле (4.1), значения констант определяем по табл. 6 приложения для нормальных жирных спиртов:
![]()
![]()
Определим относительную ошибку расчета. По табл. 5 приложения находим, что ТПВ метилового спирта равны 280-312 К.
![]()
![]() .
.
Следовательно, результаты расчета занижены менее чем на 3 %.
Пример 2. Определить температурные пределы воспламенения ацетона, если его концентрационные пределы в воздухе равны 2,2–13 %. Атмосферное давление – нормальное.
Решение.
По формуле (4.4) определим давление насыщенного пара ацетона, соответствующее нижнему и верхнему температурным пределам воспламенения:
![]() гПа;
гПа;
![]() гПа.
гПа.
Из табл. 7 приложения следует, что НТПВ находится между температурами 241,9 и 252,2 К, а ВТПВ – между 271,0 и 280,7 К. Линейной интерполяцией определим ТПВ:
![]()
![]()
Зная справочные значения ТПВ ацетона (253-279 К, табл. 5 приложения), можно определить относительную ошибку расчета:
![]()
![]()
4.2. Расчет температур вспышки и воспламенения
Наиболее распространенным и достаточно точным является расчет температур вспышки и воспламенения по формуле В.И. Блинова:
![]() (4.5)
(4.5)
где
![]() температура
вспышки (воспламенения);
температура
вспышки (воспламенения);
![]() давление
насыщенного пара при температуре вспышки
(воспламенения);
давление
насыщенного пара при температуре вспышки
(воспламенения);
![]() коэффициент
диффузии паров горючего в воздухе;
коэффициент
диффузии паров горючего в воздухе;
n – стехиометрический коэффициент при кислороде – количество молей кислорода, необходимого для полного окисления (до СО2, Н2О, SO2) одного моля горючего вещества;
А – константа метода определения (табл. 4.1).
Таблица 4.1
Константа метода определения для расчета температуры вспышки и воспламенения
Температура вспышки или воспламенения (К) |
Значения параметра А
|
Температура вспышки в закрытом тигле |
28,0 |
Температура вспышки в открытом тигле |
45,3 |
Температура воспламенения |
53,3 |
При отсутствии данных по коэффициенту диффузии последний определяют по формуле:
![]() (4.6)
(4.6)
где коэффициент диффузии, м2/с;
mi – количество i-го элемента в молекуле горючего вещества;
![]() атомные
(элементные) составляющие (табл. 4.2).
атомные
(элементные) составляющие (табл. 4.2).
Таблица 4.2
Атомные составляющие для определения коэффициента диффузии
веществ
Название i-го элемента |
Значение
|
Углерод |
25-50* |
Водород |
1 |
Кислород |
17 |
Азот |
16 |
Сера |
48 |
Хлор |
37 |
Бром |
79 |
Йод |
104 |
Фтор |
16 |
*
Значение
![]() зависит
от числа атомов углерода и их положения
в молекуле горючего:
зависит
от числа атомов углерода и их положения
в молекуле горючего:
1)
![]() для
атомов углерода, входящих в ароматический
цикл;
для
атомов углерода, входящих в ароматический
цикл;
2)
![]() для атомов углерода в открытой цепи,
если их количество меньше или равно
восьми (
для атомов углерода в открытой цепи,
если их количество меньше или равно
восьми (![]() );
);
3)
![]() для
атомов углерода в открытой цепи при
С>8;
для
атомов углерода в открытой цепи при
С>8;
4)
![]() для атомов углерода, входящих в
неароматический цикл при
;
для атомов углерода, входящих в
неароматический цикл при
;
5)
![]() для
атомов углерода, входящих в неароматический
цикл, если С>8.
для
атомов углерода, входящих в неароматический
цикл, если С>8.
----------------------------------------------------------------------------------------------------
Простым, но менее точным является расчет температуры вспышки в закрытом тигле по формуле Элея:
![]() (4.7)
(4.7)
где
![]() температура вспышки, оС;
температура вспышки, оС;
температура кипения, оС;
К – коэффициент, определяемый по формуле:
![]() (4.8)
(4.8)
где
![]() количество
элементов углерода, водорода, серы,
азота, кислорода, хлора, фтора, брома в
молекуле горючего вещества.
количество
элементов углерода, водорода, серы,
азота, кислорода, хлора, фтора, брома в
молекуле горючего вещества.
Температура вспышки в закрытом тигле может быть определена по нижнему температурному пределу воспламенения:
![]() (4.9)
(4.9)
Эта
формула применима, если
![]()
Температуру воспламенения алифатических спиртов и сложных эфиров можно рассчитывать по формуле:
![]() , (4.10)
, (4.10)
где температура кипения вещества, оС;
К – эмпирический коэффициент, равный 6.10-4 для спиртов и 7.10-4 для сложных эфиров.
Температура вспышки смесей различных нефтепродуктов и других органических веществ может быть определена по формуле:
![]() (4.11)
(4.11)
где А – концентрация компонента смеси с более высокой температурой вспышки (% об.);
В – концентрация компонента смеси с более низкой температурой вспышки (% об.);
![]() температура
вспышки компонента А (оС);
температура
вспышки компонента А (оС);
![]() температура
вспышки компонента В (оС);
температура
вспышки компонента В (оС);
![]() эмпирический
коэффициент, определяемый по таблице
4.3 при
эмпирический
коэффициент, определяемый по таблице
4.3 при
![]() .
.
Таблица 4.3
Значение эмпирического коэффициента φ для расчета температуры вспышки смесей веществ
А |
В |
|
А |
В |
|
100 |
0,0 |
0,0 |
40 |
60 |
21,7 |
95 |
5 |
12,0 |
35 |
65 |
19,4 |
90 |
10 |
20,0 |
30 |
70 |
17,0 |
85 |
15 |
26,0 |
25 |
75 |
14,5 |
80 |
20 |
29,2 |
20 |
80 |
11,9 |
75 |
25 |
30,4 |
15 |
85 |
9,2 |
70 |
30 |
30,3 |
10 |
90 |
6,5 |
65 |
35 |
30,0 |
5 |
95 |
3,3 |
60 |
40 |
29,0 |
0,0 |
100 |
0,0 |
55 |
45 |
17,6 |
|
|
|
50 |
50 |
25,9 |
|
|
|
