
- •Раздел II: “Консервативная гинекология”
- •Иннервация женских внутренних половых органов.
- •Вульвит – воспаление наружных женских половых органов.
- •Сальпингоофорит – воспаление придатков матки.
- •Пельвиоперитонит – воспаление брюшины малого таза.
- •Параметрит – воспаление околоматочной клетчатки.
- •Гонорея – венерическая болезнь, вызываемая гонококками.
- •Туберкулез половых органов.
- •Понятия о хронических неспецифических воспалительных заболеваниях женских половых органов.
- •Хронические метроэндометрит и сальпингоофорит. Клиника, диагностика, лечение.
- •Трихомоноз женских половых органов.
Раздел II: “Консервативная гинекология”
I. КЛИНИЧЕСКАЯ И ТОПОГРАФИЧЕСКАЯ АНАТОМИЯ ВНУТРЕННИХ ПОЛОВЫХ ОРГАНОВ, КРОВОСНАБЖЕНИЕ, ИННЕРВАЦИЯ, ЛИМФАТИЧЕСКАЯ СИСТЕМА, СВЯЗОЧНЫЙ АППАРАТ, БРЮШИНА И КЛЕТЧАТКА МАЛОГО ТАЗА.
I Клиническая анатомии женских внутренних половых органов (см. “Вопросы по акушерству” раздел II, вопр. № 1).
II Кровоснабжение женских половых органов:
Кровоснабжение наружных половых органов осуществляется преимущественно за счет внутренней и наружной срамных артерий:
внутренняя срамная артерия (a. pudenda interna) берет начало от внутренней подвздошной артерии, идет вниз, выходит из полости таза, отдает ветви, идущие к наружным половым органам, промежности, влагалищу и прямой кишке;
наружные срамные артерии (aа. pudendaе ехternaе) ветви бедренной артерии (2-3 тонких стволика). Одна из этих артерий идет вверх и достигает надлобковой области, разветвляясь в коже, другие доходят к половым губам.
Главными источниками кровоснабжения внутренних половых органов являются маточные и яичниковые артерии:
маточная артерия (a. uterina) – парный сосуд, отходит от подчревной артерии, идет к матке по околоматочной клетчатке, распологающейся в основании широких связок, по пути перекрещивается с мочеточником, подходит к боковой поверхности матки на уровне внутреннего зева. В этом месте от маточной артерии отходит довольно крупная ветвь, снабжающая шейку и верхний отдел влагалища – шеечно-влагалищная ветвь (ramus cervico-vaginalis).
Основной ствол маточной артерии (ramus ascendens) поднимается, извиваясь по ребру матки вверх, отдает по пути многочисленные веточки, питающие стенки матки, и доходит до дна матки, где отдает веточку, идушую к трубе. После этого конечные ветви маточной артерии соединяются с веточками яичниковой артерии, идущими в верхнем отделе широкой связки;
Артериальные ветви, отходящие от основного, восходящего ствола маточной артерии, образуют густую сеть тонких кровеносных сосудов, обильно снабжающих кровью мышечную и слизистую оболочки и брюшинный покров матки;
яичниковая артерия (a. ovarica) – парный сосуд, отходит от брюшной аорты, несколько ниже почечной артерии, спускается вместе с мочеточником вниз, проходит по воронко-тазовой связке к верхнему отделу широкой связки, отдает ветви к яичнику и трубе. Конечный ствол яичниковой артерии анастомозирует с концевым отделом маточной артерии.
В кровоснабжении влагалища, кроме маточной и срамной артерий, участвуют также ветви пузырной и геморроидальной артерий.
Артерии половых органов сопровождаются одноименными венами, причем каждую артерию обычно сопровождают две вены. Вены внутренних половых органов образуют сплетения (маточно-яичниковое, пузырное и др.)
Иннервация женских внутренних половых органов.
В иннервации половых органов участвуют симпатическая и парасимпатическая нервная система, а также спинномозговые нервы.
Волокна симпатической НС, иннервирующие половые органы, берут начало от аортального и солнечного сплетений, направляются вниз и на уровне V поясничного позвонка образуют верхнее подчревное сплетение. От указанного сплетения отходят волокна, которые идут книзу и в стороны и образуют правое и левое нижние подчревные сплетения.
Нервные волокна от этих сплетений направляются к мощному маточно-влагалищному сплетению (тазовому сплетению). Маточно-влагалищное сплетение расположено в параметральной клетчатке, сбоку и кзади от матки, на уровне внутреннего зева шеечного канала. К этому сплетению подходят ветви тазового нерва, относящегося к парасимпатической нервной системе. Cимпатические и парасимпатические волокна, отходящие от маточно-влагалищного сплетения, иннервируют влагалище, матку, внутренние отделы маточных труб, мочевой пузырь. Тело матки иннервируется главным образом симпатическими волокнами, а шейка и влагалище – преимущественно парасимпатическими.
Яичник иннервируется симпатическими и парасимпатическими нервами из яичникового сплетения. К яичниковому сплетению подходят нервные волокна из аортального и почечного сплетений.
Наружные половые органы иннервируются в основном срамным нервом.
Таким образом, нервы внутренних половых органов связаны через аортальное, почечное и другие сплетения с нервами внутренних органов.
В стенках матки, труб и в мозговом слое яичника образуются густые нервные сплетения. Тончайшие нервные веточки, отходящие от этих сплетений, направляются к мышечным волокнам, покровному эпителию и всем другим клеточным элементам. В слизистой оболочке матки концевые нервные веточки направляются также к железам, в яичнике – к фолликулам и желтым телам. Тончайшие концевые нервные волокна заканчиваются в виде пуговок, колбочек и т.д. Эти нервные окончания воспринимают химические, механические, термические и другие раздражения.
Нервные окончания внутренних половых органов относятся к интерорецепторам, которые воспринимают раздражения из внутренних органов. Раздражения, воспринимаемые чувствительными нервными окончаниями, передаются по нервным волокнам в лежащие выше отделы НС, где располагаются центры, регулирующие деятельность внутренних половых органов. Импульсы из этих центров передаются по двигательным и секреторным нервным волокнам в половые органы и направляют их деятельность (сокращение мускулатуры, секреция желез, продукция гормонов и другое). Нервные центры, регулирующие деятельность половых органов, располагаются на разных уровнях ЦНС.
Лимфатическая система половых органов.
Лимфатическая система половых органов состоит из густой сети извилистых лимфатических сосудов и множества лимфатических узлов. Лимфатические пути и узлы располагаются преимущественно по ходу кровеносных сосудов. Лимфатические сосуды, отводящие лимфу от наружных половых органов и нижней трети влагалища, идут к паховым лимфатическим узлам. Лимфатические пути, отходящие от средней и верхней трети влагалища и шейки матки, идут к лимфатическим узлам, располагающимся по ходу подчревных и подвздошных кровеносных сосудов.
Из тела матки, труб и яичников лимфа отводится по сосудам, располагающимся вдоль яичниковой артерии, и идет к лимфатическим узлам, лежащим на аорте и нижней полой вене.
Между указанными системами лимфатических путей половых органов существуют анастомозы.
Связочный аппарат половых органов.
В нормальном положении матку с трубами и яичники удерживает подвешивающий аппарат, закрепляющий аппарат и поддерживающий аппарат:
Подвешивающий аппарат:
Круглые связки (lig. rotundum) – отходят от углов матки (немного кпереди и ниже места отхождения труб), идут под передним листком широкой связки к внутренним отверстиям паховых каналов. Пройдя паховый канал, круглые связки веерообразно разветвляются, прикрепляются к клетчатке лобка и больших половых губ. Круглые связки притягивают дно матки кпереди (наклонение кпереди). Во время беременности круглые связки утолщаются и удлиняются;
Широкие связки (lig. latum) – двойные листки брюшины, идущие от ребер матки до боковых стенок таза. В верхних отделах широких связок проходят трубы, в задних листках расположены яичники, между листками находится клетчатка, а также сосуды и нервы;
Крестцово-маточные связки (lig. sacrouterinum) отходят от задней поверхности матки в области перехода тела в шейку, идут кзади, охватывают с двух сторон прямую кишку и прикрепляются на передней поверхности крестца. Эти связки притягивают шейку матки кзади. Во время родов круглые и крестцово-маточные связки способствуют удержанию матки на месте;
Собственные связки яичников (lig. ovarii proprium) начинаются от дна матки сзади и ниже места отхождения труб и идут к яичникам;
Воронкотазовые связки (lig. infundibulopelvicum)
Прямокишечно-маточные мышцы (mm. rectouteri)
Закрепляющий аппарат матки (retinaculum uteri) состоит из соединительнотканных тяжей с небольшим количеством мышечных клеток, которые идут от нижнего отдела матки (зоны уплотнения клетчатки):
кпереди к мочевому пузырю и далее к симфизу;
к боковым стенкам таза (основные связки – lig. cardinale);
кзади, составляя соединительнотканный остов крестцово-маточных связок.
Поддерживающий аппарат составляют мышцы и фасции тазового дна, которые препятствуют опусканию вниз половых органов и внутренностей.
Клетчатка малого таза.
Под брюшинным покровом органов малого таза располагается тазовая клетчатка, которая прилегает к внутренним половым органам в разных отделах. Клетчатка заполняет все свободные промежутки между органами малого таза в той части, которая не покрыта брюшиной и располагается выше фасции таза. В рыхлой тазовой клетчатке выделяются области, где преобладает плотная волокнистая соединительная ткань. Эти участки уплотнения составляют, в частности, закрепляющий аппарат внутренних половых органов.
В тазовой клетчатке различают следующие отделы:
Околоматочная (параметральная) клетчатка – занимает пространство между листками широких связок от боковых стенок таза;
Околопузырная (паравезикальная) клетчатка;
Околовлагалищная (паравагинальная) клетчатка – окружает влагалище, располагается преимущественно в пространстве, идущем от боковых отделов влагалища до стенок таза;
Околопрямокишечная (параректальная) клетчатка – располагается вокруг прямой кишки.
Все указанные отделы тазовой клетчатки не ограничены, а связаны друг с другом многочисленными соединительнотканными элементами.
Тазовая клетчатка имеет большое значение. Рыхлая клетчатка способствует физиологической подвижности и правильному функционированию внутренних половых органов, мочевого пузыря и прямой кишки, позволяет органам менять объем (наполнение и опорожнение мочевого пузыря и прямой кишки, изменение величины матки в связи с беременностью и родами и другое). Плотные отделы тазовой клетчатки закрепляют тазовые органы в подвижно-подвешенном состоянии, участвуют в удержании матки и других отделов полового аппарата в нормальном положении. Клетчатка таза образует ложе для мочеточников, кровеносных и лимфатических сосудов, лимфатических узлов, нервных стволов и сплетений.
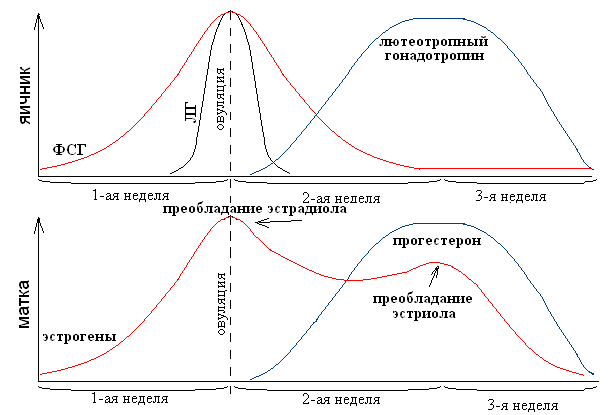
II. СОВРЕМЕННЫЕ ПРЕДСТАВЛЕНИЯ О НЕЙРО-ЭНДОКРИННОЙ РЕГУЛЯЦИИ МЕНСТРУАЛЬНОГО ЦИКЛА. ФАЗЫ МЕНСТРУАЛЬНОГО ЦИКЛА.
См. вопросы по акушерству (раздел I, вопрос 23).
Содержание в крови гонадотропных и стероидных гормонов в зависимости от фазы менструального цикла меняется следующим образом:
III. АЛГОРИТМ ПОСТАНОВКИ ДИАГНОЗА, РОЛЬ СИСТЕМЫ ОПРОСА И МЕТОДОВ ОБЩЕГО И СПЕЦИАЛЬНОГО ИССЛЕДОВАНИЯ В ДИАГНОСТИКЕ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ.
При обследовании гинекологических больных можно выделить следующие этапы:
Сбор анамнеза:
Паспортные данные – Ф.И.О., возраст, профессия, семейное положение, условия труда и быта.
Жалобы больной:
Боли, которые у гинекологических больных отличаются большим разнообразием по степени, характеру локализации, времени появления и т.д.:
- интенсивность болевых ощущений находится в связи с особенностями нервной системы, эмоциональным состоянием женщины, степенью вовлечения в патологический процесс нервных окончаний, растяжением висцеральной брюшины, обменными нарушениями в очаге воспаления, со специфичностью воспалительного процесса (при гонорейном воспалении придатков матки боли в острой стадии бывают интенсивными и длительными, при туберкулезном воспалении – боли могут быть сравнительно небольшими, даже при значительном распространении) и рядом др. факторов.
- нарастающими, схваткообразными, тянущими, давящими;
- боли могут возникать внизу живота (при заболеваниях матки), пояснично-крестцовой области (при загибе матки кзади - ретрофлексии), в подвздошно-паховых областях (при заболеваниях придатков матки);
- большое значение имеет время появления болей. Боли, регулярно возникающие в середине менструального цикла, могут быть связаны с овуляцией. Появление прогрессирующих болей во второй половине цикла, продолжающихся в течение 1-2-го дня менструации, характерно для эндометриоза. Боли, возникающие во время полового акта, чаще обусловлены хроническим воспалительным процессом придатков матки или позадишеечным эндометриозом;
- иррадиация болей. Иннервация матки находится в связи с XI-XII грудными и с III-V крестцовыми сегментами спинного мозга, поэтому отраженные боли при патологических изменениях этого органа появляются в нижней части спины, пояснице, иногда в подчревной области. При заболеваниях яичников и маточных труб боли ощущаются в нижней части спины, в поясничной, паховой и подчревной областях;
- реперкуссия – отражение раздражения из менее возбудимой области в более возбудимую, вследствие чего боль может ощущаться в области здорового органа, связанного общностью иннервации с патологическим очагом;
Нарушения функции половых органов (менструальной, половой, репродуктивной, секреторной);
Нарушение функции органов, связанной с половыми органами в анатомическом и функциональном отношении (мочевыводящие пути, прямая кишка);
Наследственность.
Перенесенные заболевания.
Функции половой системы:
Менструальная функция – является важнейшей функцией репродуктивной системы женщины и свидетельствует как о полноценности самой системы, так и о здоровье женщины в целом. При выяснении особенностей менструальной функции необходимо обращать внимание на следующие моменты:
В каком возрасте появились первые менструации и каков был их характер;
Через какой промежуток времени установился регулярный менструальный цикл;
Какова продолжительность цикла;
Сколько дней продолжается менструация и каково количество теряемой крови;
Изменение менструального цикла после начала половой жизни, абортов, родов и др.;
Время последней менструации;
Изменение цикла в связи с данным гинекологическим заболеванием.
Основные виды нарушения менструальной функции:
Аменорея – отсутствие менструаций;
Гипоменструальный синдром – ослабление (гипоменорея), укорочение (олигоменорея) и урежение (опсоменорея) менструаций;
Меноррагия – кровотечение, связанное с менструальным циклом, носящее циклический характер и проявляющееся увеличением кровопотери во время менструации (гиперменорея), большей продолжительностью менструальных кровотечений (полименорея) и нарушениями (укорочениями) их ритма (пройоменорея);
Метроррагия – ациклические маточные кровотечения, не связанные с менструальным циклом;
Альгодисменорея – болезненная менструация.
Половая функция:
Наличие полового влечения (либидо);
Наличие чувства удовлетворения (оргазм);
Нарушения половой функции – болезненность при половых сношениях, контактные кровотечения, затруднение или невозможность полового сношения;
Репродуктивная функция:
Время наступления беременности после начала половой жизни;
Количество беременностей, их течение и исходы;
Наличие осложнений беременности, родов и послеродового периода;
Число абортов, при каких сроках они проводились, были ли осложнения;
Секреторная функция – важный показатель состояния женских половых органов. При многих гинекологических заболеваниях, а также при патологических процессах, не связанных непосредственно с половой системой, происходит количественное или качественное изменение секрета.
Бели – патологические выделения из половых органов женщины:
Вестибулярные бели
Влагалищные бели
Шеечные бели
Маточные бели
Трубные бели.
Функции органов, связанных с половыми органами в анатомическом и функциональном отношении:
Мочевыделительная система
Прямая кишка.
История настоящего заболевания, которая анализируется в хронологическом порядке.
В результате подробного опроса больной можно сделать предварительное заключение о возможном характере заболевания.
II. Общее объективное обследование:
Изучение типов конституции:
Нормальный тип;
Гипрестенический тип – невысокий (средний) рост, длина ног по сравнению с длиной туловища незначительна. Кифоз спины мало выражен, поясничный лордоз расположен высоко, плечевой пояс относительно узок. Подкожный жировой слой развит хорошо. Специфические функции женского организма в большинстве случаев не изменены.
Инфантильный тип – может иметь место как общий (универсальный), так и половой (генитальный) инфантилизм без общих признаков недоразвития. Инфантильный тип характеризуется небольшим ростом, недоразвитием молочных желез, общеравномерносуженным тазом. Первая менструация нередко наступает позже обычного срока, а менструации характеризуются нерегулярностью и болезненностью.
Астенический тип – ему присуща анатомическая и функциональная слабость всей мышечной и с/т систем. У женщин астенического типа отмечаются расслабление мышечного и с/т аппарата тазового дна и промежности, нередко усиление, удлинение и болезненность менструаций.
Интерсексуальный тип – характеризуется недостаточной дифференцировкой пола, особенно вторичных половых признаков. Этому типу присущи физические и психические признаки мужского организма. Волосяной покров сильно развит, нередко по мужскому типу, черты лица напоминают мужские, половые органы часто гипопластичны.
Антропометрические исследования – имеют важное значение в диагностике эндокринных нарушений:
Окружность грудной клетки
Высота большого вертела от пола
Рост
Расстояние между большими вертелами бедер
Расстояние между плечевыми костями на уровне больших бугорков
Определение степени развития жировой ткани и ее распределения
Определение особенностей распределения волосяного покрова:
Лануго – нежное оволосение;
Оволосение, свойственное лицам обоего пола;
Оволосение, характерное для одного пола;
У женщин может иметь место:
Нормальное оволосение – в области лона и в подмышечных впадинах;
Гипертрихоз – выраженное оволосение на местах, характерных для женского организма (лобок, большие половые губы, подмышечные впадины);
Гирсутизм – усиленное оволосение по мужскому типу (на лице, межгрудной борозде, околососковых кружках, средней линии живота);
Вирилизм – совокупность признаков, характеризующихся появлением мужских черт, вызванных действием андрогенов.
Осмотр кожи.
Изучение состояния внутренних органов (по системам).
Cпециальное (гинекологическое) исследование:
Осмотр наружных половых органов.
Исследование с помощью зеркал – имеет большое значение для выявления пат. изменений влагалища и шейки матки.
Влагалищное исследование – производится путем введения II и III пальцев во влагалище. Позволяет определить ширину входа во влагалище, его длину, глубину, характеристики шейки матки (длина, состояние), состояние промежности и мышц тазового дна, тела матки и придатков.
Ректальное исследование – производят II пальцем. Оно помогает составить представление о состоянии шейки матки, паравагинальной и параректальной клетчатки, установить изменения в прямой кишке. К этому исследованию прибегают у пациенток, не живших половой жизнью.
Ректовагинальное исследование – выполняется введением II пальца во влагалище, а III пальца – в прямую кишку. Производится при подозрении на пат. изменения в параметральной клетчатке и прямокишечно-маточных мышцах.
Зондирование матки – осуществляется маточным зондом. Позволяет установить имеющиеся в полости матки деформации, пороки развития, длину полости матки, заращение внутреннего зева шейки матки.
Пункция брюшной полости через задний свод влагалища – проводят с целью дифференциальной диагностики между внематочной беременностью и воспалением придатков матки.
Биопсия – прижизненное иссечение небольшого участка ткани для микроскопического исследования. Проводится при подозрении злокачественности пат. процесса.
Хромодиагностика – смазывают пат. очаг и окружающие его здоровые ткани раствором Люголя. При этом неизмененный эпителий влагалища и шейки матки, содержащий достаточное количество гликогена, равномерно окрашивается в темно-коричневый цвет (йодпозитивная реакция). Пат. участки вследствие недостаточного количества гликогена раствором Люголя не окрашиваются и выделяются на коричневом фоне в виде более светлых пятен различных оттенков (йоднегативная реакция).
Раздельное диагностическое выскабливание слизистой оболочки шейки матки и тела матки – проводят для выяснения состояния слизистой при различных патологических процессах. Сначала производят введенной в полость матки кюреткой выскабливание слизистой оболочки всех стенок матки, а затем – слизистой оболочки канала шейки матки. Полученные соскобы помещают раздельно в сосуды с формалином и отправляют для гистологического исследования.
Аспирационная биопсия – осуществляется при помощи шприца Брауна, на который надевается специальный наконечник, вводимый в полость матки. Аспирируют небольшое количество свободно отделяющегося эндометрия, который наносят на предметное стекло, делают мазок, окрашивают и исследуют под микроскопом.
Аспирационный кюретаж – производится полой кюреткой, соединенной с вакуум-насосом.
Тесты функциональной диагностики (см. вопр. по акушерству, раздел I-й вопрос №23).
Исследование влагалищных мазков (бактериоскопическое) – позволяет определить степень чистоты влагалищного содержимого:
I степень – обнаруживают палочки молочно-кислого брожения (палочки Додерляйна), эпителиальные клетки, реакция влагалищного содержимого кислая;
II степень – умеренное количество палочек Додерляйна, имеются клетки плоского эпителия, единичные лейкоциты, реакция влагалищной среды слабокислая;
III степень – появление кокковой флоры, увеличение числа лейкоцитов, палочки Додерляйна практически не встречаются, реакция слабощелочная;
IV степень – разнообразная кокковая флора, большое количество лейкоцитов, отсутствие палочек Додерляйна, реакция щелочная.
Методы изучения проходимости маточных труб:
Пертубация – продувание маточных труб. В канал шейки матки под контролем манометра с помощью специального устройства нагнетают воздух с перерывами в 15-20 секунд. Давление в системе постепенно повышают. Если в течение 0,5-1 минуты давление не падает, проба считается отрицательной (трубы непроходимы).
Кимографическая пертубация позволяет выявить проходимость или непроходимость маточных труб, их спазм или стенозирование. Для получения пневмокимограмм пользуются специальным аппаратом.
Наилучшим временем для проверки проходимости труб является начало второй фазы менструального цикла.
Противопоказания к пертубации: острые и подострые воспалительные процессы в половых органах, III-IV степень чистоты влагалища, опухоли матки и придатков, общие инфекционные болезни, заболевания ССС;
Гидротубация – введение в маточные трубы (через полость матки) изотонического раствора хлорида натрия под давлением. При проходимости маточных труб давление жидкости, определяемое по показаниям манометра, по достижении определенной величины начинает снижаться. При непроходимости давление возрастает;
Метросальпингография (гистеросальпингография)
16. Рентгенологические методы
Метросальпингография – позволяет определить состояние матки и маточных труб. Исследование проводится с рентгенконтрастными растворами (йодолипол, кардиотраст и др.)
Рентгенологическая картина матки зависит от фазы менструального цикла:
Фолликулярная фаза – вследствие повышения тонуса матки полость матки имеет вид удлиненного треугольника с выраженной “талией” по бокам вследствие втянутости боковых линий, истмический отдел матки расширен (4-5 мм) и укорочен;
лютеиновая фаза – полость тела матки расширена, “талия” сглажена, истмический отдел матки резко сужен, что свидетельствует о пониженном тонусе матки.
Сократительная деятельность маточных труб также зависит от фазы менструального цикла:
в первой фазе тонус повышен;
во второй фазе – тонус труб понижен, перистальтика при этом становится ритмичной. Поэтому для определения функционального состояния маточных труб рентгенологическое исследование следует проводить во второй фазе менструального цикла.
Противопоказаниями к метросальпингографии являются инфекционные заболевания, общие и местные воспалительные процессы, воспалительные заболевания женских половых органов в острой и подострой стадиях, III и IV степени чистоты влагалища, предположение о наличии беременности, повышенная чувствительность к препаратам йода.
Внутриматочная флебография – по характеру заполнения контрастным веществом венозной сети позволяет судить о расположении и размерах миоматозных узлов (малососудистые зоны характерны для межмышечной локализации миоматозного узла, симптом “кольца” – для подбрюшинного узла), а также провести дифференциальный диагноз между опухолью яичников и опухолью матки;
Пневмоперитонеография органов малого таза – дает возможность определить контуры матки и яичников. Этот метод исследования используют для диагностики подбрюшинных миоматозных узлов, опухолей и склерокистозных изменений яичников;
Метросальпингография в сочетании с пельвиграфией – позволяет более точно определить локализацию опухоли и составить представление о ее взаимосвязи с окружающими тканями;
Кольпография – дает представление о величине, форме, емкости, наличии порока развития или атрезии влагалища;
Краниография – изучение области турецкого седла позволяет судить о нарушениях гипоталамо-гипофизарной системы;
Лимфография – позволяет выявить увеличение или изменение структуры лимфатических узлов, а также дифференцировать метастазы в лимфатические узлы от воспалительных изменений.
17. Эндоскопические методы исследования – осмотр внутренних половых органов с помощью специальных оптических инструментов и приборов. С помощью этих методов можно произвести прицельную биопсию.
В гинекологической практике применяются следующие основные эндоскопические методы:
Кольпоскопия – осмотр влагалища и влагалищной части шейки матки с помощью бинокулярной или монокулярной лупы, снабженной осветительным прибором (увеличение исследуемого участка в 30 раз и более);
Микроскопическая кольпоскопия (кольпомикроскопия) – кольпоскопия под большим увеличением (в 80-90 раз) с помощью контактного объектива и с предварительным окрашиванием области исследования;
Цервикоскопия – осмотр слизистой оболочки шейки матки с помощью цервикоскопа;
Гистероскопия – исследование внутренней поверхности матки с целью выявления патологических изменений эндометрия;
Перитонеоскопия (лапароскопия) – метод исследования, с помощью которого производится осмотр органов малого таза и брюшной полости оптическим инструментом, введенным в брюшную полость через отверстие в передней брюшной стенке.
С помощью лапароскопии можно выполнить ряд гинекологических оперативных вмешательств – стерилизацию (коагуляция маточных труб, наложение танталовой скобки или шва), рассечение и коагуляция спаек в малом тазу, коагуляция эндометриоидных очагов, пункция ретенционных образований яичников, коагуляция ткани яичника у больных с апоплексией яичников;
Кульдоскопия – осмотр органов малого таза с помощью оптического инструмента, введенного в брюшную полость через задний свод влагалища.
Противопоказаниями к эндоскопическим методам исследования являются тяжелое состояние больной, пороки сердца в стадии декомпенсации, недавно перенесенный инфаркт миокарда, резко выраженные склеротические изменения сосудов мозга и сердца у лиц преклонного возраста, тяжелые заболевания легких с нарушением их функции, фиксированная ретрофлексия матки, обширный спаечный процесс в брюшной полости, выполняющие весь малый таз опухолевые образования.
18. Ультразвуковое исследование (см. раздел I, вопр. 17).
19. Тепловидение – метод регистрации инфракрасного излучения, полученного с различных участков тела.
20. Диагностическое чревосечение (лапаротомия).
21. Гормональные методы диагностики – применяются для выявления причин нарушения менструальной функции и уровня поражения системы “гипоталамус-гипофиз-яичники-матка”. Они помогают проведению дифференциальной диагностики и выбору рациональной терапии. С этой целью ставятся пробы, стимулирующие или подавляющие функцию отдельных звеньев системы регуляции менструального цикла. Иногда проводят комбинированные пробы, основанные на сочетании стимуляции деятельности одной эндокринной железы и подавлении функции другой.
Применяют следующие пробы:
проба с рилизинг-фактором – применяется с фолликулстимулирующим рилизинг фактором (фоллиберином) и лютеинизирующим рилизинг-фактором (люлиберином). Основным показанием к проведению этой пробы является выяснение вопроса о поражении гипофиза в основном при аменорее центрального генеза. При патологических изменениях гипофиза пробы с фоллиберином и люлиберином являются отрицательными, поскольку стимулирующее воздействие не может дать ответной реакции со стороны гипофиза в виде усиления продукции фолликулостимулирующего и лютеинизирующего гонадотропинов. Если пробы с рилизинг-гормонами свидетельствуют о нормальной функции гипофиза, то аменорея центрального генеза обусловлена поражением гипоталамуса.
Оценка пробы с фоллиберином и люлиберином проводится на основании изучения содержания в крови фолликулостимулирующего и лютеинизирующего гонадотропинов с помощью радиоиммунных методов.
проба с фолликулостимулирующим гонадотропином – используется для определения функционального состояния яичников (при аменорее, задержке полового развития и др.) Обычно для этого используют пергонал (75 ЕД фолликулостимулирующего гонадотропина и 75 ЕД лютеинизирующего гонадотропина). После введения пергонала (5000 ЕД в течение 10 дней) определяют содержание эстрогенов в крови с следят за динамикой функциональных показателей (кариопикнотический индекс, симптомы “зрачка”, “листка папоротника”, натяжения слизи). При нормальной функции яичников проба положительная.
проба с хориогонином – применяется для уточнения состояния яичников. Хориогонин назначают в течение 5 дней внутримышечно по 1500-5000 ЕД. Результаты оценивают по повышению содержания прогестерона в крови и базальной температуре свыше 37°С. Если яичники способны функционально реагировать на стимулирующее влияние хориогонина, после его введения усиливается образование гормона желтого тела, что свидетельствует о центральном генезе нарушений. Отрицательные результаты пробы подтверждают первичную неполноценность яичников.
проба с прогестероном – используется в основном чтобы исключить маточную форму аменореи. Проба считается положительной, если через 2-3 дня после 6-8-дневного в/м введения прогестерона (10 мг в день) у больной появляется менструальноподобное кровотечение. Положительная проба не только позволяет исключить маточную форму аменорей, но и указывает на достаточную эстрогенную активность яичников. Отрицательная проба свидетельствует о глубоком поражении эндометрия или о наличии слабой эстрогенной стимуляции.
проба с эстрогенами и прогестероном – проводится после отрицательной пробы с прогестероном. Больной в течение 10 дней вводят один из эстрогенных препаратов, а затем назначают прогестерон в течение 8 дней. Положительная проба (появление менструальноподобной реакции) исключает маточную форму аменореи и свидетельствует о недостаточной эндокринной функции яичников.
проба с комбинированными эстроген-гестагенными препаратами (бисекурин, нон-овлон) проводится для определения функционального состояния гипоталамо-гипофизарной системы и ее резервных способностей. Эти препараты назначают по 21-дневной схеме в течение 3 месяцев. После отмены при хорошем состоянии гипоталамо-гипофизарной системы возникает эффект отдачи, в результате которого отмечается овуляция. Отсутствие ответной реакции после отмены препарата указывает на нарушение гипоталамо-гипофизарной системы.
проба с кломифеном (стимулятором овуляции).Его назначают по 50-100 мг в день с 5-го по 10-й день менструального цикла. При положительной реакции прием препарата сопровождается повышением секреции ФСГ и ЛГ, в результате чего происходит овуляция.
проба с кортизоном или дексаметазоном – применяется с целью определения источника повышенного содержания андрогенов. Проба основана на угнетении секреции АКТГ. Дексаметазон назначают по 0,5 мг 4 раза в день в течение 2 дней. Резкое снижение экскреции 17-кетостероидов с мочой свидетельствует о надпочечниковом генезе гиперандрогении.
проба с АКТГ – проводится для определения функционального состояния коры надпочечников. Введение АКТГ (по 40 ЕД в/м в течение 2 дней) вызывает резкое повышение содержания 17-кетостероидов в моче при надпочечниковом генезе заболевания и незначительное повышение – при яичниковом генезе.
22. Медико-генетические методы исследования (см. раздел I, вопр. 13, 14).
23. Цитологические методы исследования. Выделяют следующие типы цитограмм:
I тип – цитологические особенности соответствуют возрасту исследуемой;
II тип – при фоновых процессах
- IIa тип – клеточный состав, наблюдаемый при воспалении;
- IIб тип – пролиферативные процессы, возникающие на фоне воспаления;
III тип – изменения эпителия, соответствующие предопухолевым процессам (дисплазия)
- IIIа тип – слабая или умеренная дисплазия;
- IIIб тип – тяжелая дисплазия;
IV тип – отражает начало малигнизации, можно заподозрить рак;
V тип – изменения эпителия, позволяющие говорить о раке;
VI тип – нельзя сделать какое-либо заключение.
24. МЕТОДЫ ОБСЛЕДОВАНИЯ РЕПРОДУКТИВНОЙ СИСТЕМЫ ЖЕНЩИНЫ (См. вопр. 3)
25. МЕТОДЫ ИССЛЕДОВАНИЯ СОСТОЯНИЯ МАТОЧНЫХ ТРУБ И ИХ ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ ПРИ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЯХ (См. вопр. 3)
26. РЕНТГЕНОКОНТРАСТНЫЕ МЕТОДЫ ДИАГНОСТИКИ (МЕТРОСАЛЬПИНГОГРАФИЯ, ФЛЕБОГРАФИЯ), ИХ ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ (См. вопр. 3, пункт III 16)
27. ГОРМОНАЛЬНЫЕ МЕТОДЫ ДИАГНОСТИКИ В ГИНЕКОЛОГИИ (См. вопр. 3, пункт III 21)
28. КОЛЬПОСКОПИЯ, БИОПСИЯ, ДИАГНОСТИЧЕСКОЕ ВЫСКАБЛИВАНИЕ, ЦИТОЛОГИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ, ГИСТЕРОСКОПИЯ. ИХ РОЛЬ В ДИАГНОСТИКЕ ГИНЕКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ (См. вопр. 3)
9. ФИЗИЧЕСКИЕ, БАЛЬНЕОЛОГИЧЕСКИЕ МЕТОДЫ ЛЕЧЕНИЯ, ГИНЕКОЛОГИЧЕСКИЙ МАССАЖ, ЛЕЧЕБНАЯ ФИЗКУЛЬТУРА, САНАТОРНО-КУРОРТНОЕ ЛЕЧЕНИЕ ГИНЕКОЛОГИЧЕСКИХ БОЛЬНЫХ.
Физические методы лечения.
В основе механизма лечебного действия физических факторов наряду с их местным влиянием лежит рефлекторная реакция организма, реализуемая нейрогуморальным путем в виде активной саморегуляции трофических процессов на различных уровнях – от клеточного до организма в целом. Разнообразные физические факторы (средства), используемые в гинекологии с лечебной целью, объединяют в две основные группы:
Естественные (природные) факторы:
Климатотерапия – лечебное использование климатических факторов: воздушной среды (аэротерапия), солнечной радиации (гелиотерапия), морских купаний (талассотерапия). Этот вид лечения способствует повышению устойчивости организма к неблагоприятным условиям внешней среды и улучшению функций половой системы. Климатотерапия является действенным средством вторичной профилактики при рецидивирующих воспалительных заболеваниях половых органов и нейроэндокринных расстройствах, а также эффективным методом медицинской реабилитации, в т.ч. после хирургического лечения.
Водолечение – является непременным компонентом общетонизирующих и закаливающих лечебных мероприятий, особенно при нейроэндокринных гинекологических синдромах, расстройствах менструальной функции при гинекологических заболеваниях у детей и подростков. Наиболее часто в гинекологии используют обливания, обмывания, ванны (общие и местные, включая “тазовые”) и души. Положительной особенностью водолечения является возможность проведения процедур в домашних условиях (по рекомендации врача и под систематическим медицинским контролем). По сравнению со многими другими лечебными физическими факторами противопоказания к проведению таких воздействий очень ограничены.
Минеральные и радоновые ванны наиболее часто используют при хронических воспалительных заболеваниях внутренних половых органов, спаечных процессах в малом тазу, нарушениях гормональной функции яичников. Сероводородные (сульфидные), хлоридные натриевые, мышьякосодержащие (мышьяковистые) и углекислые воды усиливают эстрогенную активность яичников, а радоновые воды ее снижают. Специфической для гинекологии особенностью лечебного применения минеральных и радоновых вод является возможность проведения влагалищных орошений, сочетание которых с ваннами значительно повышает эффективность терапии.
Грязелечение (пелоидолечение). Основные показания к грязелечению: хронические воспалительные процесс внутренних половых органов при неизмененной и сниженной гормональной функции яичников, спаечные процессы в малом тазу, генитальный инфантилизм. Клиническая результативность иловых и торфяных лечебных грязей в гинекологии практически одинакова, что открывает большие возможности для внекурортного грязелечения. Специфической методической особенностью грязелечения гинекологических больных является широкое использование влагалищных грязевых тампонов, нередко в сочетании с ректальными.
Пелоидоподобные вещества (парафин, озокерит, глина, нафталанская нефть) – оказывают обезболивающее, противовоспалительное, рассасывающее, антиспазматическое действие, и по направленности влияния на гормональную функцию яичников (стимуляция эстрогенной активности) сходны с лечебными грязями. Поэтому показания к назначению пелоидов и пелоидоподобных веществ практически одинаковы.
Искусственные факторы (преформированные) – факторы, созданные путем преобразования одних форм энергии в другие с помощью специальных аппаратов (аппаратная физиотерапия):
Светолечение – показано с целью теплового воздействия (видимые и инфракрасные лучи) для получения анальгезирующего, дегидратирующего, десенсибилизирующего и противовоспалительного эффекта (УФ лучи) при стабилизированном и отграниченном (подостром) воспалении внутренних половых органов. В последнем случае светолечение является действенным средством профилактики спаечного процесса в органах малого таза.
Вибротерапия – при гинекологических заболеваниях в основном проводится с помощью ультразвука, обладающего болеутоляющим, десенсибилизирующим и выраженным дефиброзируюшим свойствами.
Ультразвуковая терапия – наиболее эффективна при хронических воспалительных заболеваниях внутренних половых органов и спаечных процессах в малом тазу. УЗ воздействия целесообразно сочетать с лекарственными гидротубациями, если целью лечения является устранение непроходимости маточных труб, обусловливающее бесплодие.
Электролечение. Разнообразие средств электролечения позволяет строго индивидуализировать воздействие, что значительно повышает его результат. Воздействие постоянным электрическим полем высокой напряженности показано при лечении нейроэндокринных гинекологических синдромов.
Переменные электромагнитные поля высокой, ультравысокой (УВЧ) и сверхвысокой (СВЧ) частоты (индуктотермия) применяются преимущественно при воспалительных заболеваниях половых органов. Индуктотермия наиболее эффективна при лечении хронических воспалительных процессов гениталий, а УВЧ- и СВЧ-терапия – при разрешающихся острых и обострившихся хронических воспалительных заболеваниях. Эти же факторы эффективны в качестве средств профилактики и ранней терапии послеоперационных инфильтратов.
Магнитное поле (постоянное и переменное) используется при тех же заболеваниях, что и УВЧ- и СВЧ-терапия. Кроме того, воздействие магнитных полей может быть применено при эндометриозе и миоме матки.
Токи высокого напряжения наиболее часто применяются в виде местной дарсоновализации, показанной при стойком болевом синдроме воспалительного генеза, генитальном инфантилизме, рецидивирующем кольпите. Больным с хроническим воспалением внутренних половых органов, протекающим на фоне генитального инфантилизма, целесообразно назначение тока надтональной частоты, диатермии.
Токи низкого напряжения находят применение в гинекологии в виде гальванизации и низкочастотной импульсной электротерапии. Гальванизация (лечебное использование постоянного тока) чаще всего является компонентом лекарственного электрофореза. В качестве самостоятельного метода лечения гальванизация показана при нейроэндокриннх гинекологическх синдромах и расстройствах менструальной функции, в этих случаях нередко проводят эндоназальную гальванизацию.
Импульсные токи низкой частоты (диадинамические, синусоидальные модулированные, флюктуирующие) являются действенным средством болеутоления при стойком болевом синдроме воспалительного генеза. Низкочастотные монополярные импульсные токи прямоугольной формы используют для проведения электросна и центральной электроанальгезии при нейроэндокринных гинекологических синдромах с целью купирования болей в послеоперационном периоде. Большое значение в гинекологии этот вид терапии получил для стимуляции рецепторов шейки матки. Вследствие возбуждения шеечно-гипоталамо-гипофизарного рефлекса восходящим путем достигается гемостаз при дисфункциональных маточных кровотечениях.
Аэроионы и гидроаэроионы, лечебное применение которых известно под названием аэро- и гидроаэроионотерапииф, используют для активации защитно-приспособительных механизмов женского организма с целью предоперационной подготовки, реже при климактерическом синдроме.
Сочетанная физиофармакотерапия:
Электрофорез – одновременное воздействие на организм гальванического или импульсного монополярного тока низкой частоты и лекарственного вещества, приобретающего повышенную реакционную способность вследствие введения в ткани в виде ионов. Ведущим компонентом такого воздействия является ток, под влиянием которого возникает выраженный и продолжительный терапевтический эффект при введении в организм очень небольшого количества медикамента. Электрофорез лекарственных веществ показан при воспалительных заболеваниях внутренних органов, как в подострой стадии, так и в период обострения процесса, при спаечных изменениях в малом тазу, нарушениях менструальной функции и другом. Применяют воздействия накожные (область молочных желез, передней брюшной стенки, крестцового ромба) и внутриполостные (влагалищные, эндоцервикальные, эндоназальные).
Выбор лекарственного вещества для электрофореза осуществляют дифференцированно. Наиболее широко проводят электрофорез биотических препаратов, которые являются важными факторами регуляции метаболических процессов в организме и активно влияют на его основные функции. Так, при электрофорезе ионы цинка оказывают фибролитическое действие и повышают вегетативных тонус органов малого таза; ионам йода присуще усиление диссимиляционных процессов, выраженное размягчающее влияние на спаечные структуры; ионы магния способствуют релаксации гладкомышечных волокон; ионы кальция усиливают ассимиляционные процессы, повышают проницаемость стенок сосудов. Широко используются болеутоляющие и противовоспалительные свойства ионов анальгина.
Лекарственный электрофорез является эффективным средством терапии эндокринных расстройств, поскольку ионы меди повышают продукцию эстрогенов, а ионы йода и цинка снижают ее и усиливают активность желтого тела. Влияние на продукцию эстрогенов и прогестерона осуществляется на уровне системы “гипоталамус-гипофиз”.
Фонофорез (ультрафонофорез) лекарственных веществ – одновременное воздействие на кожу, реже – на
слизистую оболочку влагалища УЗ колебаний и медикаментозного препарата, сохраняющего все специфические фармакологические свойства. Основной клинический эффект обусловлен действием УЗ, который повышает адсорбционные свойства кожи, усиливает терапевтическое воздействие лекарственного средства и позволяет в известной степени локализовать направленное действие его в зоне патологического очага (матка, придатки) или в непосредственной близости от него. Наиболее часто проводят фонофорез гидрокортизона, йодида калия, ихтиола, биологически активных веществ, содержащихся в лечебной грязи или нафталанской нефти. Основными показаниями к фонофорезу являются хронические воспалительные процессы в матке, придатках, тазовой брюшине и клетчатке, а также необходимость реабилитации больных после хирургического лечения, в первую очередь тубэктомии по поводу внематочной беременности.
Электроаэрозольтерапия.
За исключением аменореи и неотложных состояний, лечение физическими факторами следует начинать с 5-7-го дня менструального цикла. В другие сроки начало физиотерапии существенно увеличивает вероятность возникновения отрицательных ответных реакций как общего, так и местного характера. Для общей патологической реакции характерны ухудшение самочувствия, возникновение вегетативных эндокринно-сосудистых нарушений, а также клинических признаков активации инфекционного процесса в экстрагенитальных очагах. Местная (в зоне проведения процедур) патологическая реакция при воздействии на область головы и шеи проявляется симптомами транзиторного нарушения мозгового кровообращения. При брюшностеночно-крестцовых, влагалищных и ректальных процедурах возможны ациклические кровянистые выделения из половых путей, появление или усиление болей внизу живота и в крестце, обильные бели, дизурические явления. При воспалительных заболеваниях внутренних половых органов возникают или усиливаются боли, выявляется локальный экссудативный процесс, изменяются гематологические и биохимические показатели крови, свидетельствующие о прогрессировании воспаления. Поэтому при патологической общей или местной реакции на ФТЛ следует уменьшить интенсивность воздействия, а при усилении клинической симптоматики заболевания – заменить используемый лечебный фактор другим или вообще отменить ФТЛ.
Для получения оптимального лечебного эффекта от применения физических факторов целесообразно последовательное проведение серии физиотерапевтических процедур. Этим достигается продолжение вызванных физическим фактором метаболических изменений даже после прекращения его воздействия. Благодаря такому последействию отдаленные результаты лечения, как правило, бывают более выраженными, чем непосредственные. У гинекологических больных период последействия курса лечения преформированными физическими факторами составляет около 2 месяцев, минеральными ваннами и орошениями – около 4 месяцев, грязями – около 6 месяцев.
Лечебный массаж – эффективное средство улучшения кровообращения и лимфотока, активации окислительно-восстановительных процессов и тканевого дыхания, формирования более совершенных защитных и компенсаторных реакций.
При нейроэндокринных гинекологических синдромах, эмоционально-невротических расстройствах, обусловленных длительным течением воспалительных заболеваний и нарушений менструальной функции, целесообразен ручной массаж (классический, сегментарный, точечный и др.)
При генитальном инфантилизме и гипофункции яичников воспалительного генеза показан вибрационный массаж, проводимый с помощью специальных аппаратов.
Специфической разновидностью ручного массажа является гинекологический массаж, заключающийся в механическом воздействии на матку, придатки, брюшину и клетчатку малого таза. Гинекологический массаж показан при генитальном инфантилизме и спаечных процессах в малом тазу, обусловливающих возникновение неправильного положения матки.
Лечебная физкультура – метод лечения, использующий в качестве терапевтического фактора естественную функцию человека – движение – с целью общеукрепляющего воздействия и специально для восстановления нарушенной деятельности половой системы.
Из всех средств лечебной физкультуры в гинекологии наиболее часто назначают гимнастические упражнения, реже – прогулки и дозированную ходьбу (терренкур). Лечебная гимнастика включает наряду с дыхательными активные упражнения для мышц спины, корпуса, брюшного пресса, тазового дна и нижних конечностей. Этим достигают улучшения крово- и лимфообращения, в т.ч. в органах малого таза, стимуляции обменных процессов (общих и местных) в патологическом очаге, повышения тонуса организма и оптимизации психоэмоционального состояния больной.
Санаторно-курортное лечение показано при хронических воспалительных заболеваниях матки, придатков, тазовой брюшины и клетчатки, исключая генитальный туберкулез (в этом случае лечение должно проводиться в специализированных санаториях), послеоперационных спаечных процессах в малом тазу, фиксированных неправильных положениях матки, генитальном инфантилизме, нарушениях менструальной функции (после исключения обусловливающих их органических заболеваний, кроме хронического воспаления внутренних половых органов), климактерическом синдроме.
Недопустимо направление на санаторно-курортное лечение женщин с симптоматическим диагнозом ”бесплодие” без выявления причины отсутствия беременности, “аменоррея” – без установления происхождения ее. Максимальная эффективность курортной терапии в гинекологии отмечается при небольшой продолжительности пат. процесса.
Для решения вопроса о показаниях и установлении противопоказаний к санаторно-курортному лечению проводят мед. отбор больных обязательным участием терапевта. Кроме общих противопоказаний (злокачественные новообразования любой локализации, болезни крови, активные формы туберкулеза легких, органов брюшной полости и брюшины, сердечно-сосудистые заболевания в стадии декомпенсации), для гинекологических больных существуют специальные противопоказания. К ним относятся период после аборта (до первой менструации), состояние после операции по поводу злокачественного новообразования. Лечение на грязевых и бальнеологических курортах тепловыми процедурами противопоказано при наличии полипа, кровоточащей псевдоэрозии шейки матки, миоме матки, эндометриозе, кисте яичника, маточном кровотечении, дисфункции яичников, обусловленной органическими заболеваниями нервной и эндокринной системы.
После выявления показаний и исключения противопоказаний к санаторно-курортному лечению прежде всего необходимо правильно выбрать тип курорта. При отсутствии экстрагенитальных заболеваний выбор типа курорта определяется характером патологии половой системы.
Большое значение имеет выбор вида лечения – санаторного или амбулаторного. Затем необходимо определить наиболее благоприятный сезон (время года) для курортного лечения. При гинекологических заболеваниях курортное лечение может быть проведено в любое время года, однако желательно избежать направления на южные курорты в жаркие летние месяцы женщин с климактерическим синдромом и выраженными эмоционально-неврологическими расстройствами.
Большое внимание следует уделять подготовительным лечебным профилактическим мероприятиям: санации половых путей (лечение кольпита, удаление полипа, лечение псевдоэрозии шейки матки) и экстрагенитальных очагов хронической инфекции.
ПРИНЦИПЫ ГОРМОНАЛЬНОЙ ТЕРАПИИ В ГИЕНКОЛОГИИ. ПОНЯТИЕ О СТИМУЛИРУЮЩЕЙ И ЗАМЕСТИТЕЛЬНОЙ ДОЗЕ.
Гормональную терапию, показания к которой в гинекологии многообразны, условно подразделяют на заместительную, блокирующую, стимулирующую и поддерживающую.
Заместительная гормонотерапия применяется при гипофункции разного генеза. Различают циклическую гормонотерапию, которая основана на циклическом применении эстрогенных и гестагенных препаратов соответственно фазам менструального цикла. При выраженном половом инфантилизме и аменорее заместительная терапия может состоять из двух этапов. Первый этап – подготовительный. Он заключается в первоначальном введении только эстрогенных препаратов, с этой целью применяются различные эстрогенные препараты в течение 20 дней с 10-дневными перерывами. Проводят несколько курсов такого лечения до появления менструальноподобной реакции. Затем проводится второй этап заместительной терапии, состоящий из циклического применения эстрогенов (в течение 10-12 дней) и гестагенов (в течение 8 дней). При недостаточности функции желтого тела может применяться заместительная терапия только гестагенами, которые назначают за 8-10 дней до начала менструации.
Гормонотерапия, блокирующая функцию яичников, основана на подавлении циклических изменений в них путем воздействия на гипоталамо-гипофизарную систему. Для этого чаще всего используют комбинированные эстроген-гестагенные препараты (нон-овлон, бисекурин и др.), которые применяют с 5-го по 25-й день менструального цикла. Используют также ”чистые” гестагены (фуринал и др.), назначаемые в непрерывном режиме. Эти препараты применяют для лечения эндометриоза, миомы матки, гиперпластических процессов, предрака эндометрия и при другой патологии.
Стимулирующая гормонотерапия основана на прямой или опосредованной стимуляции функции яичников. Стимулирующий эффект вызывают препараты гонадотропных гормонов (пергонал, хориогонин), а также клонифен (клостильбегид). Применение стимулирующей терапии требует большой осторожности, т.к. при длительном и бесконтрольном ее проведении возможно возникновение синдрома гиперстимуляции яичников, который проявляется болями в животе, увеличением размеров яичников вплоть до апоплексии и даже некроза.
Поддерживающая терапия основана на применении небольших доз половых гормонов с целью нормализации вегетативно-сосудистых и эмоционально-психических расстройств, возникших в результате снижения функции яичников, но не нормализации репродуктивной. Поддерживающая терапия показана в основном при климактерическом синдроме и при синдроме истощения яичников.
ЛАПАРОСКОПИЯ И КОЛЬПОСКОПИЯ. ПОКАЗАНИЯ, УСЛОВИЯ ВЫПОЛНЕНИЯ, ДИАГНОСТИЧЕСКАЯ ЦЕННОСТЬ.
См. вопр. №3, пункт III. 17
ПРИЧИНЫ ЖЕНСКОГО И МУЖСКОГО БЕСПЛОДИЯ. СИСТЕМА И МЕТОДЫ ОБСЛЕДОВАНИЯ ПРИ БЕСПЛОДНОМ БРАКЕ.
Бесплодие – неспособность лиц детородного возраста к воспроизводству потомства вследствие нарушения оплодотворения или имплантации оплодотворенной яйцеклетки.
Брак считается бесплодным, если беременность у женщины не наступает в течение года регулярной половой жизни (половые сношения не реже 1 раза в неделю) без использования средств и методов контрацепции.
Причиной бесплодия могут быть нарушения репродуктивной системы у одного или обоих супругов.
Диагноз бесплодия у женщины может быть установлен только после исключения бесплодия мужчины при положительных пробах, подтверждающих совместимость спермы и слизи шейки матки.
Обследование бесплодных супругов проводят одновременно.
Обследование мужчины – проводят у специалистов по мужскому бесплодию. Обязательным условием обследования является анализ спермы мужчины посткоитальный тест:
1. Исследование спермы:
Количество сперматозоидов – 20 к 106/мл
Подвижность – больше 25%, активно подвижных сперматозоидов с поступательным движением через 60 мин с момента получения эякулята
Морфология – больше 50% нормальных форм
Агглютинация
Объем эякулята – больше 2 мл (2-5 мл)
Вязкость – нормальная
рН 7,2-7,8
лейкоциты меньше 1,0*106/мл
Патологические изменения при исследовании фертильной спермы:
астеноспермия – недостаточное количество активно подвижных сперматозоидов
некроспермия – отсутствие живых сперматозоидов
тератоспермия – большое количество патологических форм сперматозоидов
олигоспермия – недостаточное количество сперматозоидов в эякуляте
азооспермия – отсутствие сперматозоидов при наличии клеток сперматогенеза
аспермия – отсутствие клеток сперматогенеза
Азооспермия и аспермия – глубоко патологические состояния, обычно связанные либо с непроходимостью семявыносящих путей, либо с атрофией канальцев яичек.
2. Посткоитальный тест (проба Шуварского-Симса-Хунера) – определение числа подвижных сперматозоидов в шеечной слизи через 2,5-3 ч после полового сношения за 1-2 дня до овуляции после 3-дневного воздержания. Оценка результатов:
отрицательный – сперматозоидов нет
слабоположительный – 2-6 сперматозоидов в поле зрения
положительный – более 7 сперматозоидов в поле зрения
При отрицательном посткоитальном тесте необходимы дополнительные исследования для заключения иммунологической причины бесплодия – образование антиспермальных антител в шейке матки.
Обследование женщины.
Анамнез:
Число и исход предыдущих беременностей и родов, послеобортные и послеродовые осложнения, число живых детей
Продолжительность бесплодия
Методы контрацепции, продолжительность их применения
Заболевания (диабет, туберкулез, заболевания щитовидной железы, надпочечников и др.)
Медикаментозная терапия (применение цитостатических, психофармакологических препаратов, транквилизаторов)
Операции, способствующие возникновению бесплодия (аппендэктомия, операции на яичниках, трубах, матке, кишечнике, мочевыводящих путях, почке)
Воспалительные процессы в органах малого таза и ЗППП, тип возбудителя, продолжительность и характер терапии
Заболевания шейки матки, их характер, лечение (консервативная, крио- или лазеротерапия, электрокоагуляция)
Наличие выделений из сосков молочных желез, связь их с лактацией
Эпидемические, производственные факторы, вредные привычки (курение, алкоголизм, наркомания)
Наследственные заболевания у родственников 1-ой и 2-ой степени родства
Менструальный анамнез, возраст менархе, характер цикла, характер нарушений цикла, наличие межменструальных выделений, болезненность менструации
Половая функция, боль при половом акте (диспареуния поверхностная или глубокая)
Объективное исследование
Рост, масса тела, ИМТ (отношение массы тела в кг к квадрату роста в м); при наличии ожирения – его тип, когда отмечена прибавка массы тела (после замужества, родов, аборта, в пубертатном периоде) и ее характер (медленное или быстрое нарастание массы тела)
Наличие галактореи, степень развития молочных желез: характер оволосения, наличие гипертрихоза и его степень, состояние кожи (сухая, влажная, жирная, наличие угревой сыпи, полос растяжения, их количество и цвет)
Рентгенография черепа и турецкого седла
Исследование глазного дна и полей зрения (цветовых)
Гинекологическое бимануальное исследование и осмотр шейки матки в зеркалах при показаниях – кольпоскопия
Специальные методы исследования
Тесты функциональной диагностики в течение 2-3 циклов
Гормональные исследования: определение эстрадиола, прогестерона, лютеитнизирующего и фолликулостимулирующего гонадотропина, пролактина, тестостерона, дегидроэпиандростерона в крови на 2-5-ыи и 20-22-ои дни цикла (при невозможности провести исследование содержания гормонов в крови можно ограничиться проведением тестов функциональной диагностики и определением 17-кетостероидов и прегиандиона в моче на 20-22-ой день цикла)
Гистеросальпингография на 6-7-ой день цикла
Пертубация (кинопертубация) в дни овуляции
УЗ-исследование – динамическое измерение диаметра фолликулов на 8-11-ый день цикла
Лапароскопия на 18-24-ый день менструального цикла
Биопсия эндометрия за 2-3 дня до начала менструации (при показаниях сочетать с гистероскопией).
Установление причин бесплодия часто бывает сложным процессом, требующим от врача много времени (в среднем 5-6 месяцев, а иногда и года). Обследование супружеской пары состоит из нескольких этапов:
I этап – изучение анамнеза мужа и жены, проведение общеклинического исследования, после чего ставится предварительный диагноз
II этап – учитывая, что наиболее часто встречается трубное и мужское бесплодие, следует исключить или подтвердить указанные факторы. Для этой цели проводят ми кроскопическое исследование спермы мужа. Исключив мужское бесплодие, определяют проходимость маточных труб.
III этап – тщательное обследование больной для диагностики наличия овуляции и определения совместимости цервикальной слизи и спермы (тесты функциональной диагностики, экскреция прегнандиола с мочой, содержание прогестерона в крови, биопсия эндометрия, посткоитальный тест)
IV этап – включает специальные методы, которые проводятся в зависимости от ранее полученных данных. При установлении нарушений овуляции предпринимаются гормональные исследования с определение экскреции и мочой эстрагенов, 17-кетостероидов. Проводятся различные функциональные пробы с введением гормонов. Очень ценными диагностическими тестами являются определение в крови уровня фолликулостимулирующего гонадотропина, пролактина, эстрагенов и прогестерона. При обследовании мужчины в трудных для диагностики случаях определяется его гормональный статус, иногда проводится биопсия яичка, вазография. При подозрении на наследственную патологию предпринимается медикогенетическое исследование.
ФОРМЫ ЖЕНСКОГО БЕСПЛОДИЯ, ИХ ДИАГНОСТИКА, ЛЕЧЕНИЕ, ПРОФИЛАКТИКА.
У женщины различают:
Абсолютное бесплодие – если имеются причины, полностью исключающие возможность зачатия (отсутствие матки и яичников)
Относительное бесплодие – если причина, вызывающая бесплодие может быть устранена.
Первичное бесплодие – при отсутствии в анамнезе беременности при наличии регулярное половой жизни в течение 1-2 лет.
Вторичное бесплодие – при наличии в анамнезе беременности.
К числу важнейших причин женского бесплодия относятся:
Воспалительные заболевания половых органов.
Заболевания желез внутренней секреции.
Недоразвитие (инфантилизм и гипоплазия) половых органов.
Неправильное положение половых органов.
Эндометриоз матки, труб, яичников.
Опухоли половых органов.
Экстрагенитальные заболевания (ревматизм, нефрит, туберкулез, аллергия).
Неполноценное в количественном и качественном отношении питание.
Иммунологические факторы.
Принято различать следующие основные формы бесплодия женщин (по этиологии):
1.Эндокринное бесплодие – бесплодие, обусловленное нарушением овуляции
а) ановуляция.
Хроническая ановуляция может быть следствием нарушения функции гипоталамо-гипофизарной системы (нарушение ритма и количества выделения гонадолиберинов и гонадотропных гормонов гипофиза), развившегося вследствие нейроинфекции, интоксикации, психоэмоционального стресса, церебральной травмы и др. Ановуляция является также симптомом эндокринных заболеваний, а именно поликистоза яичников, дисфункции коры надпочечников, гиперпролактинемии, послеродового ожирения, гипо- и гипертиреоза, болезни Иценко-Кушинг, нервных и психических заболеваний.
Проявлениями хронической ановуляции, помимо бесплодия, могут быть также нарушения менструального цикла – дисфункциональные маточные кровотечения, аменорея, олигоменорея.
Диагноз ановуляции основан на данных тестов функциональной диагностики: монофазная базальная темпертура, монотонный кариопикнотический индекс (как правило, колеблющийся в пределах, характерных для начала первой фазы цикла), отсутствие симптома “зрачка” натяжения шеечной слизи 2-5 см. С диагностической целью применяют лапароскопию, при которой оценивают внешний вид яичников, отсутствие овуляторной стигмы и овуляторных тел, выявляют неэндокринные причины бесплодия – спаечный процесс, наличие эндометриоидных эктопий в малом тазу. Дополнительная хромопертубация – введение красящего вещества (индигокармин, ме6тиленовый синий) через наружный маточный зев – позволяет установить непроходимость маточных труб или локализацию их непроходимости.
б) Лютеинизация неовулировавшего фолликула.
Предполагают, что в возникновении этой патологии определенную роль играет стресс, гиперпролактинемия и воспаление яичников. Диагноз весьма затруднителен, т.к. тесты функциональной диагностики и содержание гормонов в крови и моче не отличаются от таковых в течение овуляторного цикла. При УЗ-исследовании и измерении диаметра фолликулов отмечают медленное постепенно уменьшение размеров преовуляторного фолликула (тогда как для овуляции характерно исчезновение доминантного фолликула). При лапароскопии, выполненной на 13-15 день цикла, выявляют геморрагическое желтое тело без овуляторной стигмы.
в) Недостаточность лютеиновой фазы цикла (гипофункция желтого тела) сопровождается уменьшением синтеза прогестерона. Причиной бесплодия при недостаточности лютеиновой фазы цикла могут быть: неполноценные секреторные превращения эндометрия, препятствующие имплантации оплодотворенной яйцеклетки; снижение перистальтической активности маточных труб вследствие дефицита прогестерона.
Недостаточность лютеиновой фазы цикла может наблюдаться как физиологическое явление после менархе, родов, аборта в течение нескольких менструальных циклов. Причинами недостаточности лютеиновой фазы цикла могут быть гиперандрогения надпочечникового происхождения, гиперпролактинемия, воспалительные заболевания матки и придатков, гипотиреоз. Помимо бесплодия, при недостаточности лютеиновой фазы цикла отмечаются скудные кровянистые выделения на 4-7 день до менструации.
Диагноз недостаточности лютеиновой фазы цикла устанавливается на основании укорочения гипертермической фазы базальной температуры до 4-8 дней при разнице температуры в первой и второй фазе цикла менее 0,4 гр. Цельсия; снижение содержания пергнандиола в моче ниже 3 мг/сут, прогестерона в крови ниже 15 нмоль/л на 4-ый день повышения базальной температуры; неполноценной фазы секреции в эндометрии за 2-3 дня до менструации.
Все многочисленные варианты эндокринных расстройств, ведущие к нарушению овуляции, могут быть условно объединены в отдельные клинические группы, для которых характерен соответствующий симптомокомплекс:
Первая группа – гипоталамо-гипофизарная недостаточность (патологические состояния, определяемые как генитальное недоразвитие);
Вторая группа – гипоталамо-гипофизарная дисфункция (больные с расстройствами менструального цикла);
Третья группа – яичниковая недостаточность;
Четвертая группа – врожденные или приобретенные нарушения половой системы;
Пятая группа – гиперпролактинемия при наличии опухоли с гипоталамо-гипофизарной области;
Шестая группа – гиперпролактинемия без поражения гипоталамо-гипофизарной области;
Седьмая группа – аменорея на фоне опухоли в гипоталамо-гипофизарной области.
Лечение эндокринного бесплодия проводят женщинам до 35 лет при отсутствии у них соматических заболеваний, являющихся противопоказанием к беременности и родам. При наличии эндокринных заболеваний необходима терапия указанной патологии.
Распространенным методом лечения ановуляции является стимуляция овуляции. Применяются следующие схемы введения препаратов:
Кломифен (кломифеницитрат, клостильберид) – по 50-150 мг с 5 по9 день от начала менструации или от начала менструальной реакции, индуцированной лекарственными препаратами. С этой целью применяют оральные контрацептивы типа нон-овлона, бисекурила и др. по 1 таб. в течение 7-10 дней.
Кломифен в той же дозе и в те же сроки в сочетании с хорионическим гонадотропином, который вводят после достижения доминантным фолликулом преовуляторных размеров (не менее 18 мм в диаметре) в дозе 4500-300 ЕД;
Можно использоват тамоксифен (зитозониум), обладающий антиэстрогенной активностью. Препарат назначают с 5 по 9 день цикла в дозе 10-20 мг в день.
Пергонал (человеческий менопаузальный гонадотропин) с 5 дня индуцированной менструальной реакции в дозе 150 ЕД ежедневно под контролем УЗ-измерения диаметра фолликула.
Можно использовать синтетические аналоги гонадотропных рилизинг-гормонов гипоталамуса, стимулирующего выделение лютеинизирующего гонадотропина гипофизом и опосредованно овуляцию в яичнике. Препарат вводят в/в с часовым интервалом, в т.н. пульсирующем режиме, имитирующем выделение гонадолиберина гипоталамусом.
При бесплодии, вызванном недостаточностью лютеиновой фазы цикла, проводят патогенетическое лечение заболеваний, вызвавших это нарушение функции яичников. Проводят также гормональную терапию заместительного характера препаратами желтого тела или норстероидами, обладающими гестагенным действием. Используют прогестерон по 1 мг 1% р-ра в/м с 18-20 дня цикла в течение 8-6 дней;17-оксипрогестерона капронат по 1 мг 12,5% р-ра на 17 или 20 день цикла; норколут, который назначают с 16 по 26 день цикла в дозе 5 мг в день. Рекомендуется применение хорионического гонадотропина, стимулирующего гормональную секрецию желтого тела (по 1000-1500 ЕД в/м на 2,4,6 день повышения базальной температуры). Длительнсть терапии 3-4 менструальных цикла.
При бесплодии, обусловленной нелютеинизацией неовулировавшего фолликула, рекомендуется стимуляция овуляции.
Необходимо помнить, что при неправильном подборе дозы препаратов, стимулирующих овуляцию, может возникнуть осложнение – синдром гиперстимуляции яичников.
Прогноз в отношении восстановления репродуктивной функции при правильном определении причины эндокринного бесплодия и своевременном проведении адекватной терапии благоприятный. При наличии у женщины заболеваний или нарушений функции эндокринных желез лечение необходимо начинать с терапии указанных эндокринных заболеваний. Обычно нормализация функций эндокринных желез приводит к восстановлению овуляторно-менструаьного цикла. Только при продолжающейся ановуляции или недостаточности лютеиновой фазы цикла рекомендуется стимуляция овуляции и терапия, о которой говорилось выше.
В случаях, когда бесплодие связано с нарушеним функции гипоталамо-гипофизарной системы, терапия малоэффективна.
При наступлении беременности после проведения лечения необходимо наблюдение за женщиной с ранних сроков. Поскольку эти беременные составляют группу высокого риска по вынашиванию беременности в первом триместре беременности.
II. Трубное и трубно-перитонеальное бесплодие.
К этой форме бесплодия относят:
1. функциональную патологию маточных труб, которая характеризуется нарушением их сократительной активности (дискоординация, гипо- и гипертонус). Причиной этого принято считать психоэмоциональную неустойчивость, гипофункцию яичников, гиперандрогению, гипер- или гипопростагландинемию.
2. органическую патологию маточных труб, которая включает нарушение проходимости, спаечный процесс, возникшее как правило, после воспалительных процессов в органах малого таза или после оперативных вмешательств на матке, придатках, кишечнике, как осложнение абортов или родов.
Диагноз трубного бесплодия устанавливают на основании данных анамнеза и специального обследования. Применяют пертубацию или кимопертубацию в дни, соответствующие овуляции, с целью уточнения функционального состояния труб; гистеросальпингографию с водорастворимыми контрастными веществами на 6-7 день цикла, т.к. во вторую фазу цикла эндометрий, подвергающийся секреторным изменениям, может препятствовать проникновению контрастного вещества в маточные трубы. Наиболее информативным методом исследования является лапароскопия с одновременной хромопертубацией.
При наличии в малом тазу спаечного процесс его оценивают следующим образом: 1-ая степень – единичные тонкие спайки; 2-ая степень – спайки плотные, от спаек свободно более 50% яичника; 3-я степень – спайки множественные и плотные, свободно менее 50% яичника; 4-ая степень – поверхность яичника не видна, спайки плотные, пластинчатые.
При лечении функционального трубного бесплодия, причиной которого являются психоэмоциональные нарушения, применяют седативные средства, психотерапию, спазмолитики, блокаторы синтеза простагландинов (индометацин и др.) – в предовуляторном периоде, рекомендуется применение УЗ в импульсном режиме на область придатков. В течение менструального цикла проводят 10-12 процедур электростимуяции с целью восстановления функциональной активности маточных труб. Обычно лечение продолжают в течение двух менструальных циклов. Усилению функции маточных труб способствует также проведение гинекологического массажа, сероводородные и мышьяковистые ванны.
Лечение трубного бесплодия воспалительного генеза должно начинаться с ликвидации явлений воспаления в зависимости от стадии процесса. Наряду с антибактериальной терапией необходимо применять физические методы лечения, десенсибилизируюшие средства и адаптогены. При наличии явлении экссудации во время острой или подострой стадии заболевания вместе с антибиотиками целесообразно применение адаптогенов и физических факторов (магнитное поле, электрофорез цинка, ИК-лазер). При хроническом рецидивирующем воспалительном процессе лечение следует начинать с применения препаратов типа продиозана или пирогенала с последующим добавлением антибактериальных средств широкого спектра действия, десенсибилизирующих средств, физиотерапии и спазмолитиков.
Следующим этапом лечения с минимальным интервалом должно быть грязелечение и бальнеотерапия. После окончания противовоспалительной терапии женщинам с непроходимыми маточными трубами или при затрудненной их проходимости можно применять гидротубацию (не более 2 курсов, т.к. при большом количестве гидротубации травмируется эпителий маточных труб, который в дальнейшем не регенерирует).
Лечебные гидротубации не показаны при хронических рецидивирующих воспалительных заболеваниях придатков длительностью более 2 лет. В связи с этим показано своевременное оперативное лечение трубного и трубно-перитонеального бесплодия, объем и характер которого устанавливают при лапароскопии.
Абсолютным противопоказанием к оперативному лечению является туберкулез половых органов, относительным противопоказанием считается возраст старше 35 лет, длительность трубного бесплодия более 5 лет, частые обострения воспалительного процесса в придатках матки, острый воспалительный процесс, перенесенный в течение предшествующего года, резко выраженный спаечный процесс в малом тазу (IV степень).
При операции на маточных трубах используют хирургическую технику. Основные виды хирургических вмешательств:
фимбриолизис – освобождение фимбрий трубы из сращений;
сальпинголизис – резделение сращений вокруг труб, ликвидация перегибов и искривлений;
сальпингостоматорафия – создание нового отверстия в трубе с запаянным ампулярным концом;
сальпинго-сальпингоанастомоз – резекция части трубы с последующим соединением концов;
пересадка трубы в матку при непроходимости в интерстициальных отделах.
В послеоперационном периоде показана рассасывающая терапия, электрофорез цинка и меди, магнитотерапи, ультразвук, рекомендуются также ранние гидротубации без применения глюкокортикоидных препаратов, способствующих образованию спаек.
В течение 4 месяцев после операции назначают контрацепцию с применением оральных гормональных контрацептивов (ригевидон, тривистон и др.)
При невозможности осуществления оперативного лечения консервативное проводят лишь при I степени распространения спаек и начинают его с УЗ терапии и желательно в импульсном режиме. В последующем показано грязелечение и гинекологический массаж.
Профилактика трубного и трубно-перитонеального бесплодия включает предупреждение и рациональное лечение воспалительных заболеваний половых органов, проведение реабилитационных мероприятий в ранние сроки после гинекологических операций у молодых женщин, своевременную диагностику и лечение аппендицита.
III. Бесплодие при гинекологических заболеваниях без нарушения овуляции:
Эндометриоз, диагноз которого устанавливают на основании анамнеза, наличия альгоменорреи. Решающая роль в диагностике принадлежит лапароскопии в предменструальном периоде, когда эндометриоидные гетеротопии отчетливо видны на брюшине органов малого таза и поверхности яичников.
Внутриматочные синехии – образуются после травматичных выскабливаний по поводу абортов, маточных кровотечений, грубого отделения плаценты. Синехии представляют собой бессосудистые тяжи в полости матки, идущие между ее стенками, чаще в области дна и деформирующие полость матки. Клиническими проявлениями этой патологии, называемой синдромом Ашермана, являются аменорея или гипоменорея в сочетании с овуляторным бесплодием.
На основании гистероскопической картины выделяют следующие формы внутриматочных синехий:
Легкая форма – синехии тонкие, нитеобразные, занимают менее четрерти полости матки, трубные углы свободные или облитерированы;
Форма средней тяжести – синехии занимают более четверти полости матки, частично облитерировано, трубные углы облиерированы;
Тяжелая форма – синехии занимают более четверти полости матки, дно матки облитерировано, трубные углы облитериованы.
Причиной внутриматочных синехий может быть также туберкулезное поражение эндометрия.
Диагноз устанавливается на основании типичного анамнеза. Решающее значение в диагностике имеет гистероскопия, при которой определяется степень распространенности процесса.
Лечение: разделение спаек острым путем под контролем гистероскопии и введение специального протектора, представляющего собой полиэтиленовый каркас с катетером. Через катетер в течение недели вводят смесь, содержащую 64 ЕД лидазы, 0,1% р-р эстрадиола дипропионата и 125 мг суспензии гидрокортизона ацетата. Каркас удаляют на 7-8-й день и в полость матки вводят петлю Липса сроком на 2 года. В течение 6 месяцев после разделения спаек рекомендуется циклическая гормонотерапия.
Прогноз для восстановления менструальной функции благоприятный, для репродуктивной – менее обнадеживающий. Наступившая беременность часто осложняется невынашиванием, а роды – плотным прикреплением плаценты.
Патология шейки матки.
Шейка матки – первое существенное препятствие на пути сперматозоидов. Обычно сперматозоиды быстро проходят через цервикальный канал, однако при ряде патологических состояний он становится непреодолимой преградой для мужских половых клеток.
К этим патологическим состояниям относятся:
Аномальное положение шейки (при выпадении или смещении матки кзади);
Хронический воспалительный процесс в шейке матки, при котором образуется слизь, препятствующая продвижению сперматозоидов (например, при инфицировании видами Streptococcus, Staphylococcus, Gardnerella)
Колонизация шейки матки м/о, цитотоксичными по отношению к сперматозоидам (например, Ureoplasma)
Предшествующее хирургическое вмешательство на шейке матки (например, конизация), способное привести к уменьшению количества шеечной слизи
Предшествующее прижигание каких-либо образований на шейке матки с помощью лазерной или электроаппаратуры, повлекшее за собой сужение цервикального канала
Наличие в цервикальной слизи антител к сперматозоидам.
При подозрении на бесплодие, связанное с патологией шейки матки, исследуют цервикальную слизь:
Определение рН слизи (в норме 8,0)
Бактериологический посев
Определение характера слизи в середине цикла, степени ее кристаллизации и вязкости
Серологические тесты на антитела
Проведение посткоитальной пробы
Анализ поведения сперматозоидов в цервикальной слизи – исследование слизи после искусственного помещения в нее спермы партнера, микроскопическая оценка in vitro (поведение сперматозоидов в шеечной слизи донора сравнивают с поведением сперматозоидов в слизи пациентки, а поведение сперматозоидов партнера сравнивают с поведением донорских сперматозоидов в шеечной слизи пациентки).
Лечение:
Лечение малыми дозами эстрогенов
Антибиотикотерапия
Кортикостероиды для предотвращения возможного образования антител против сперматозоидов
Гонадотропины
Хирургическая коррекция деформации шейки матки
Искусственное внутришеечное или внутриматочное осеменение
Экстракорпоральное оплодотворение и имплантация концептуса.
Бесплодие, обусловленное иммунологическими факторами.
Причиной этой формы бесплодия является образование антиспермальных Ат. Известно 2 вида Ат:
Ат, образующиеся в семенной плазме к сперматозоидам, что приводит к аутоагглютинации сперматозоидов
Ат, образующиеся в слизистой оболочке цервикального канала и вызывающие полную иммобилизацию сперматозоидов.
при лекарственной терапии иммунологического бесплодия применяют глюкокортикоидные препараты, обладающие иммунодепрессивными свойствами.
искусственное осеменение, внутриматочное введение спермы.
ЭКО и транспорт эмбриона
Психогенное бесплодие.
У женщин с эмоционально-неустойчивой психической сферой конфликтные ситуации в семье, на работе, неудовлетворенность половой жизнью, а также настойчивое желание иметь ребенка или, наоборот, боязнь беременности могут вызвать нарушение овуляции.
Для лечения используют психотерапевтические методы, суггестивную терапию, по совету психоневролога могут быть рекомендованы транквилизаторы, седативные препараты.
Бесплодие неясного генеза.
При этом виде бесплодия в результате тщательного обследования супругов выяснить причину бесплодия не удается.
ШЕЕЧНЫЙ ФАКТОР ЖЕНСКОГО БЕСПЛОДИЯ: ЭТИОЛОГИЯ, ДИАГНОСТИКА, ТЕРАПИЯ.
См. вопр. 13, пункт III, 3.
ЭКСТРАКОРПОРАЛЬНОЕ ОПЛОДОТВОРЕНИЕ (ЭКО) В ТЕРАПИИ БЕСПЛОДНОГО БРАКА.
ЭКО и трансплантация эмбриона – оплодотворение яйцеклетки (ооцитов) вне организма и пересадка дробящихся эмбрионов в полость матки.
Показания для ЭКО:
Абсолютное трубное бесплодие (состояние после двусторонней тубэктомия)
Непроходимость или затрудненная проходимость обеих маточных труб при отсутствии эффекта от ранее проведенного оперативного или длительного (более 5 лет) консервативного лечения.
Бесплодие неясного генеза после проведенного полного клинического обследования, включая гормональное, эндоскопическое, иммунологическое.
Субфертильность спермы мужа при отсутствии эффекта при проведении гомологического осеменения.
Условия проведения ЭКО:
Сохраненная в полном объеме функциональная способность матки к имплантации и вынашиванию беременности.
Отсутствие противопоказаний к беременности и родам (соматические, психические, генетические заболевания).
Сохраненная способность яичников к адекватному ответу на стимуляцию овуляции – экзогенную или эндогенную
Отсутствие новообразований, воспалительных и анатомических изменений в органах малого таза.
При отсутствии этих условий, а также женщинам старше 40 лет ЭКО и трансплантация эмбриона противопоказаны.
Последовательность проведения метода:
Стимуляция суперовуляции
Аспирация ооцитов
Оплодотворение ооцитов
Культивирование оплодотворенных ооцитов
Перенос дробящихся эмбрионов в матку.
Успех ЭКО в значительной мере зависит от числа полученных при пункции преовуляторного фолликула яйцеклеток и от числа перенесенных в матку эмбрионов. Этот феномен получил название “функции помощи”. В связи с этим обязательно проводят стимуляцию суперовуляции, которая достигается комбинированным введение антиэстрогенов (кломифен) и гонадотропино (пергонал, хорионический гонадотропин). Применяют следующие схемы суперовуляции:
кломифен – 50-150 мг в день со 2 или 3 дня цикла в течение 5 дней; пергонал по 75-150 ЕД в/м на 3,5,7 дни цикла и далее ежедневно до достижения доминантным фолликулом диаметра 16-18 мм
пергонал по 75-150 ЕД со 2 дня цикла ежедневно до достижения доминантным фолликулом диаметра 16-18 мм
Через 24-48 ч после достижения фолликулом указанных размеров вводят в/м 5-10 тыс. ЕД хорионического гонадотропина.
Применение указанных схем приводит к образованию до 20 фолликулов, из которых может быть получено до 60 яйцеклеток. В течение всего этого времени женщина находится под постоянным динамическим контролем: проводят ежедневное УЗ исследование с измерением диаметра фолликулов, определением эстрадиола и лютеинизирующего гонедотропина в крови.
Пункцию фолликулов проводят через 24-36 ч после введения хорионического гонадотропина. Пункцию можно осуществлять трансабдоминальным путем или через влагалище под контролем УЗ датчиков. Трансвагинальный путь значительно облегчает визуализацию фолликулов и снижает частоту нежелательных осложнений (ранения органов малого таза и крупных органов). Кроме того, этот путь дает возможность аспирировать ооциты даже при пораженных спаечным процессом придатках.
Сперму мужа промывают, центрифугируют для отделения от семенной плазмы. Затем сперматозоиды переносят в специальный термостат, где уже находятся яйцеклетки. При осеменении на 1 яйцеклетку добавляют 200-300 тыс. сперматозоидов.
Процесс культивирования дробящихся яйцеклеток происходит в специальной среде с абсолютной влажностью, при 37°С и 5% содержании углекислого газа, обеспечивающем оптимальный уровень рН, в течение 2 сут.
На стадии 4-х и более бластомер дробящиеся эмбрионы помещают в специальный пластиковых катетер и через шейку матки переносят в полость матки (на ее дно) в минимальном объеме (0,05 мл) питательной среды.
Для контроля ранних сроков развивающейся беременности проводят динамическое определение β-субъединицы хорионического гонадотропина, которое помогает определить беременность с 7-9-го дня после трансплантации эмбриона. При наступлении беременности за женщинами ведется постоянное наблюдение методами, принятыми для ведения беременности и родов женщин с отягощенным акушерских анамнезом.
ОРГАНИЗАЦИОННЫЕ МЕРОПРИЯТИЯ ПО ПРОБЛЕМЕ БЕСПЛОДНОГО БРАКА.
Обследование супружеской пары
Лечение
При отсутствии эффекта от проводимого лечения и наличии условий проводят искусственное осеменение или ЭКО с трансплантацией эмбриона.
(см. вопр. II № 12-15).
НЕЙРОЭНДОКРИННЫЕ СИНДРОМЫ: ПРЕДМЕНСТРУАЛЬНЫЙ (ПМС), КЛИМАКТЕРИЧЕСКИЙ, ПОСТКАСТРАЦИОННЫЙ.
ПРЕДМЕНСТРУАЛЬНЫЙ СИНДРОМ – сложный пат. симптомокомплекс, возникащий в предменструальные дни и проявляющийся в нервно-психических, вегето-сосудистых и обменно-эндокринных нарушениях. Обычно симптомокомплекс ПМС проявляются за 2-10 дней до начала менструации и проходит сразу после ее начала или в первые дни.
Частота ПМС увеличивается с возрастом.
Ведущую роль в патогенезе ПМС отводят гиперэстрогенемии (относительной при дефиците прогестерона или абсолютной) и обусловленной ею задержке Na и жидкости в тканях организма, прежде всего в ЦНС. Гиперпролактинемия и гиперпростагландинемия также способствуют задержке жидкости в организме. Отмечают возможную роль эндорфина в развитии гиперпролактинемии и гиперпростагландинемии.
Таким образом, ПМС – отражение дисфункции различных отделов ЦНС, возникающей в результате воздействия неблагоприятных факторов у женщин с врожденной либо приобретенной неполноценностью гопоталамо-гипофизарной системы. Возникновение различных форм ПМС объясняется вовлечением в пат. процесс различных структур гипоталамуса и лимбико-ретикулярного комплекса, а также различным характером нарушения биохимических процессов в этих областях.
Часто начало ПМС связано со стрессовыми ситуациями.
Существует гипотеза о первичности нейрогормональных нарушений на уровне гипоталамуса, что позволяет отнести ПМС к диэцефальной патологии – гипоталамическому синдрому.
У больных ПМС в репродуктивном возрасте установлена гипофункция желтого тела и соответственно снижение секреции прогестерона во второй фазе цикла, что способствует возникновению абсолютной либо относительной гиперэстрогении; отмечено также повышение гистамина и серотонина во второй фазе менструального цикла, повышение секреции АКТГ.
У больных ПМС в переходном возрасте установлено повышение уровня эстрадиола, пролактина, альдостерона и АКТГ во вторую фазу цикла.
По клинической картине выделяют следующие формы ПМС:
легкую форму-появление 3-4 симптомов за 2-10 дней до начала менструации при значительной выраженности 1-2 симптомов заболевания;
тяжелую форму - проявления 5-12 симптомов за 3-14 дней до менструации, причем 2-5 симптомов или все резко выражены.
Выделяют 3 стадии ПМС:
Компенсированную стадию - симптомы болезни с годами не прогрессируют, появляются во второй фазе цикла и с наступлением менструации прекращаются;
Субкомпенсированную стадию - тяжесть заболевания усугубляется с годами, симптомы проходят только с прекращением менструации;
Декомпенсированную стадию - симптомы заболевания продолжаются в течение нескольких дней после прекращения менструации, а «светлые» промежутки постепенно сокращаются.
Выделяют следующие клинические формы предменструального синдрома:
нервно-психическую форму - характеризуется раздражительностью, слабостью, плаксивостью, агрессивностью, повышенной чувствительностью к звукам и запахам, нагрубанием молочных желез. У молодых женщин преобладают депрессия, в переходном возрасте - агрессивность;
отечную форму - характеризуется нагрубанием и болезненностью молочных желез, отечностью лица, голеней, пальцев рук вздутием живота, раздражительностью, слабостью, потливостью, зудом кожи, во вторую фазу цикла отрицательным диурезом (задержкой жидкости до 500-700 мл);
цефалгическую форму - характеризуется мигренеподобной головной болью, раздражительностью, тошнотой и рвотой, чувствительностью к звукам и запахам, головокружением, депрессией, болью в области сердца, потливостью, онемением рук, нагрубанием молочных желез, отеками (диурез при этом положительный и артериальное давление нормальное);
кризовую форму - развивается на фоне нелеченых вышеуказанных форм. В генезе кризовых состояний при ПМС важную роль играют гиперэстрогения, дисфункция дофаминергических структур гипоталамической области. Кризы начинаются после стрессовых ситуации и носят типичный характер симпатоадреналового криза (подъем артериального давления, тахикардия, потливость, чувство страха и так далее);
атипичную форму - протекает как гипертермическая и офтальмоплегическая форма мигрени, циклические аллергические реакции вплоть до отека Квинке, циклический язвенный гингивит и стоматит, циклическая «бронхиальная астма», циклическая рвота.
Основной диагноза является циклический характер патологических симптомов. Для исключения органической патологии с учетом преобладания тех или иных симптомов следует проводить рентгенографию черепа и турецкого седла, шейного отдела позвоночника, исследование почек и желудочно-кишечного тракта, электроэнцефалографию, электрокардиографию с функциональными пробами, определение состояния глазного дна и периферических полей зрения и другое.
При ПМС в предменструальные дни ухудшается течение большинства имеющихся хронических заболеваний.
Лечение:
Психотерапия, включающая доверительную беседу с пациенткой и объяснение сущности заболевания, аутотренинг, совет о режиме труда и отдыха;
Соблюдение диеты, особенно во вторую фазу цикла, с ограничением кофе, чая, поваренной соли, жидкости, животных жиров, молока;
Массаж (общий, воротниковой зоны);
Бальнеотерапия;
Эндоназальный электрофорез витамина BI;
Центральная электроанальгезия с 5-6 го дня цикла;
Медикаментозная терапия:
- гестагены (норколут) прегнит с 16-го дня цикла;
-комбинированные эстроген-гестагенные препараты (овулен, бисекурин, нон-овлон);
-антигистаминные препараты (тавегил, пипольфен, терален) - ежедневно за 2 дня до предполагаемого ухудшения состояния, включая и первый день менструации;
-парлодел (при повышении уровня пролактина) - во вторую фазу цикла за 2 дня до ухудшения состояния в течение 8-10 дней;
-диуретики (верошпирон, бринальдикс);
-витамин В6 (пиридоксин) - препарат, влияющий на обмен гистамина и обладающий антиэстрогенным действием;
-препараты, подавляющие синтез простагландинов (напросин, индометацин);
-психотропные средства (нейролептики, транквилизаторы) при эмоциональной лабильности.
Лечение проводят циклами по 3 месяца подряд с перерывом 2-3 месяца и возобновляют в случае рецидива заболевания. В переходном возрасте предпочтительнее лечение небольшими дозами (1/2-1/4 часть терапевтической дозы) 2-3 раза в день, начиная за 2-3 дня до средины цикла и продолжая до 2-3-го дня менструации.
При достижении положительного эффекта следует рекомендовать больным проводить профилактическое поддерживающее лечение при длительном стрессе, тяжелых экстрагенитальных заболеваниях, перемене климата, инфекционных заболеваниях.
За больными ПМС необходимо диспансерное наблюдение, так как они являются группой риска возникновения тяжелого климактерического синдрома, заболеваний сердечно-сосудистой системы, развития гиперпластических процессов в матке и молочных железах. Больные ПМС должны наблюдаться у гинеколога, терапевта, нефролога, психоневролога, невропатолога. Наблюдение должно проводиться 1 раз в 3 месяца, у остальных специалистов-1 раз в 4-6 месяцев.
Посткастрационный синдром - комплекс патологических вегетососудистых, нервно-психических и обменно-эндокринных симптомов, развивающихся после тотальной или субтотальной овариэктомии у женщин репродуктивного возраста.
Хирургическое выключение яичников вызывает сложные реакции адаптации в нейроэндокринной системе.
внезапное снижение уровня половых гормонов приводит к нарушению секреции неиротрансмиттеров, ответственных за функционирование подкорковых структур в мозгу, обеспечивающих координацию кардиоваскулярных, респмраторных, температурных реакций, что вызывает патологические симптомы;
нарушение секреции нейропетидов гипоталамуса (релизинг-гормонов) нарушают функцию важнейших желез внутренней секреции;
в коре надпочечников усиливается образование глюкокортикоидов;
после кастрации андрогены коры надпочечников являются единственным источником внегонадного синтеза эстрогенов в жировой ткани. Уменьшение образования андрогенов приводит к уменьшению синтеза эстрогенов и усугубляет процессы дезадаптации организма;
в щитовидной железе вследствие нарушения функции регулирующих механизмов нарушается синтез ее гормонов;
в патогенезе остеопороза ведущую роль играет снижение уровня эстрогенов и тестостерона, обладающих анаболическим действием и способствующих ретенции кальция костной тканью. Резорбция кальция из костной ткани и повышение уровня его в крови вызывают снижение секреции паратгормона паращитовидных желез. Уменьшается также содержание кальцитонина, образование которого стимулируют эстрогены. Уменьшение уровня кальцитонина и паратгормона подавляет процесс включения кальция в костную ткань и способствует вымыванию его в кровь и выделению с мочой.
Основные клинические проявления посткастрационного синдрома – вегетососудистые симптомы, приливы жара, покраснение лица, потливость, сердцебиение, артериальная гипертензия, боли в области сердца, головная боль.
Обменно-эндокринные нарушения при посткастрационном синдроме – ожирение, гиперхолестеринемия, гепатохолециститы.
Метаболические нарушения при посткастрационном синдроме – атрофические изменения в тканях наружных половых органов, молочных железах, уретре, мочевом пузыре:
влагалище – развитие кольпитов, появление трещин, лейкоплакии, крауроза вульвы;
молочные железы – замещение железистой ткани соединительной и жировой.
Трофические нарушения:
остеопороз, который проявляется локальными болями в поясничном или грудном отделе позвоночника, болью в области коленных, лучезапястных, плечевых суставах, ноющими болями в мышцах.
Клинические симптомы посткастрационного синдрома развиваются уже через 2-3 недели после операции и достигают полного развития через 2-3 месяца. В первые 2 года преобладают неровегетативные симптомы. У небольшого числа больных посткастрационный синдром в течение 2-3 лет подвергается обратному развитию, у большинства же больных он приобретает затяжное течение и длится до 8-10 лет.
Диагноз посткастрационного синдрома устанавливается на основании типичных клинических симптомов и анамнеза.
Лечение:
в настоящее время принята ранняя терапия посткастрационного синдрома, которую рекомендуется начинать после операции, не дожидаясь появления классических проявлений;
препараты, содержащие эстрогены – оральные контрацептивы (бисекурин, нон-овлон, овидон), трех- и двухфазные препараты (рекомендуется принимать в циклическом режиме); препараты конъюгированных эстрогенов (эстрона и эстриола). Эстрогенсодержащие препараты рекомендуется принимать в течение 3-4 месяцев с последующим перерывом до 1 месяца в зависимости от состояния женщины и возобновления у нее симптомов посткастрационного синдрома;
общеукрепляющая терапия;
витамины В1, С, РР;
транквилизаторы;
физиотерапевтические методы – начинают применять в первый месяц после операции. Используют микроволновую терапию волнами сантиметрового диапазона на область надпочечников, которую сочетают с закаливающими и тонизирующими процедурами (обтирание, обливание прохладной водой, ванны хвойные, морские, хлорнатриевые);
санаторно-курортное лечение – в условиях привычной для больных климатической зоны.
Климактерический синдром – клинический симптомокомплекс, развивающийся в процессе угасания функции репродуктивной системы на фоне общей возрастной инволюции организма, характеризующийся вазомоторными, эндокринно-обменными и нервно-психическими симптомами.
Наиболее типичные симптомы – приливы жара к лицу, голове, верхней половине туловища, потливость, сердцебиение, головокружение, нарушение сна, утомляемость, эмоциональная лабильность. Эти жалобы появляются в возрасте 46-50 лет, имеют различную интенсивность и могут продолжаться до 60 лет.
Возникновение климактерического синдрома связано с нарушениями адаптационных механизмов и метаболического равновесия в периоде возрастной перестройки нейроэндокринной системы на фоне прогрессивного снижения гормональной функции яичников.
Кроме вышеперечисленных симптомов, при климактерическом синдроме имеют место нарушения менструального цикла (ановуляторные циклы, скудные менструации, обильные ациклические кровотечения дисфункционального характера), изменения функции щитовидной и поджелудочной желез (сопровождаются чрезмерным увеличением массы тела или, наоборот, похуданием, развитием сахарного диабета или прогрессированием латентно протекающей его формы).
Выделяют следующие формы климактерического синдрома:
типичную форму – развивается у практически здоровых женщин и характеризуется обычной симптоматикой;
осложненную форму (сочетанную) – особенности клинического течения синдрома определяются сопутствующими заболеваниями. В этих случаях синдром протекает более тяжело, длительно и атипично с преобладанием симптомов сопутствующего заболевания.
По тяжести течения различают следующие формы климактерического синдрома:
легкая форма – относительно небольшое число приливов в течение суток (до 10) при ненарушенных общем состоянии и работоспособности больной;
форма средней тяжести – помимо приливов (до 10-20 в сутки), характерны головная боль, головокружения, ухудшение сна и памяти;
тяжелая форма – резко выраженные клинические проявления заболевания с почти полной трудоспособностью.
Лечение:
показаниями к лечению служит климактерический синдром тяжелой и средней тяжести;
общеукрепляющее лечение;
диета с включением в пищу овощей, фруктов;
витаминотерапия – витамины А (антигистаминное действие, ускоряет внутриклеточные окислительные процессы), С (воздействует на нарушенный липидный обмен), Е (улучшает капиллярное кровообращение в области гипофиза, способствует усилению синтеза холестерина и стероидных гормонов);
лечебная физкультура – утренняя гимнастика (15-20 мин.), групповые занятия (3 раза в неделю по 30-45 мин.), элементы спортивных игр, оздоровительно-тренировочные занятия;
лечебные ванны, веерный душ, подводный массаж;
нейролептики (френолон, этапиразин, трифтазин) – в течение 4-12 недель до получения терапевтического эффекта, после чего медленно и постепенно прекращают прием препарата;
парлодел (у больных с атипичным течением заболевания);
заместительная гормональная терапия:
малые дозы комбинированных эстроген-гестагенных препаратов (1/2-1/4 суточной контрацептивной дозы);
тканеспецифические гонадомиметики – тибалон.
ПОСЛЕРОДОВЫЕ НЕЙРОЭНДОКРИННЫЕ СИНДРОМЫ.
Послеродовый нейроэндокринный синдром (послеродовое ожирение) – особая форма нарушения менструальной и генеративной функции на фоне увеличения массы тела после беременности, законичившейся артифициальным или самопроизвольным абортом, или родами.
При послеродовом ожирении нарушения генеративной и менструальной функции развиваются в течение 3-12 месяцев после родов или прервавшейся беременности в сочетании с вегетативно-обменными нарушениями, ведущими среди которых является прогрессирующее нарастание массы тела.
При послеродовом ожирении у женщин с неблагоприятным преморбидным фоном (наследственная отягощенность эндокринными заболеваниями, ожирением, перенесенные в детском или пубертатном возрасте инфекции, интоксикации) восстановления гипофизотропных функций гипоталамуса и нормализации метаболических сдвигов не происходит и развивается клиническая картина синдрома, для которого характерны повышение выделения АКТГ и вследствие этого увеличение содержания кортизола; повышение выделения пролактина и уровня тестостерона в крови; незначительное снижение и выраженное уменьшение концентрации прогестерона (отсутствие овуляции); гипергликемия; нарушения липидного обмена – увеличение концентрации ЛПНП и ЛПОНП, холестерина, триглицеридов, повышение коэффициента атерогенности.
Женщины с послеродовым ожирением имеют характерный анамнез. Для семейного анамнеза характерны ожирение, сахарный диабет, диабетоподобные состояния, гипертензия. Женщины обычно отмечают неустойчивый менструальный цикл с начала менархе, тенденцию к задержкам, избыточную массу тела с детства, частые ОРВИ. Женщины часто болеют детскими инфекциями в пубертатном и постпубертатном возрасте. Основным анамнестическим признаком является быстрая прибавка массы тела (не менее 8-10 кг) после прервавшейся беременности или родов. Беременность и роды, как правило, протекают с явлениями гестоза и других осложнений и являются точкой отсчета для развития ожирения, нарушений цикла, бесплодия или гипертрихоза.
Клиническая симптоматика:
ожирение (массово-ростовой индекс обычно выше 30);
ановуляторная гипофункция яичников;
умеренный гипертрихоз;
тенденция к артериальной гипертензии;
гипрегликемия;
гипоталамические (диэнцефальные) нарушения – головная боль, быстрая утомляемость, головокружение, полиурия, полидипсия, полифагия, гипретермия;
характерный внешний вид – кушингоидное распределение жировой ткани, “климактерический горбик”, увеличение за счет ожирения окружности грудной клетки, увеличение межвертельного размера таза, полосы растяжения на коже живота, бедер и ягодиц, признаки гиперандрогении (жирная себорея, угреватая сыпь на коже лица, спины, груди);
нарушения менструального цикла (по гипоменструальному типу, реже ациклические маточные кровотечения), обусловленные нарушением гипоталамической регуляции выброса ЛГ и ФСГ гипофизом;
выраженные пролиферативные изменения в эндометрии (железисто-кистозная, рецидивирующая железисто-кистозная и атипическая гиперплазия);
фиброзно-кистозная мастопатия;
при лапароскопии:
первый тип изменений – неувеличенные яичники со сглаженной капсулой без следов овуляции и желтых тел;
второй тип изменений – увеличенные яичники с гладкой поверхностью, утолщенной белесоватой капсулой, через которую просвечивают множественные голубоватые кисточки диаметром 2-4 мм.
Большое значение в установлении диагноза послеродового ожирения имеют типичный анамнез, особенности течения заболевания и симптоматики и даже внешний вид больных. Женщинам, у которых предполагается диагноз послеродового ожирения, производят следующие диагностические процедуры:
рентгенографию турецкого седла и черепа с оценкой ложа гипофиза и измерением его размеров, учетом признаков внутричерепной гипертензии и гиперостоза;
ЭЭГ с функциональными нагрузками (световые, звуковые раздражители, дозированная гипервентиляция);
определение толерантности к глюкозе;
определение АКТГ, пролактина, кортизола, тестостерона в крови и 17-кетостероидов в моче;
биопсию эндометрия;
УЗ исследование яичников для установления из размеров;
лапароскопию с целью определения размеров яичников, их макроструктуры и получения биоптата для гистологического исследования.
Лечение:
редукционная диета, направленная на снижение массы тела; диетотерапия имеет целью снижение отрицательного энергетического баланса за счет ограничения калоража до 1200-1800 ккал при соблюдении принципов сбалансированного питания;
регуляторы нейромедиаторного обмена – хлоракон, дифенин. Их назначают женщинам, у которых в клинической картине преобладают явления гиперкортицизма;
парлодел, действие которого реализуется через нормализацию секреции дофамина. Его назначают женщинам с повышенным уровнем пролактина и гипертензией;
при отсутствии овуляции и наступления беременности на фоне нормализации массы тела и обмена веществ (следствие вторичных поликистозных яичников) стимулируют овуляцию кломифеном или проводят хирургическую стимуляцию овуляции (клиновидная резекция или термокаутеризация яичников при лапароскопии);
лечение гиперпластических процессов эндометрия – синтетические гестагены (норколут), комбинированные эстроген-гестагенные препараты. Терапию проводят под контролем биопсии (или аспирации) эндометрия каждые 3 месяца при атипической гиперплазии и каждые 6 месяцев при рецидивирующей гиперплазии эндометрия.
Послеродовый гипопитуитаризм (синдром Шиена) – синдром, развивающийся вследствие некротических изменений в гипофизе, возникающих на фоне спазма или внутрисосудистого свертывания крови в сосудах передней доли гипофиза после кровотечений или ИТШ при родах или абортах, характеризующийся симптомокомплексом, клинически проявляющимся в снижении функции периферических эндокринных желез.
Способствуют развитию вышеуказанных изменений особенности кровоснабжения гипофиза, масса передней доли которого во время беременности увеличивается в 2 раза. Определенную роль играют препараты спорыньи, широко применяемые во время родов и при кровотечениях. Гестоз является предрасполагающим фактором.
Выраженная клиническая картина синдрома Шиена развивается при поражении 80% ткани аденогипофиза.
При синдроме Шиена наряду с некротическими изменениями в гипофизе вследствие внутрисосудистых тромбозов возникают изменения трофического характера других органов и систем – почек, печени, мозговых структур. Предрасполагающими моментами для синдрома Шиена являются повторные частые роды (с интервалом менее 2 лет).
Синдром характеризуется различной степенью гипофункции щитовидной, надпочечниковой и половых желез.
Выделяют следующие формы синдрома:
глобальную – с клиническими проявлениями недостаточности тиреотропного, АКТГ, гонадотропинов (заболевание может протекать в легкой и тяжелой форме);
частичную – с недостаточностью гонадотропной, тиреотропной, адренокортикотропной функции;
комбинированную недостаточность:
гонадотропной и тиреотропной функций;
тиреотропной и адренокортикотропной функций;
гонадотропной и адренокортикотропной функций.
В зависимости от степени тяжести синдрома выделяют 3 формы:
легкую – характеризуется головной болью, быстрой утомляемостью, зябкостью, тенденцией к гипотензии. У больных отмечается снижение функции щитовидной железы и глюкокортикоидной функции надпочечников;
средней тяжести – характеризуется снижением гормональной функции яичников (олигоменорея, ановуляторное бесплодие), щитовидной железы (пастозность, склонность к отечности, ломкость ногтей, сухость кожи, утомляемость, гипотензия с наклонностью к обморокам).
тяжелую – выявляется симптоматика тотальной гипофункции гипофиза с выраженной недостаточностью гонадотропинов (стойкая аменорея, гипотрофия половых органов и молочных желез), тиреотропного гормона (микседема, облысение, сонливость, снижение памяти), АКТГ (гипотензия, адинамия, слабость, усиленная пигментация кожи), отмечается выраженное падение массы тела.
Для синдрома Шиена характерна анемия, плохо поддающаяся обычной терапии.
Решающим в установлении диагноза синдрома Шиена является характерный анамнез и связь начала заболевания с кровотечениями и ИТШ при родах или аборте. Характерным признаком синдрома является отсутствие нагрубания молочных желез после родов и агалактия. При гормональных исследованиях выявляют разной степени снижения в крови гонадотропинов, АКТГ и тиреотропного гормонов, гормонов щитовидной железы, эстрадиола, кортизола. При введении тропных гормонов соответственно повышается уровень периферических гормонов в крови. Отмечается также гипогликемия и гипогликемический тип кривой при нагрузке глюкозой; в моче снижено содержание 17-кетостероидов.
Лечение:
заместительная терапия глюкокортикоидами и тиреотропными препаратами при клинических проявлениях гипофункции соответствующих желез. Целесообразнее использовать кортизон и преднизолон, обладающие менее выраженной антикортикотропной активностью;
при аменорее или олигоменорее женщинам до 40 лет применяют циклическую гормонотерапию. После 40 лет используют андрогены, учитывая их анаболических эффект;
анаболические препараты (ретаболил, метиландростендиол);
витамины групп В, С, РР;
биостимуляторы (алоэ, ФИБС);
при анемии больным показаны препараты железа под контролем анализа крови;
питание должно быть полноценным, следует избегать дефицита белка.
Больных с тяжелой формой синдрома Шиена лечат только в условиях эндокринологического стационара.
Синдром Киарри-Фроммеля – характеризуется аменореей, галактореей и атрофией половых органов.
В основе заболевания лежит повышение секреции пролактина, что может быть связано с нарушением функции ацидофильных клеток передней доли гипофиза, ответственных за секрецию пролактина, с подавлением функции базофильных клеток, вырабатывающих фолликулостимулирующий гонадотропин, или с расстройством функции гипоталамуса, центры которого оказывают в норме тормозящее влияние на секрецию пролактина за счет пролактинингибирующего фактора.
Заболевание может быть связано с функциональными нарушениями в гипоталамо-гипофизарной системе, возникающими в связи с беременностью, после родов (особенно патологических), в результате длительного кормления грудью, а также вне связи с беременностью как последствие стресса или длительного применения лекарственных средств, ревматической инфекции или хромофобной аденомы гипофиза.
В патогенезе синдрома большое значение имеют нарушения количественных соотношений между продукцией эстрогенов, прогестерона и пролактина.
Заболевание чаще всего встречается в возрасте 17-35 лет.
Клиническая картина характеризуется продолжающейся лактацией вне физиологического периода (не связанной с беременностью или кормлением), нарушением менструального цикла в виде аменореи. Возможны также жалобы на головную боль, изменение массы тела (чаще прибавка, реже похудание), снижение остроты зрения. При длительном течении заболевания наступают атрофические изменения в половых органах.
Диагностика основывается на данных анамнеза (связь с беременностью и родами), характерных клинических симптомах, определении концентрации в крови фолликулостимулирующего гонадотропина, пролактина, эстрогенов и прогестерона.
При послеродовом синдроме Киари-Фроммеля (связанном с нарушением функции системы “гипоталамус-гипофиз”) проводят стимуляцию гипоталамической области и яичников. С этой целью применяются непрямая электростимуляция гипоталамо-гипофизарной области, введение эстрогенов, физиотерапия (электроназальный электрофорез витамина В1), электростимуляции шейки матки.
Наблюдается хороший эффект от применения кломифена, а также препарата L-ДОФА, который способствует высвобождению пролактинингибирующего фактора в гипоталамусе. Наилучший эффект дает применение парлодела, подавляющего продукцию пролактина.
СИНДРОМ СКЛЕРОКИСТОЗНЫХ ЯИЧНИКОВ
Синдром склерокистозных яичников (поликистозные яичники) – синдром, в совокупность симптомов которого входят аменорея, гирсутизм, бесплодие, ожирение и двустороннее увеличение яичников.
Выделяют следующие клинические и патогенетические формы синдрома склерокистозных яичников:
первичные склерокистозные яичники:
яичниковая форма
вторичные склерокистозные яичники:
надпочечниковая форма
гипоталамо-гипофизарная форма.
Яичниковая форма (первичные поликистозные яичники, синдром Штеина-Левенталя).
Ведущую роль в развитии яичниковой формы играют нарушения ритмичного (цирхорального) выброса гонадотропного рилизинг-гормона в медиобазальных структурах гипоталамуса вследствие инфекции, интоксикации, возможно, генетической природы. Эти изменения формируются в препубертатном и пубертатном периоде, вследствие чего циклическая секреция гонадотропинов не устанавливается. Опосредованно нарушается процесс созревания фолликулов и формируется хроническая ановуляторная дисфункция яичников. Эти функциональные изменения вызывают ряд морфологических изменений в яичниках: кистозную атрезию фолликулов, гиперплазию клеток теки и стромы яичников (места секреции андрогенов), дистрофические процессы в клетках гранулезы, утолщение белочной оболочки. Нарушается гормональная секреция – усиливается образование андрогенов и уменьшается образование эстрогенов в яичниках.
Хроническая ановуляция с периода полового созревания обусловливает кардинальный симптом яичниковой формы склерокистозных яичников – первичное бесплодие; постоянным симптомом являются ациклические, редкие менструации (олигоменорея), реже вторичная аменорея, умеренный гипертрихоз и ожирение универсального характера с равномерным распределением жировой ткани. Все эти симптомы появляются с пубертатного возраста.
Нередко отмечаются гиперпластические процессы в эндометрии (железисто-кистозная гиперплазия, аденоматозная гиперплазия, аденоматозные полипы) как результат постоянного действия эстрогенов при отсутствии влияния прогестерона, вызывающего секреторную трансформацию слизистой оболочки матки.
Основным патогномоничным симптомом первичных склерокистозных яичников является двухстороннее увеличение яичников (в 2-6 раз).
Макроскопически (при лапароскопии или лапаротомии) яичники имеют характерный вид: гладкая, утолщенная капсула перламутрового цвета с мелкими, древовидно ветвящимися сосудами по поверхности; множественные мелкие кисточки (атрезирующиеся фолликулы)около 5-8 мм в диаметре обычно не просвечивают через утолщенную капсулу яичника, но хорошо видны на разрезе.
Диагностика:
анамнез – первичное бесплодие, олигоменорея, ожирение и гипертрихоз с периода менархе;
УЗ-исследование (изменения особенно хорошо видны при использовании влагалищных датчиков);
увеличение тестостерона в крови и 17-кетостероидов в моче;
при проведении пробы с дексаметазоном содержание 17-кетостероидов в моче и тестостерона в крови снижается на 30-40%;
лапароскопия.
Лечение:
Консервативное:
Стимуляция овуляции кломифеном с 5-го по 9-й день от начала менструальных выделений, самостоятельных или индуцированных приемом синтетических эстроген-гестагенных препаратов. До этого в течение 3-х месяцев рекомендуется провести курс приема синтетических прогестинов. После приема кломифена необходимы контрольные исследования: измерение базальной температуры, регистрация величины фолликула с помощью УЗИ, определение эстрадиола на 10-12-й день и прогестерона на 22-24-й день в крови;
При стимуляции секреции прогестерона при недостаточности лютеиновой фазы после кломифенотерапии рекомендуется хорионический гонадотропин на 13-й, 14-й, 15-й дни цикла;
Оперативное:
Двухсторонняя клиновидная резекция яичников – производится при неэффективной терапии кломифеном в течение 6 месяцев и наличии аденоматозных изменений в эндометрии, длительности бесплодия более 5 лет и у женщин, впервые обратившихся к врачу в возрасте старше 30 лет. В день операции производится выскабливание слизистой оболочки матки с целью удаления патологически измененной слизистой оболочки и исключения предраковых изменений эндометрия;
Термо- и электрокаутеризация яичников, лазеропунктура во время лапароскопии.
Профилактика гиперпластических процессов эндометрия проводится с помощью синтетических прогестинов (типа однофазных оральных контрацептивов). Препараты назначают в течение 6-8 месяцев с последующим контролем состояния эндометрия. Эта терапия способствует уменьшению гипертрихоза и уменьшению размеров яичников.
Надпочечниковая форма (поликистозные яичники надпочечникового генеза) – развивается на фоне постпубертатного адреногенитального синдрома. При этой форме повышение синтеза андрогенов в коре надпочечников подавляет выделение гонадотропных гормонов аденогипофизом, секреция гонадотропинов приобретает монотонный характер. В результате подавляется процесс овуляции, нарушается процесс фолликулогенеза в яичниках и формируется кистозная атрезия фолликулов. Увеличение яичников не столь выражено (в 1,5-2 раза), иногда увеличение имеет асимметричных характер. Макроскопически (при лапароскопии) капсула яичников сглажена, белесоватого цвета, утолщена, через нее просвечивают множественные кистозные фолликулы диаметром до 5-8 мм.
При надпочечниковой форме склерокистозных яичников отсутствует ожирение, гипертрихоз имеет более выраженный характер, сочетается с акне, жирной себореей, телосложение имеет нерезко выраженные вирильные черты (широкие плечи, узкий таз). Менструальный цикл нарушен по типу олигоменореи; как правило, имеет место ановуляция, реже – недостаточность лютеиновой фазы. Беременность наступает редко и, как правило, заканчивается самопроизвольным абортом при сроке до 8-10 недель.
Диагноз:
анамнез (прерывание беременности ранних сроков);
осмотр (выраженный гипертрихоз, отсутствие ожирения);
УЗИ яичников;
увеличение концентрации тестостерона в крови и 17-кетостероидов в моче и ее снижение на 50-75% после проведения пробы с дексаметазоном.
Лечение:
терапия дексаметазоном под контролем характера менструального цикла, базальной температуры, выделения 17-кетостероидов с мочой;
стимуляция овуляции кломифеном (при отсутствии ее в течение 2-3 месяцев глюкокортикоидной терапии);
для уменьшения гипертрихоза – верошпирон (обладает антиандрогенными свойствами), препарат “Диане”;
если женщина не заинтересована в беременности, регулировать менструальный цикл и уменьшить гипертрихоз можно с помощью гормональных контрацептивов;
Гипоталамо-гипофизарная форма (поликистозные яичники центрального генеза) – развивается у женщин на фоне нейроэндокринного синдрома, послеродового ожирения, гипоталамического или диэнцефального синдрома.
Нарушение функционального состояния гипоталамических структур при этой форме происходит под влиянием осложнений беременности и в родов, инфекции, интоксикации, стрессов, травмы мозга. При отсутствии лечения развивается хроническая ановуляция с формированием морфологических и гормональных нарушений яичников, что приводит к развитию вторичных склерокистозных яичников.
Клиническая картина характеризуется множественными проявлениями гипоталамических нарушений: вегетососудистой дистонией, нарушениями аппетита, сна и бодрствования, жаждой, раздражительностью, плаксивостью, нарушениями жирового обмена, углеводного обмена (гипергликемия), что приводит к значительному увеличению массы тела (отложение жира на плечевом поясе, “климактерический горбик”). Характерно наличие полос растяжения на коже и усиленной гиперпигментации в области складок кожи. Менструальный цикл нарушен по типу олигоменореи, редко аменореи. Нередко отмечаются дисфункциональные маточные кровотечения из гиперплазированного эндометрия. Бесплодие при этой форме чаще вторичное, гипертрихоз имеет умеренный характер, возникает одновременно с ожирением и по мере прогрессирования ожирения усиливается.
Диагноз:
анамнез;
УЗИ яичников;
лапароскопия.
Лечение:
коррекция метаболических нарушений (для снижения массы тела) – редукционная диета с ограничением жиров и углеводов, умеренные физические нагрузки;
лекарственные препараты, регулирующие нейромедиаторный обмен (дифенин, хлоракон, парлодел);
стимуляция овуляции кломифеном (при отсутствии овуляции после снижения массы тела);
синтетические прогестины типа оральных контрацептивов (женщинам с гиперпластическими процессами в эндометрии);
клиновидная резекция яичников (женщинам с гиперпластическими процессами в эндометрии, при длительности заболевания более 5 лет, в течение которых стимуляция овуляции и была неэффективна).
КЛИНИКА, ДИАГНОСТИКА И ЛЕЧЕНИЕ ВОСПАЛИТЕЛЬНЫХ ПРОЦЕССОВ ЖЕНСКИХ ПОЛОВЫХ ОРГАНОВ ИНФЕКЦИОННОЙ ЭТИОЛОГИИ В СОВРЕМЕННЫХ УСЛОВИЯХ.
Механизмы, препятствующие активизации условно-патогенных микроорганизмов, присутствующих в половых путях, и их участие в воспалительном процессе:
физиологическая десквамация и цитолиз поверхностных клеток эпителия влагалища, обусловленные влиянием яичниковых гормонов;
неспецифические антимикробные механизмы, действующие на клеточном уровне: фагоцитоз, неспецифические гуморальные факторы (трансферрин; опсонины, усиливающие фагоцитарную активность клеток), лизоцим (обладает антимикробной активностью), лизин (выделяется тромбоцитами в очаге воспаления);
иммунные механизмы защиты от грибковой, вирусной инфекции, внутриклеточных бактериальных паразитов (Т-лимфоциты, иммуноглобулины, система комплемента);
для верхних отделов половой системы особое значение имеют защитные организмы на уровне цервикального канала и эндометрия:
слизь, скапливающаяся в цервикальном канале представляет собой своеобразный барьер, разделяющий верхние и нижние отделы полового тракта. Цервикальная слизь содержит антибактериальные вещества, антитела к таким микроорганизмам, как кишечная палочка, гонококки, сальмонелла, антитела к вирусам простого герпеса и грибам кандида;
в матке защитную функцию несет эндометрий, препятствующий проникновению микроорганизмов периодическим отторжением его функционального слоя во время менструации. Определенную защитную функцию во время менструации несут лейкоциты, инфильтритующие базальный слой эндометрия. Богатое кровоснабжение матки обеспечивает ее гуморальными факторами защиты.
Проникновение инфекционных агентов в верхние половые пути происходит с помощью сперматозоидов, трихомонад, возможен пассивный транспорт микроорганизмов, на последнем месте – гематогенный и лимфогенный пути.
Проникновению инфекции в верхние половые пути способствуют внутриматочные процедуры (зондирование, гистеросальпингография, гистероскопия, пертубация, гидротубация, операции на половых органах), прерывание беременности.
Возбудителей воспалительных заболеваний женских половых органов делят на:
специфические – туберкулез, гонорея;
неспецифические – стафилококк, кишечная палочка, хламидии, микоплазмы, вирусы и др. (УПМ)
