
- •10/1. Основные разделы и методы. Содержание и задачи курса. Общенаучное и практическое значение науки о поверхностных явлениях и дисперсных системах. Исторические этапы развития науки.
- •10/2.Мицеллообразование. Понятие о ккм. Строение мицелл. Мицеллы пав в водных растворах. Моющее действие мыл.
- •10/3.Для коагуляции 10 -3 золя гидроксида алюминия требуется 10 мл раствора сульфата алюминия с концентрацией 0,01 кмоль/м3. Определите порог коагуляции золя.
- •12/1. Основные классификации: по дисперсности, агрегатному состоянию вещества, структуре, межфазному взаимодействию. Получение дисперсных систем.
- •13/2. Молекулярные коллоиды. Строение и свойства. Взаимодействие с растворителем.
- •14/1. Лиофобные дисперсные системы. Факторы устойчивости лиофобных систем. Быстрая и медленная коагуляция. Кинетика коагуляции по Смолуховскому, уравнение Смолуховского.
- •14/2.Приведите и охарактеризуйте основные физико-химические свойства растворов белков.
- •15/1. Аэрозоли. Способы получения и свойства аэрозолей. Факторы устойчивости аэрозолей.
- •15/2. Адсорбция и пов-тное натяжение. Связи адсорбции с параметрами системы. Изотерма адсорбции.
- •15/3. Классификация свободнодисперсных систем по размерам частиц. Лиофильные и лиофобные золи. Приведите примеры типичных мицелл, поясните их состав, в чем они одинаковы, чем различаются.
- •16/1. Метод избытков Гиббса. Фундаментальное адсорбционное уравнение Гиббса. Гиббсовская адсорбция. Частное выражение уравнения Гиббса.
- •16/2. Эмульсии. Приведите классификации эмульсий и методы их изучения. Опишите основные физ-хим. Св-ва. Что такое обращение фаз эмульсий?
- •17/1. Поверхностная активность.Адсорбция орг.Мол-л.Правило Траубе.Понятие о пав.
- •17/2.Приведите классификацию структурир. Систем.Опишите мех-мы образ-ия и разруш-ия структурир.Систем.Что такое тиксотропия, синерезис?
- •17/3.Общая хар-ка поверхн-ой энергии.Поверхн.Эн.В общем ур-ии I и II начал термодин-ки. Пов-тное натяжение как мера энергии Гиббса межфазной границы.
- •18/1.Структурир.Системы.Вязкость и упругопластические св-ва дисп.Систем.Ур-ие Ньютона.
- •18/2.Кинетика коагуляции.Ур-ие Смолуховского.
- •18/3.Задачи кол.Химии в решении экологич.Проблем.На примере решения проблем водо-газоочистки.
- •19/1Суспензии,их полидисперсность.Стабилизация суспензий в водных и орг.Средах. Технич-ие суспензии и пасты мин.И орг.В-в.
- •19/2.Кинетика коагуляции эл-тами.Теории коагуляции эл-тами;химическая,длфо.
- •19/3.Правило фаз Гиббса и дисперсность.
- •20/1.Получение дисп.Сис-м.Методы диспергирования. Адсорбционное ↓ прочности (эффект Ребиндера).
- •20/3.Классификация мех-мов адсорбции(физ.Адсорбция,хемосорбция и ионообменная). Особенности составляющих сил Ван-дер-Ваальса при адсорбции.
- •21/1.Факторы устойчивости.Коагуляция типично гидрофоб.Коллоидов.Опишите осн. Факторы коагуляции без исп.Электролитов.
- •21/2.Адсорбция газов и паров на однород.Пов-ти.З-н Генри.Ур-ие мономолек.Адсорбции Ленгмюра и его анализ.Опред-ие констант в ур-ии Ленгмюра.
- •2 1/3.Для коагуляции 10-3 м3 золя Al(oh)3 требуется 10 мл р-ра Al2(so4)3 с конц-цией 0,01 кмоль/м3.Определите порог коагуляции.
- •22/1.Теория полимолекулярной адсорбции бэт,ур-ие изотермы адсорбции,его анализ.
- •22/2.Электрокинетические явления. Электрофорез. Потенциал и ток течения. Эффект седиментации.
- •22/3. Что такое частичная концентрация? Какие методы ее определения вы знаете?
- •23/1 Пористые тела. Колич. Хар-ки пористых материалов. Классификация пористых тел по Дубинину.
- •23/2Теории д.Э.С Гуи-Чэмпэна, Штерна. Представления Грэма.Электрокинетический потенциал.
- •24/1Особенности адсорбции на микропористых материалах. Потенциальная теория Поляни. Адсорбционный потенциал. Характеристическая кривая адсорбции.
- •24/2 Что такое электрокинетический потенциал? Какие факторы определяют величину этого потенциала?
- •26/1 Возникновение объёмно-пористых стр-р. Структурообразование по теории длфо. Коагуляционно- тиксотропные и конденсационно- кристаллизационные стр-ры.
- •27/1.Ньютоновские и неньютоновские жидкости. Вязкость жидких агрегативно устойчивых дисперсных систем. Уравнение Бингама и Эйнштейна. Измерения вязкости с помощью вискозиметра.
- •27/2 Природные и синтетические вмс. Строение макромолекул и их св-ва. Набухание и растворение вмс. Степень и скрость набухания.
- •27/3 Расклинивающее давление и его составляющие
- •28/1Общие вопросы устойчивости дисперсных систем. Седиментационная и агрегативная устойчивость.
- •28/2 Адсорбция на границе раствор-газ. Поверхностное натяжение. Уравнение Гиббса и его анализ.
- •29/1 Классификация поверхностных явлений. Смачивание. Краевой угол смачивания. Уравнение Юнга.
- •29/2.Почему и в каких случаях лиофильные золи проявляют свойства растворов низкомолекулярных веществ и коллоидных систем?
- •29/3Адгезия, когезия, смачивание и растекание жидкости. Уравнение Дюпре для работы адгезии. Закон Юнга. Связь работы адгезии с краевым углом (уравнение Дюпре-Юнга).
- •30/1 Природные и синтетические вмс. Строение макромолекул и их свойства. Набухание и растворение вмс. Степень и скорость набухания.
- •30/3 Критическая концентрация мицеллобразования (ккм). Основные факторы, влияющие на ккм. Методы определения ккм.
- •1/1 Термодинамика растворения вмс. Влияние природы вмс и растворителя на состояние макромолекул в растворе. Ассоциаты молекул. Возможность микрогетерогенности в растворе вмс.
- •1/2 Капиллярные явления и их роль в природе и технологии. Уравнение капиллярной конденсации Кельвина.
- •2/1 Получение и важнейшие методы обнаружения дисперсных систем.
- •2/3 Факторы стабилизации в системах с твердой дисперсной средой. Высокопористые материалы, их классификация и специфические особенности.
- •3/1 Двойной электрический слой по теории Штерна, перезарядка поверхности. Строение мицеллы и дэс.
- •3/2Специфика свойств дисперсных систем. Классификация по дисперсности, агрегатному состоянию, структуре, межфазному взаимодействию.
- •3/3Броуновское движение и его молекулярно-кинетическая природа. Связь между средним сдвигом частиц и коэффициентом диффузии (закон Эйнштейна – Смолуховского).
- •4/1Особенности оптических свойств дисперсных систем. Уравнение Релея для светорассеяния и его анализ. Фиктивное поглощение света дисперсными системами и уравнение Ламберта-Бугера-Бера.
- •4/2Студни. Схема взаимосвязи процессов образования и распада структур в системе геля.
- •4/3Теории Поляни-Дубинина объемного заполнения микропор.
- •5/3Сравнительная характеристика физической и химической адсорбции. Уравнение Фрейндлиха. Изотерма адсорбции. Теплота адсорбции. Кинетика адсорбции.
- •6/1Растворы вмс. Получение и св-ва р-ров вмс. Изоэлектрическое состояние м-л вмс.
- •6/2Рассеяние света дисперсными системами. Анализ уравнения Рэлея.
- •6/3 Что такое структурная вязкость и как он меняется под нагрузкой.
- •7/1Модель двойного электрического слоя на пов-ти ч-цы золя (по Гельмгольцу-Гуи-Штерну). Поясните, как меняется потенциал в дэс. Электрокинетический потенциал.
- •8/1.Структурированные дисперсные системы. Классификация, методы получения и основные св-ва: тиксотропия, синерезис, релаксационные явления, гистерезис.
- •8/2. Диффузия. Законы Фика для диффузии. Коэффициент диффузии.
- •8/3. Напишите формулу мицеллы золя на основе агрегата PbO2 c отрицательным зарядом мицеллы. Поясните роль адсорбционных процессов в образовании мицеллы.
- •9/1 Белки. Физико-химические свойства растворов белков. Строение пленок белков на межфазной поверхности.
- •9/2.Механизмы возникновения заряда на частицах дисперсной фазы. Строение дэс по Штерну-Гельмгольцу-Гуи.
- •88. Ассоциирование органических молекул в растворах.
- •31/2. Гели. Получение и свойства. Механизм и кинетика набухания.
- •36.Седиментационно-диффузное равновесие в золях. Условие этого равновесия.
- •11/3Структурно – механические св-ва дисперсных систем. Понятие о деформациях, прочности, пластичности
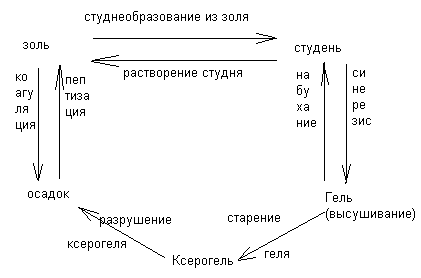
4/2Студни. Схема взаимосвязи процессов образования и распада структур в системе геля.
Студни – структурированные дисперсные системы с жидкой дисперсионной средой, образованные молекулами полимера и растворителя.
Способ получения: набухание образца полимера, разрушение растворов полимеров.
Специфические свойства: термодинамически неустойчивы, набухают, тиксотропны, способны к релаксации и синерезису.
Пример: пищевые студни, желе, карамели, творог.
Схема:
4/3Теории Поляни-Дубинина объемного заполнения микропор.
Адсорбция на пористых телах зависит от структуры и размера пор, от природы взаимодействующих веществ, от внешних факторов (температуры, давления), от характера транспортных явлений в порах.Основа теории объемного заполнения пор – теория Поляни о многослойной адсорбции.
Основные положения теории Поляни о многослойной адсорбции:
адсорбция обусловлена физическими силами, прежде всего дисперсионными силами.
активных центров на поверхности нет, но существует поле адсорбционных сил;
адсорбционные силы действуют на больших расстояниях от поверхности, образуя объем, наполняемый молекулами адсорбтива;
действие адсорбционных сил при удалении от поверхности падает до нуля;
притяжение адсорбированной молекулы к поверхности адсорбента не зависит от наличия других адсорбирующихся молекул;
адсорбционные силы не зависят от температуры, т.е. с изменением температуры объем не изменяется. Действие температуры связывается с интенсивностью теплового движения молекул адсорбтива.
Теория объемного заполнения микропор адаптирует положения теории Поляни применительно к специфике адсорбции в пористых телах.
Специфика заключается в следующем:
в микропорах адсорбированные молекулы взаимодействуют между собой и со стенками пор. В результате происходит объемное заполнение пор адсорбированным веществом. Это позволяет в качестве основного геометрического параметра использовать объем микропор;
адсорбция в микропорах избирательна из-за ситового эффекта и того, что большинство молекул взаимодействуют с поверхностью адсорбента;
в микропорах поля поверхностных сил противоположных стенок пор перекрываются. Это значительно повышает энергию адсорбции.
За меру адсорбционного взаимодействия в теории объемного заполнения микропор принят адсорбционный потенциал ε, кот. Соответствуем работе переноса 1 моля газа с поверхности жидкого адсорбата (давление рs) в равновесную газовую фазу (давление р): ε=RTln(ps/p).
Т.о. задача теории объемного заполнения микропор сводится к поиску способа перехода от обычных координат изотермы(А, р) к параметрам адсорбционного поля, т.е к установлению взаимосвязи этих параметров.
Д ля
описания адсорбции Поляни предложил
использовать не обычные изотермы
адсорбции, а зависимости ε от V,
где V
– адсорбционный объем.(экспериментально
определяется с помощью изотермы
адсорбции вида V=AVм
Зависимость ε от V
не меняется с изменением температуры,
поэтому кривые, соответствующие этим
зависимостям, назыв. характеристическими
кривыми.
ля
описания адсорбции Поляни предложил
использовать не обычные изотермы
адсорбции, а зависимости ε от V,
где V
– адсорбционный объем.(экспериментально
определяется с помощью изотермы
адсорбции вида V=AVм
Зависимость ε от V
не меняется с изменением температуры,
поэтому кривые, соответствующие этим
зависимостям, назыв. характеристическими
кривыми.
На основе характеристических кривых можно, зная изотерму при любой температуре, построить изотерму при любой другой температуре, по схеме: А1→φ→А2 и р1→ ε →р2
Т.о. теория Поляни позволяет вычислить величину адсорбции для любой заданной температуры, если известна хотя бы одна изотерма.
Дубинин показал зависимость м/у адсорбционным объемом и адсорбционным потенциалом V=Vmaxexp[-(ε/E)n] или A=Amaxexp[-(ε/E)n], где А и Amax – адсорбция и максимальная адсорбция соответственно, V и Vmax – заполненный объем и предельный объем абсорбционного пространства, Е – характеристическая энергия адсорбции, не зависящая от температуры, n – параметр, не зависящий от температуры.
Интегрируя, получим: lnA=lnAmax- ε n(1/E).
5/1 Гомогенная и гетерогенная конденсация. Метастабильное состояние. Механизм мицеллообразования при получении золей методом химической конденсации.
Гомогенная конденсация – образование жидкости из паров
Гетерогенная конденсация – слияние мельчайших капелек жидкости.
Метастабильное состояние – неустойчивое состояние системы, кот. легко получается из стационарного режима малейшим внешним воздействием.
Механизм получения мицелл методом хим. конденсации:
Образование зародышей.
2 механизма образования зародышей
гомогенный - новая фаза зарождается в исходно однородном перенасыщенном р-ре. М-лы образуют небольшие кластеры (образования из нескольких десятков м-л), являющиеся центрами дальнейшей кристаллизации.
гетерогенный - зародыши появляются в местах неоднородностей исходной фазы. Центрами кристаллизации в этом случае могут служить мельчайшие примеси: отдельные пылинки или заряженные ч-цы.
Кристаллизация
Происходит
кристаллизация ионов на пов-ти зародыша
и образование агрегата заданных
размеров. Скорость кристаллизации
лимитирует скорость диффузии (з-н Фика):
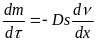 ,
где m
– масса диффундирующего в-ва,
,
где m
– масса диффундирующего в-ва,
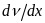 - градиент частичной концентрации, D
– коэффициент диффузии.
- градиент частичной концентрации, D
– коэффициент диффузии.
Адсорбция стабилизатора и возникновение ДЭС.
Представляет собой заключительный этап образования золя. На этой стадии прекращают рост кристаллов и стабилизируют коллоидную сис-иу добавками стабилизаторов. Стабилизатором м. служить ионы одного из реагентов, используемых для получения в-ва дисп. фазы, если этот реагент взят в избытке. Ионы стабилизатора адсорбируются на пов-ти микрокристаллического агрегата и заряжают ее. В дальнейшем на заряженной пов-ти формируется ДЭС, кот. определяет устойчивость и электронейтральность ч-ц дисп. фазы.
5/2 Изотермическая перегонка в дисперсных системах (ИПДС)
ИПДС состоит в том, что в полидисперсной системе происходит перенос в-ва от мелких ч-ц дисперсной фазы к более крупным.
Следствием процесса является постепенное исчезновение мелких ч-ц, уменьшение средней дисперсности и свободной энергии, т.е. ИПДС – один из механизмов разрушения дисперсных сис-м.
Движущая сила этого процесса – стремление сис-мы уменьшить свободную энергию и перейти в равновесное состояние. Перераспределение в-ва от мелких ч-ц к более крупным для дисперсных сис-м оказывается наиболее выгодным энергетическим процессом, уменьшающим свободную энергию сис-мы и выравнивающим хим. потенциалы в-ва в отдельных ч-цах.
Выделяют 3 основные стадии изотермич. перегонки:
растворение или испарение мелких ч-ц
транспорт в-ва от мелких ч-ц к более крупным
рост крупных ч-ц.
Растворимость
мелких сферических ч-ц c(r)
связана с размером ч-ц r:
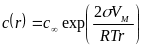 ,
где с∞
- растворимость макроч-ц, Vм
– мольный объем.
,
где с∞
- растворимость макроч-ц, Vм
– мольный объем.
Транспорт
в-ва при ИПДС осущ-ся посредством
диффузии, которую количественно можно
описать с пом. з-на Фика :
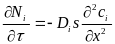 ,
где Ni
– число продиффундировавших м-л в-ва
i;
,
где Ni
– число продиффундировавших м-л в-ва
i;
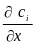 -градиент
изменения молярной концентрации, s
– пл-дь поперечного сечения, ч/з кот.
происходит диффузия, Di
– коэффициент диффузии.
-градиент
изменения молярной концентрации, s
– пл-дь поперечного сечения, ч/з кот.
происходит диффузия, Di
– коэффициент диффузии.
Растворимость ч-ц определяет концентрацию в-ва у пов-ти различных ч-ц. Разность м/у поверхностными концентрациями у малых и больших ч-ц влияет на величину градиента конц-ции (∆с), параметра, входящего в ур-ние Фика: ∆c=c(r1)-c(r2)
Если
r2
значительно больше r1,
то разность концентраций будет
определяться главным образом конц-цией
у пов-ти малой ч-цы, а значит – размером
малой ч-цы. Поэтому принимая r2
постоянной, разложив экспонент в ряд,
получим:
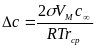 , где rср
– некоторый средний размер ч-ц.
, где rср
– некоторый средний размер ч-ц.
Т.к. величина ∆с определяет градиент концентрации – параметр, входящий в ур-ние Фика, можно сделать вывод, что транспорт в-ва при изотермической перегонке зависит от величины коэффициента диффузии, от растворимости в-ва дисперсной фазы, размеров ч-ц, поверхностного натяжения и температуры.
