
Образование галогенангидридов и их свойства
Гидроксил карбоксильной группы может быть замещен галогеном; при этом образуются галогенангидриды карбоновых кислот. Наиболее часто применяются хлорангидриды; они образуются, например, при действии на кислоты пятихлористого фосфора PCl5:
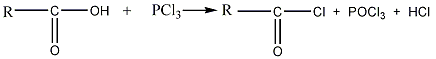
карбоновая кислота хлорангидрид карбоновой кислоты
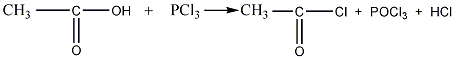
уксусная кислота хлорангидрид уксусной кислоты
В галогенангидридах галоген соединен с радикалом кислоты – ацилом, поэтому их иначе называют галогенацилами или ацилгалогенидами. В частности, хлорангидрид уксусной кислоты называется хлористым ацетилом или ацетилхлоридом. Он представляет собой бесцветную дымящую на воздухе жидкость с Ткип. 55 оС.
Галогенангидриды – очень реакционноспособные вещества; их применяют для разнообразных синтезов, при которых галоген обменивается на различные группы и образуются другие производные кислот. При действии воды происходит гидролиз галогенангидридов и они разлагаются, образуя карбоновую кислоту и галогеноводород:
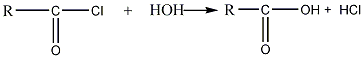
хлорангидрид кислота
С хлорангидридами низших кислот реакция протекает уже на холоду, обычно бурно, с выделением тепла.
Образование ангидридов и их свойства
1. При отщеплении молекулы воды от двух молекул кислоты образуются ангидриды карбоновых кислот. Реакция протекает под влиянием катализатора, над которым пропускают пары кислот, и может быть в общем виде представлена схемой:
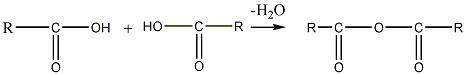
кислота кислота ангидрид
Как видно из общей формулы (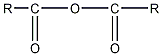 ),
ангидриды представляют собой производные
кислот, состоящие из двух соединенных
через кислород кислотных остатков
(ацилов).
),
ангидриды представляют собой производные
кислот, состоящие из двух соединенных
через кислород кислотных остатков
(ацилов).
2. Ангидриды получают также действием галогенангидрида кислоты на соль той же кислоты:
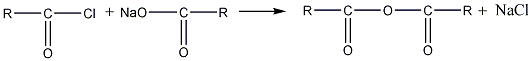
хлорангидрид соль ангидрид
Большое практическое значение имеет ангидрид уксусной кислоты, или уксусный ангидрид (ацетангидрид). Он может быть получен из хлористого ацетила и ацетата натрия:
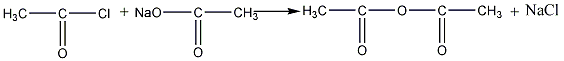
хлористый ацетил ацетат натрия ацетангидрид
3. В настоящее время ангидрид получают действием карбоновой кислоты на кетен:
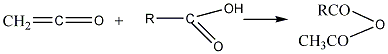
кетен карбоновая кислота ангидрид
Ангидриды кислот, подобно галогенангидридам, очень реакционноспособны; они разлагаются соединениями с активны водородом, образуя производное кислоты и свободную кислоту. При действии воды ангидриды гидролизуются на две молекулы кислоты (а), под действием аммиака образуются соответствующие амины (b), воздействием спирта можно получить соответствующий сложный эфир (c):
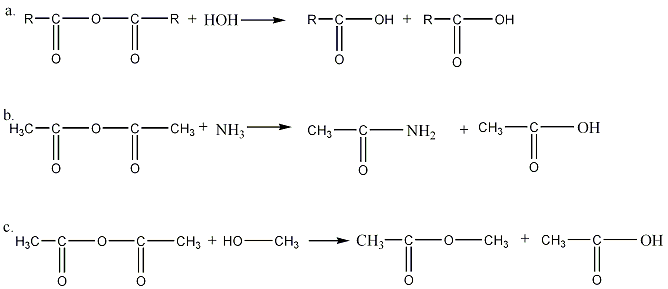
4. Двухосновные кислоты с четырьмя и пятью атомами углерода в молекуле, т. е. янтарная и глутаровая кислоты, при нагревании отщепляют элементы воды и дают внутренние циклические ангидриды:
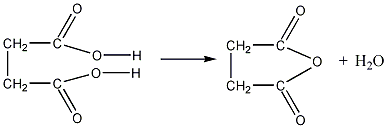
янтарная кислота ангидрид янтарной кислоты
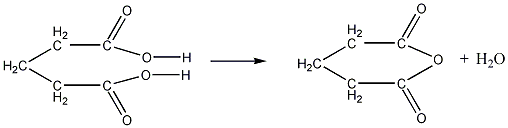
глутаровая кислота ангидрид глутаровой кислоты
Способность янтарной и глутаровой кислот давать циклические ангидриды легко объяснима при рассмотрении пространственных моделей. Так как валентный угол в тетраэдрическом атоме углерода равен 109°28', то углеродная цепь из четырех или пяти атомов может быть изогнута в виде клешни, концы которой близко подходят друг к другу. Если на концах этой цепи находятся карбоксильные группы (как, например, у янтарной и глутаровой кислот), то при таком близком расположении они, отщепляя молекулу воды, замыкают цикл. В результате образуется устойчивый пяти- или шестичленный цикл. Циклические ангидриды при реакции с аммиаком легко дают циклические амиды, обладающие кислотными свойствами:
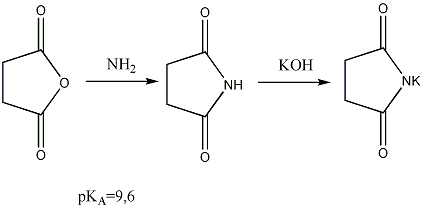
Непредельные карбоновые кислоты
Состав непредельных одноосновных кислот с одной двойной связью можно выразить общей формулой СnН2n-1СООН. Как и для любых бифункциональных соединений, для них характерны реакции как кислот, так и олефинов. а, З-Непредельные кислоты несколько превосходят по силе соответствующие жирные кислоты, так как двойная связь, находящаяся рядом с карбоксильной группой, усиливает ее кислотные свойства.
Акриловая кислота. В технике акриловую кислоту получают из этиленоксида и синильной кислоты через этиленциангидрин:
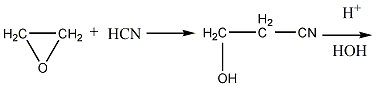
этиленоксид этиленциангидрид
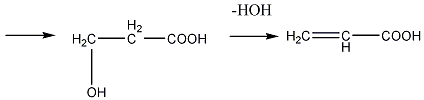
β-оксипропионовая кислота
Номенклатура:
Ангидриды называют следующим образом – первое слово ангидрид, а второе – название карбоновой кислоты от которой образован ангидрид.
