
- •21. Механические и конформационные свойства мембран. Фазовые переходы.
- •Раздел 5. Транспорт веществ и биоэлектрогенез
- •22. Транспорт неэлектролитов через мембраны. Диффузия: движущая сила. Закон Фика. Понятие об облегчённой диффузии.
- •23. Транспорт ионов через мембрану. Механизмы и движущая сила пассивного транспорта. Уравнение электрохимического потенциала.
- •24. Энергия иона и причины её понижения при транспорте через биомембраны.
- •26. Электродиффузная теория транспорта ионов через мембрану. Уравнение Нерста-Планка для потока ионов через мембрану. Уравнение Гольдмана.
- •27. Индуцированный ионный тран-т через мембрану.Затраты энерг. По формуле Борна.
- •25. Электрические свойства биомембран и транспорт ионов. Понятие о двойном электрическом слое. Плотность распределения ионов в зависимости от расстояния. Электрокинетический потенциал мембраны.
- •29. Ионный транспорт в каналах. Понятие об энергетическом профиле канала. Уравнение силы тока, переносимого ионами.
- •30. Зависимость энергетического профиля ионного канала от заполнения канала, от биоэлектрических процессов. Селективность каналов.
- •31. Общие свойства ионных каналов нервных волокон. Na-канал, к-канал, их селективность.
- •32. Функционирование ионных каналов в зависимости от от внешнего электрического потенциала, понятие воротного устройства.
- •33. Активный транспорт ионов. Перенос ионов за счет энергии атф. Схема работы каналов.
- •34. Сопряжение ионообменных процессов с гидролитическим расщеплением молекулы атф. Конформационные переходы Na, k- атФазы.
- •35. Транспорт протонов в энергосберегающих мембранах. Образование градиента электрохимических потенциалов в биомембранах.
- •36. Потенциал покоя. Формула Нерста для мембранного потенциала. Уравнение Томаса.
- •37. Потенциал действия. Мембранный потенциал и изменение ионной проницаемости мембраны. Описание ионных токов в модели Ходжкина-Хаксли.
- •38. Образование воротных токов в мембранах нервных волокон. Распространение электрического импульса в нервных волокнах.
- •39.Фотопревращение бактериородопсина. Строение бактериородопсина, конформационные переходы молекулы при поглощении кванта света. Внутримолекулярный перенос протона.
- •40. Фотоизомеризация родопсина в фоторецептурной мембране зрительных клеток позвоночных. Проницаемость мембраны и светоиндуцированный электрический сигнал
- •Фоторегуляторные и фотодеструкционные процессы Фоторегуляторные реакции
- •41. Ультрафиолетовое излучение и фотодеструкционные процессы в днк: фотоизомеризация, фотогидротация, образование пиримидиновых аддукатов. Механизмы фотореактивации.
- •42.Действие ультрафиолетового излучения на белки, на биомембраны.
27. Индуцированный ионный тран-т через мембрану.Затраты энерг. По формуле Борна.
Закономерности транспорта ионов через мембраны изучены в опытах с искусственными бислойными липидными мембранами (БЛМ).
Формула Борна оценивает затраты энергии для проникновения иона в неполярную фазу БЛМ:
![]()
где z – валентность иона, е – электрический заряд, r – радиус, εм – диэлектрическая проницаемость мембраны, εв - диэлектрическая проницаемость воды.
Рассчитанные по данному уравнению значения свободной энергии для перехода К+ из воды в неполярный растворитель с εм = 2 составляет большую величину (250-350 кДж/моль). Это создает барьер для прохождения гидратированного иона через гидрофобную часть липидного бислоя.
Энергия перехода иона в мембрану снижается с увеличением радиуса иона. Крупные органические молекулы проникают легче через БЛМ, чем катионы щелочных металлов.
28. Перенос ионов ионоформами. Затраты энергии для переноса комплекса «ион-ионофор». Избирательность ионных переносчиков. Электрические свойства мембраны и движение заряженных комплексов «ион-переносчик».
Величина энергетического барьера в мембране уменьшается, а следовательно, проницаемость мембраны для иона возрастает не только при увеличении его радиуса, но и при приближении значений εм к εв. На этих физических принципах основан перенос ионов ионофорами.
Ионофоры с ионом образуют комплексы большого размера – переносчики – либо формируют пору в мембране, заполненную водой, - каналы.
Перенос иона через мембрану включает стадии:
образование комплекса иона с ионофором на одной стороне мембраны,
перемещение комплекса через мембрану,
освобождение иона на другой стороне,
возвращение ионофора.
Возможны две схемы работы ионофора:
малая «карусель», когда ионофор не выходит из мембраны;
большая «карусель», когда ионофор проходит мембрану насквозь, а образование и распад комплексов протекает в неперемешиваемых слоях около мембраны.
Формула Борна описывает затраты энергии комплекса иона с радиусом r с переносчиком радиуса b c диэлектрической проницаемостью мембраны εм:
![]()
где εк эффективная диэлектрическая проницаемость внутренней сферы комплекса.
Энергия комплекса ион-переносчик значительно меньше энергии иона. Для заряженного комплекса радиусом 1 нм свободная энергия перехода из воды в мембрану составляет около 15 кДж/моль в отличие от соответствующих энергии дегидратации свободных ионов с радиусом 0,1-0,15 нм.
Ионными переносчиками являются макроциклические антибиотики, синтетические макроциклические комплексоны. Некоторые из них – нейтральные ионофоры – не содержат ионизируемых групп. Комплексоны, образуемые макроциклическими соединениями с катионами щелочных металлов, несут положительный заряд. Перенос иона происходит в виде заряженного комплекса. Катион входит во внутреннюю полость молекулы ионофора, структура стабилизируется за счет взаимодействия иона с 6-8 полярными группировками (эфирные, амидные или сложноэфирные). Ион металла экранирован от взаимодействия с растворителем.
Высокая избирательность валомицитина к образованию комплекса с К+ достигается хорошим стерическим соответствием К+ и внутренней полости валомицитина, которую образуют СО-группы. К+ полностью дегидратируется, а карбонильные (СО-) диполи заменяют гидратную оболочку (рис.5.2).
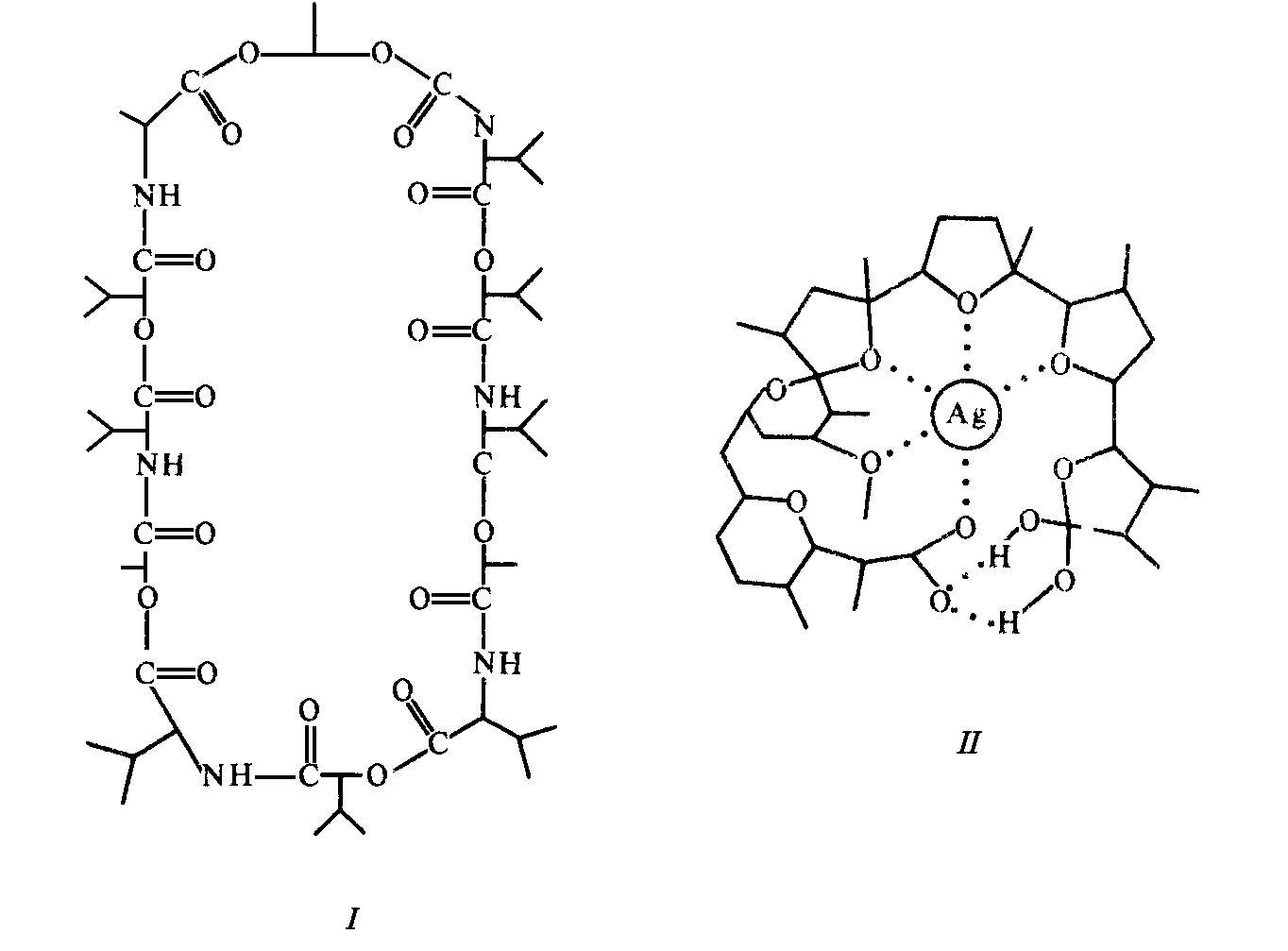
Рис. 5.2. Строение некоторых ионофоров: I — молекула валиномицина, II — система металл-кислородных и водородных связей в серебряной соли нигерицина (Рубин, 2004).
Na+ может поместиться полости валомицитина, но вследствие меньшего радиуса не взаимодействует с кислородом карбонильных групп. Энергия связывания его с водой выше энергии связывания с переносчиком.
Валомицитин обладает хорошей селективностью, переносит порядка 104 ионов/с.
Некоторые ионофоры, например нигерицин и гризориксин имеют нециклическое строение, но связывают ионы, образуя комплексную молекулу в свернутой, псевдоциклической конформации (рис. 5.2). Будучи слабыми кислотами нигерицин и его аналоги переносят два типа ионов, а при наличии градиента индуцируют обменный транспорт (обмен Н+ на К+).
Молекулы ионофора могут образовать комплекс, имеющий водную пору – канал.
Каналообразующие соединения - грамицидин А, аламетицин, амфотерицин, моназомицин и полиеновые антибиотики – обладают сродством к водной и органической фазам, поэтому образуют водную пору и сорбируются на мембране.
Полярные или заряженные группы молекулы закреплены на одной из сторон мембраны. Рассмотрим каналы, образованные грамицидином А.
Пептидная часть молекулы образована 15-ю гидрофобными аминокислотами, у которых чередуются L- и D-конфигурации. На конце молекулы формильная группа, на другом этаноламин. Каждый горизонтальный ряд аминокислот соответствует примерно одному повороту спирали, диагональные линии — пептидным связям, соединяющим отдельные витки спирали (рис. 5.3).
В мембране молекула сворачивается в спиралевидную структуру – полупору, формируя полый цилиндр длиной 3 нм и диаметром 0,5-0,8 нм. Непроводящее состояние молекулы не имеет внутренней полости. Равновесие между формами смещается под действием внешнего электрического поля. Грамицидин в субмолекулярных концентрациях повышает проводимость БЛМ в 106-108 раз.
