
- •21. Механические и конформационные свойства мембран. Фазовые переходы.
- •Раздел 5. Транспорт веществ и биоэлектрогенез
- •22. Транспорт неэлектролитов через мембраны. Диффузия: движущая сила. Закон Фика. Понятие об облегчённой диффузии.
- •23. Транспорт ионов через мембрану. Механизмы и движущая сила пассивного транспорта. Уравнение электрохимического потенциала.
- •24. Энергия иона и причины её понижения при транспорте через биомембраны.
- •26. Электродиффузная теория транспорта ионов через мембрану. Уравнение Нерста-Планка для потока ионов через мембрану. Уравнение Гольдмана.
- •27. Индуцированный ионный тран-т через мембрану.Затраты энерг. По формуле Борна.
- •25. Электрические свойства биомембран и транспорт ионов. Понятие о двойном электрическом слое. Плотность распределения ионов в зависимости от расстояния. Электрокинетический потенциал мембраны.
- •29. Ионный транспорт в каналах. Понятие об энергетическом профиле канала. Уравнение силы тока, переносимого ионами.
- •30. Зависимость энергетического профиля ионного канала от заполнения канала, от биоэлектрических процессов. Селективность каналов.
- •31. Общие свойства ионных каналов нервных волокон. Na-канал, к-канал, их селективность.
- •32. Функционирование ионных каналов в зависимости от от внешнего электрического потенциала, понятие воротного устройства.
- •33. Активный транспорт ионов. Перенос ионов за счет энергии атф. Схема работы каналов.
- •34. Сопряжение ионообменных процессов с гидролитическим расщеплением молекулы атф. Конформационные переходы Na, k- атФазы.
- •35. Транспорт протонов в энергосберегающих мембранах. Образование градиента электрохимических потенциалов в биомембранах.
- •36. Потенциал покоя. Формула Нерста для мембранного потенциала. Уравнение Томаса.
- •37. Потенциал действия. Мембранный потенциал и изменение ионной проницаемости мембраны. Описание ионных токов в модели Ходжкина-Хаксли.
- •38. Образование воротных токов в мембранах нервных волокон. Распространение электрического импульса в нервных волокнах.
- •39.Фотопревращение бактериородопсина. Строение бактериородопсина, конформационные переходы молекулы при поглощении кванта света. Внутримолекулярный перенос протона.
- •40. Фотоизомеризация родопсина в фоторецептурной мембране зрительных клеток позвоночных. Проницаемость мембраны и светоиндуцированный электрический сигнал
- •Фоторегуляторные и фотодеструкционные процессы Фоторегуляторные реакции
- •41. Ультрафиолетовое излучение и фотодеструкционные процессы в днк: фотоизомеризация, фотогидротация, образование пиримидиновых аддукатов. Механизмы фотореактивации.
- •42.Действие ультрафиолетового излучения на белки, на биомембраны.
35. Транспорт протонов в энергосберегающих мембранах. Образование градиента электрохимических потенциалов в биомембранах.
Транспорт протонов. Перенос электронов в энергосберегающих мембранах митохондрий, хлоропластов и бактерий сопровождается трансмембранным переносом Н+ и образованием градиента электрохимического потенциала этого иона ∆μН+, который включает электрический (мембранный потенциал) и концентрационный (градиент рН) компоненты:
∆μН+ = RT ln(ci / co) + zF (φi – φo) = zF ∆ φ – 2,3RT ∆pH.
Где i и o относятся к растворам, находящимся внутри и снаружи замкнутой мембранной системы. ∆ φ – разность потенциалов на мембране.
Перенос Н+ через мембраны может осуществляться транспортными механизмами трех типов.
Подвижные переносчики протонов, например, пластохинон в фотосинтетической тилакоидной мембране хлоропластов (рис. 5.16).
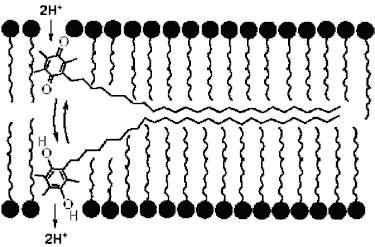
Рис. 5.16. Одна из возможных схем расположения молекулы пластохинона в мембране показана на рисунке (Тихонов, 1996)
Конформационные переходы мембранного белка при связывании протона на одной стороне мембраны и депротонировании белка с другой стороны, сопряженные с поворотом макромолекулы в мембране (рис. 5.17).
Протоны могут трансформироваться по специализированным структурам – Н+ -каналам, представляющим полость, образованную полярными группами белков.
Протонный канал – компонент всех Н+-АТФаз, представляет собой узкую полость, образованную полярными группами белка. По нему протоны поступают к каталитическому центру транспортной системы, в котором осуществляется сопряжение переноса Н+ с реакциями синтеза-гидролиза АТФ. Таким образом, основными узлами Н+-насосов являются протонный канал и активный центр.
В мембранах системы водородных связей, по которым транспортируются протоны, образованы полярными группами, не участвующими в формировании Н-связей α-спирали полипептидной цепи:
Сначала происходит перескок протона от группы к группе (рис. 5.18), происходит дополнительное смещение заряда, а затем поворот группы, в результате которого система связей возвращается в исходное состояние.
В результате поворота химической группы образуется конфигурация, не допускающая возврата протона в начальное состояние.
Лишь некоторая часть от полного заряда протона смещается за счет его перескока, остальная часть заряда смещается за счет поворота полярной группы. Благодаря этому существенно снижен энергетический барьер переноса Н+ через мембрану.
Характерные подвижности ионного и поворотного дефектов составляют 10-3 и 10-4 см/В.с. Время миграции дефектов через мембрану толщиной 5 нм не превышает 0,25 мкс и 2,5 мкс соответственно.
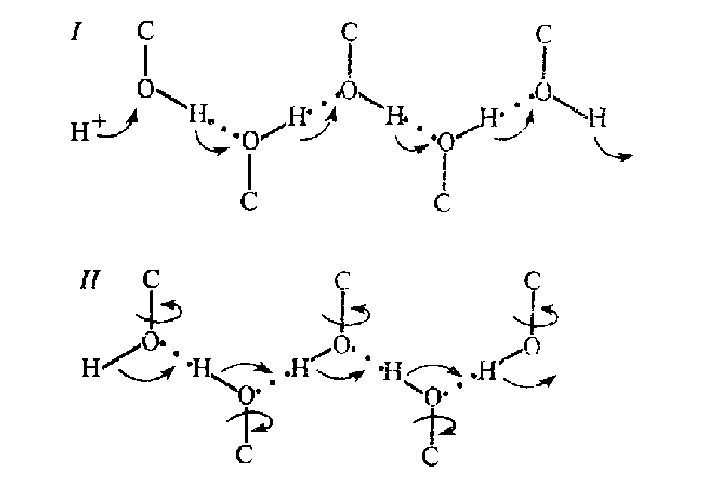
Рис. 5.18. Проведение протона по цепи Н-связей: I — стадия перескока протона, II — стадия поворота групп (миграция поворотного дефекта)
В общем виде систему активного транспорта рассматривают как трансмембранный канал с большим числом участков связывания Н+, в котором транслокация протонов происходит за счет последовательных перескоков Н+ между участками связывания. Такой ионный канал может работать как ионный насос, если структура энергетических барьеров претерпевает динамические изменения за счет энергообеспечивающей реакции, например изменяются константа диссоциации протон-связывающих участков канала и высота соседних барьеров. В этом случае протон будет освобождаться преимущественно с одной стороны мембраны, а поглощаться— с другой.
На рис. 5.19 показаны профили потенциальной энергии Н+ для основного и энергизованного состояния канала, формируемого бактериородопсином в мембранах галофильных бактерий. В основном состоянии протон занимает наиболее глубокую потенциальную яму, соответствующую главному участку связывания. Этот участок доступен с цитоплазматической стороны мембраны, но отделен от внешней среды высоким энергетическим барьером. При поглощении бактериородопсином кванта света энергетический уровень участка связывания и высота барьеров изменяются таким образом, что протон высвобождается во внешний раствор. Изменение высоты активационных барьеров, обусловленное небольшими изменениями конформации Н+ канала, может быть связано с изменением сродства к протону аминокислотных остатков переносчиков Н+.

Рис. 5.19. Энергозависимые изменения структуры барьеров в ионном канале активной транспортной системы: i — потенциальный минимум (Рубин, 2004)
