
- •4. Учитель и его назначение в обществе. Психология педагогической деятельности. Педагогические способности и индивидуальный стиль деятельности учителя.
- •Методика.
- •6 ) Энергия электростатического поля.
- •10 Постоянный ток в металлах.
- •7) Опыты Толмена и Стюарта.
- •9) Закон Био-Савара-Лапласса.
- •10.(16). Магнитные свойства вещества. Природа диа- , пара- , ферромагнетизма. Переменный ток. Сопротивление, емкость, индуктивность цепи переменного тока.
- •12.(14) .Интерференция волн
- •13.(13). Дифракция света. Принцип Гюйгенса-Френеля. Дифракция Френеля и Фраунгофера. Дифракционная решетка. Дифракция рентгеновских лучей.
- •14.(12.) Поляризация света. Методы получения поляризованного света законы Брюстера и Малюса. Рассеяние света. Закон Релея. Цвет неба и зорь.
- •Проблемы перехода к двенадцатилетнему сроку обучения. Единый государственный экзамен.
- •19.(7). Волновые свойства частиц. Опыты Девисона и Джермера. Опыт Томсона и Тартаковского.
- •Этапы возникновения девиантного поведения. Возникновение девиации - длительный процесс, проходящий несколько стадий
- •4.3.3. Линейчатые спектры
- •2.(24). 1.Внутренняя энергия.
- •2.Работа.
- •3.Теплота.
- •Теплоемкость.
Теплоемкость.
Теплоемкостью тела называется физическая величина, равная отношению
![]() ,
,
![]() .
.
Теплоемкость одного моля – молярная теплоемкость
![]() .
.
Т.к.
![]() - функция процесса
- функция процесса
 ,
то
,
то
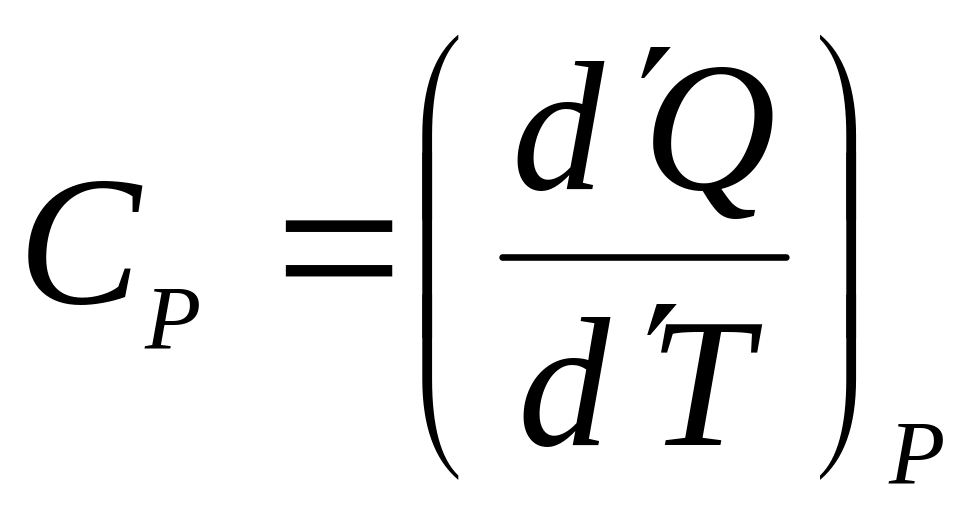 .
.
Учитывая
![]()
![]() ;
;
![]()
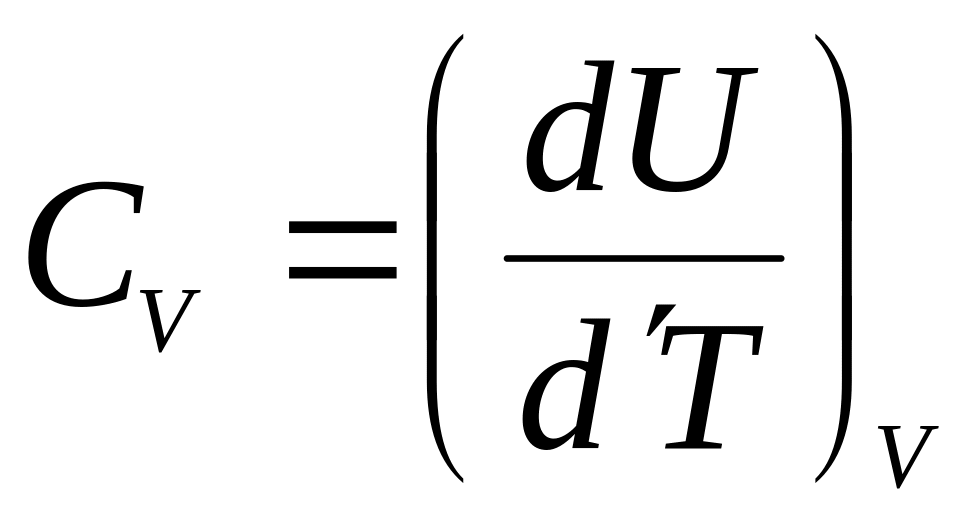 ;
;
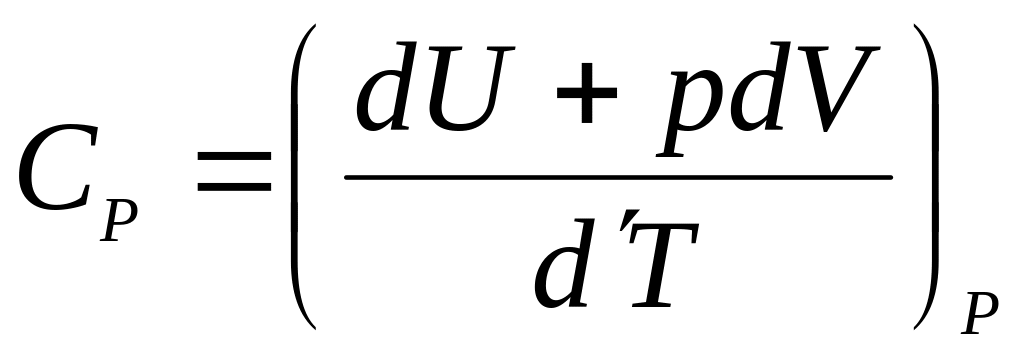
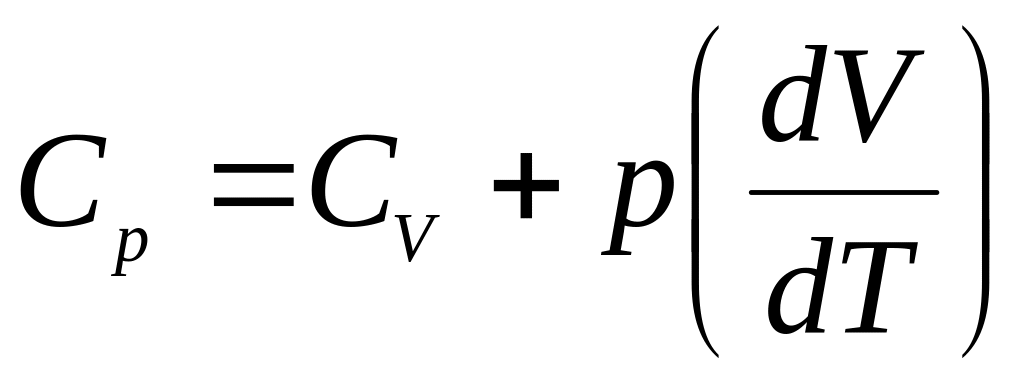
![]()
![]()
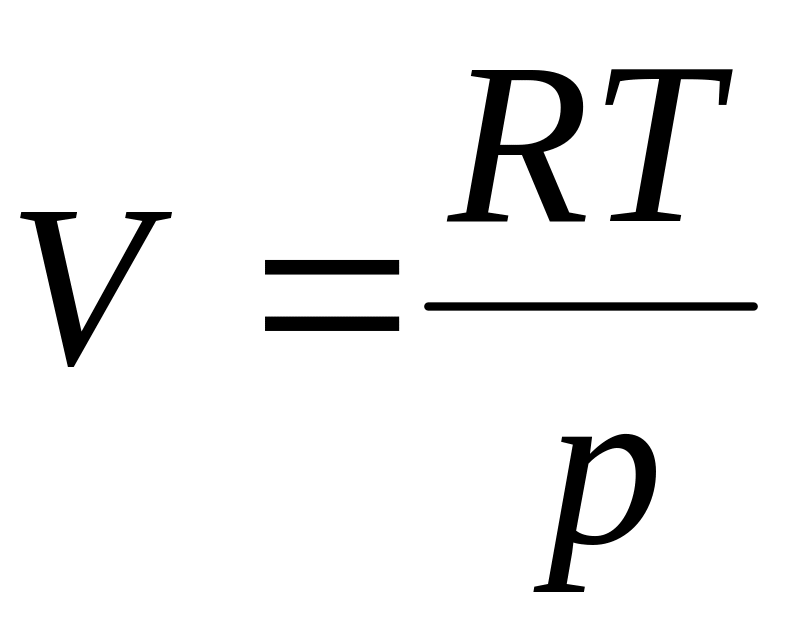
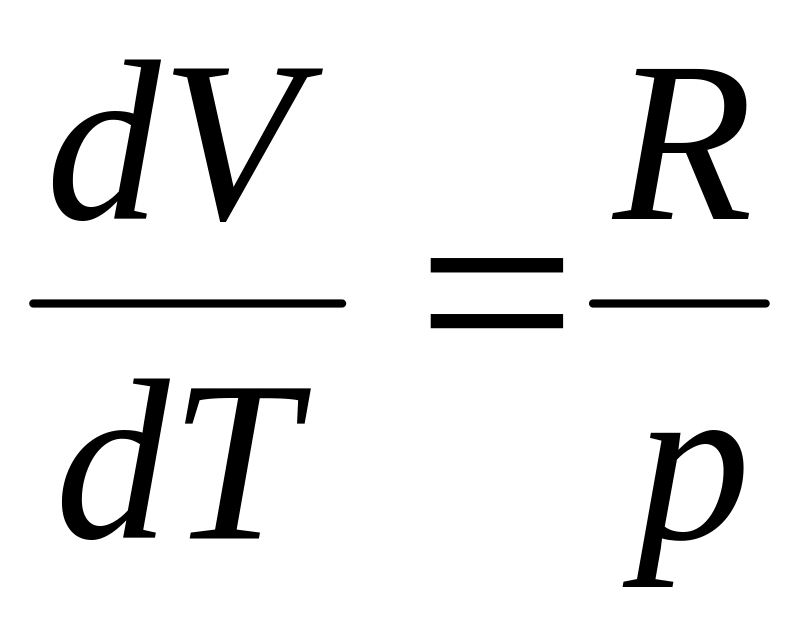 .
.
![]() -
формула Майера.
-
формула Майера.
Т.о.
задача вычисления теплоемкости сводится
к нахождению
![]() .
.
![]() .
.
Одноатомный газ
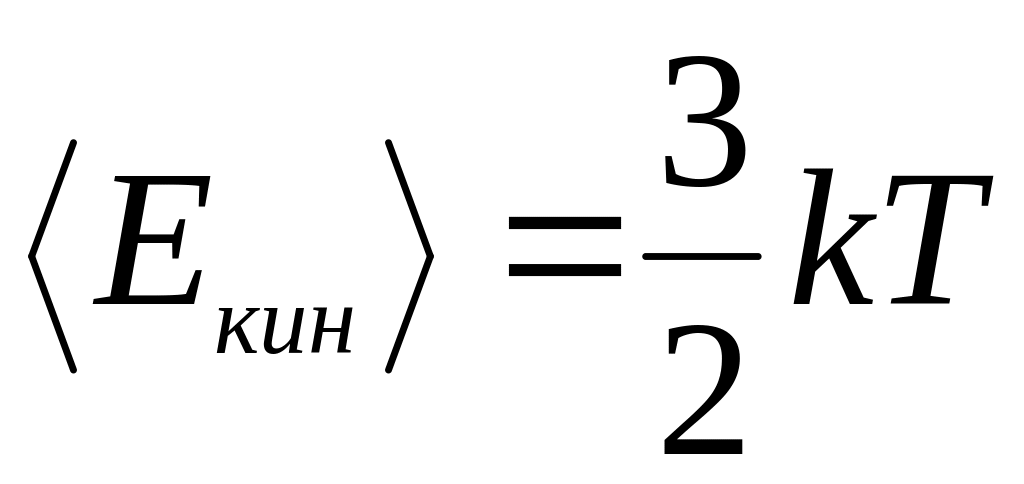
Для
одного моля:
![]()
![]() ,
отсюда
,
отсюда
![]() .
.
Двухатомный газ (О2, N2, Cl2, СО и т.д.).
(модель жесткой гантели).
Полное число степеней свободы :
![]() .
.
Тогда
![]() ,
то
,
то
![]()
![]() ;
;
![]() .
.
Многоатомные газы (H2O, CH4, C4H10O и т.д.).
![]() ;
;
![]() ;
;
![]() ;
;
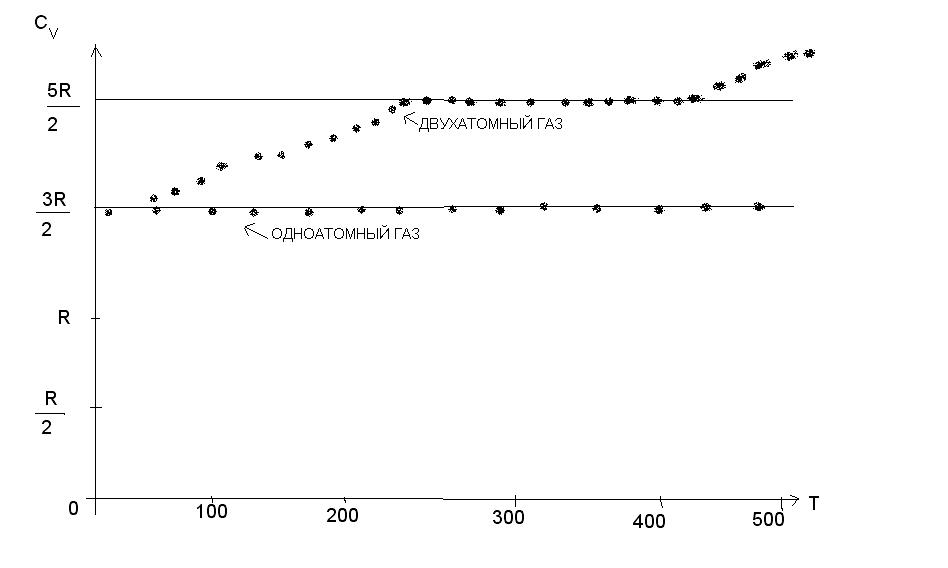 Сравним
теоретические данные с опытными.
Сравним
теоретические данные с опытными.
Видно,
что
![]() 2-х атомных газов равняется
2-х атомных газов равняется
![]() ,
но изменяется при низких температурах
вопреки теории теплоемкости.
,
но изменяется при низких температурах
вопреки теории теплоемкости.
Такой
ход кривой
от
![]() свидетельствует о «замораживании»
степеней свободы. Наоборот при больших
температурах подключаются дополнительные
степени свободы
эти данные ставят под сомнение теорему
о равномерном распределении. Современная
физика позволяет объяснить зависимость
от
используя квантовые представления.
свидетельствует о «замораживании»
степеней свободы. Наоборот при больших
температурах подключаются дополнительные
степени свободы
эти данные ставят под сомнение теорему
о равномерном распределении. Современная
физика позволяет объяснить зависимость
от
используя квантовые представления.
Методика изучения идеального газа, его термодинамическое и статистическое описание.
Существуют два определения понятия идеального газа: термодинамическое и молекулярно-кинетическое. В термодинамике под идеальным газом понимают газ, у которого при изотермическом процессе при постоянной массе давление обратно пропорционально его объему (или газ, в точности подчиняющийся газовым законам).
С молекулярно-кинетической точки зрения идеальный газ - этот газ, молекулы которого представляют собой материальные точки, не взаимодействующие друг с другом на расстоянии, но взаимодействующие при столкновениях по закону абсолютно упругого удара. Такое определение модели вполне правомерно, так как силы взаимодействия между молекулами газа в десятки миллионов раз меньше, чем в жидкостях и твердых телах, т. е. ими можно пренебречь. Принимая молекулы газа за материальные точки, исходят из того, что их суммарный объем много меньше объема сосуда и его можно не учитывать. Это связано с тем, что расстояния между молекулами газов в десятки раз больше, чем между молекулами жидкостей и молекулами твердых тел. Следует иметь в виду, что принятая модель «идеальный газ» «работает» только тогда, когда газ находится в равновесном состоянии. Если газ находится в неравновесном состоянии, то моделью идеального газа пользоваться нельзя. Это следует из тех соображений, что длина свободного пробега молекул газа обратно пропорциональна концентрации n0 молекул и их размеру:
l=1/r0n0
где
r0
- эффективный
радиус молекулы. По определению идеального
газа эффективный радиус молекулы равен
нулю (г0
= 0), тогда
длина свободного пробега молекулы
стремится к бесконечности
(l
→![]() ),
т. е. молекулы газа друг с другом не
сталкиваются и равновесное состояние
не наступает. Однако газ, находящийся
в неравновесном
состоянии, будучи предоставленным
самому себе, приходит
в равновесное состояние в результате
столкновения молекул
друг с другом, причем, как следует из
опыта, в газах тепловое равновесие
наступает быстро. Следовательно, в
процессе установления теплового
равновесия пренебрегать размерами
молекул газа
нельзя.
),
т. е. молекулы газа друг с другом не
сталкиваются и равновесное состояние
не наступает. Однако газ, находящийся
в неравновесном
состоянии, будучи предоставленным
самому себе, приходит
в равновесное состояние в результате
столкновения молекул
друг с другом, причем, как следует из
опыта, в газах тепловое равновесие
наступает быстро. Следовательно, в
процессе установления теплового
равновесия пренебрегать размерами
молекул газа
нельзя.
Но после установления теплового равновесия столкновения молекул уже ничего не меняют, поэтому можно считать, что в состоянии теплового равновесия молекулы не имеют размеров и не взаимодействуют.
Модель «идеальный газ» имеет определенные границы применимости: она не применима при высоких давлениях и низких температурах. Если газ сжать, то увеличится его плотность и уменьшатся расстояния между молекулами, поэтому размерами молекул уже нельзя пренебречь, а давление газа будет зависеть не только от ударов молекул, но и от их взаимодействия. Из эксперимента известно, что при давлении газа порядка 108 Па наблюдаются существенные отклонения от закона Бойля - Мариотта. То же самое происходит и при понижении температуры.
По программе общеобразовательной средней школы с понятием идеального газа учащихся впервые знакомят в старших классах. В зависимости от выбранной последовательности изучения материала школьникам дают либо термодинамическое определение понятия идеального газа, либо молекулярно-кинетическое.
Если сначала изучают экспериментальные газовые законы, то вводят термодинамическое понятие идеального газа, поскольку возникает необходимость показать границы их применимости. Молекулярно-кинетическое понятие идеального газа целесообразно рассмотреть сразу же после введения термодинамического определения. Это можно сделать, так как раздел начинают с темы «Основы молекулярно-кинетической теории» и учащиеся владеют необходимыми знаниями; при таком подходе и проявляется единство феноменологического и статистического методов изучения явлений и обеспечивается лучшее понимание их сущности.
Если принят дедуктивный подход к изучению газовых законов, то выводу основного уравнения молекулярно-кинетической теории газов предшествует построение модели идеального газа. В дальнейшем при выводе частных газовых законов обсуждают границы их применимости. Важно обратить внимание школьников на признаки понятия идеального газа, на границы его применимости и на непротиворечивость термодинамического и молекулярно-кинетического толкований модели.
Хотя восприятие возникает в результате непосредственного воздействия раздражителя на рецепторы, персептивные образы, всегда имеют определенное смысловое значение. Восприятие у человека теснейшим образом связано с мышлением, с пониманием сущности предмета. Сознательно воспринять предмет — это значит мысленно назвать его, т. е. отнести воспринятый предмет к определенной группе, классу предметов, обобщить его в слове.
Даже при виде незнакомого предмета мы пытаемся уловить в нем сходство со знакомыми нам объектами, отнести его к некоторой категории. Восприятие не определяется просто набором раздражителей, воздействующих на органы чувств, а представляет динамический поиск наилучшего толкования, объяснения имеющихся данных. Показательны с этой точки зрения так называемые двусмысленные рисунки, в которых попеременно воспринимаются то фигура, то фон {рис. 12). В этих рисунках выделение объекта восприятия связано с его осмысливанием и называнием (два профиля и ваза).
Подводя итог, можно заключить, что восприятие—активный процесс, в ходе которого человек производит множество перцептивных действий для того, чтобы сформировать адекватный образ предмета. Активность восприятия состоит прежде всего в участии эффекторных (двигательных) компонентов анализаторов в процессе восприятия (движения руки при осязании, движения глаза в зрительном восприятии и т. п.). Кроме того, необходима и активность на макроуровне, т. е. возможность в процессе восприятия активно перемещать свое тело.
Таким образом, при восприятии какого-либо предмета активизируются и следы прошлых восприятий. Поэтому естественно, что один и тот же предмет может восприниматься и воспроизводиться по-разному различными людьми.
Таким образом, восприятие зависит от прошлого опыта субъекта. Чем богаче опыт человека, чем больше у него знаний, тем богаче его восприятие, тем больше он увидит в предмете.
Содержание восприятия определяется и поставленной перед человеком задачей, и мотивами его деятельности. Например, слушая в исполнении оркестра музыкальное произведение, мы воспринимаем всю музыкальную ткань в целом, не выделяя в ней звучания каждого инструмента. Только поставив цель выделить звук какого-либо инструмента, это удается сделать. Тогда звук этого инструмента выступит на передний план, станет объектом восприятия, все же остальное составит фон, восприятия.
Существенным фактором, влияющим на содержание восприятия, является установка субъекта. Описано очень много случаев, когда восприятие объекта искажалось под влиянием установки, подобно тому как это произошло в комедии Н. В. Гоголя «Ревизор» при появлении Хлестакова в городе, ожидавшем приезда высокопоставленного лица.
В процессе восприятия участвуют и эмоции, которые могут изменять содержание восприятия. Важная роль эмоциональных реакций в восприятии подтверждается целым рядом различных экспериментов.
Все сказанное о влиянии на восприятие прошлого опыта субъекта, мотивов и задач его деятельности, установки, эмоционального состояния (сюда же можно отнести и убеждения, мировоззрение человека, его интересы и т, п.) показывает, чт^ восприятие — активный процесс, которым можно управлять.Восприятие — это система перцептивных действий, и овладение ими требует специального обучения и практики.
