
- •4. Учитель и его назначение в обществе. Психология педагогической деятельности. Педагогические способности и индивидуальный стиль деятельности учителя.
- •Методика.
- •6 ) Энергия электростатического поля.
- •10 Постоянный ток в металлах.
- •7) Опыты Толмена и Стюарта.
- •9) Закон Био-Савара-Лапласса.
- •10.(16). Магнитные свойства вещества. Природа диа- , пара- , ферромагнетизма. Переменный ток. Сопротивление, емкость, индуктивность цепи переменного тока.
- •12.(14) .Интерференция волн
- •13.(13). Дифракция света. Принцип Гюйгенса-Френеля. Дифракция Френеля и Фраунгофера. Дифракционная решетка. Дифракция рентгеновских лучей.
- •14.(12.) Поляризация света. Методы получения поляризованного света законы Брюстера и Малюса. Рассеяние света. Закон Релея. Цвет неба и зорь.
- •Проблемы перехода к двенадцатилетнему сроку обучения. Единый государственный экзамен.
- •19.(7). Волновые свойства частиц. Опыты Девисона и Джермера. Опыт Томсона и Тартаковского.
- •Этапы возникновения девиантного поведения. Возникновение девиации - длительный процесс, проходящий несколько стадий
- •4.3.3. Линейчатые спектры
- •2.(24). 1.Внутренняя энергия.
- •2.Работа.
- •3.Теплота.
- •Теплоемкость.
Этапы возникновения девиантного поведения. Возникновение девиации - длительный процесс, проходящий несколько стадий
Первая стадия - это возникновение предпосылок отклонений, которые формируются преимущественно в дошкольный период. Доминанты отклонений - недостаточное развитие индивидуальных психологических качеств (внимание, усидчивость, эмоциональная устойчивость), слабая психолого-педагогическая подготовка к школе (искажённая информация о ней, отсутствие элементарных учебных навыков)
Вторая стадия - появление начальных форм отклонений в поведении чаще всего возникает у учащихся начальных классов. Доминанты отклонений - отсутствие успеха в различных видах деятельности, неумение выполнять требования педагога, слабость внутригрупповых отношений.
Третья стадия-стабилизация неблагоприятных тенденций в поведении школьника. Возникает преимущественно у младших и средних подростков (10-13 лет), проступки связаны с нарушением норм жизни класса, школы носят чаще всего ситуативный характер, а в определённых ситуациях, преднамеренный характер.
Четвёртая стадия-возникновение устойчивых признаков асоциального поведения, характерны для старших подростков (14-17 лет), проступки носят, как правило, преднамеренный характер. Подобные состояния являются серьёзной предпосылкой возможных правонарушений и преступлений. Классный руководитель своей целью должен видеть выявление проблем, возникающих у ребенка или группы детей в поведении, прогнозирование развития личности ребенка и его поведенческих проявлений, возможного развития группы школьников и организацию работы по профилактике и коррекции девиантного поведения школьников.
Основные задачи, которые решают специалисты комплексной группы на уровне школы, можно сформулировать следующим образом:
Классный руководитель:
является связующим звеном в комплексной группе специалистов по организации профилактической и коррекционной работы с детьми и подростками;
делает первичный запрос специалистам и дает первичную информацию о ребенке;
организует и координирует комплексную работу по профилактике и коррекции девиантного поведения школьников. Социальный педагог:
изучает жизнедеятельность ребенка вне школы;
организует профилактическую и коррекционную работу в микрорайоне;
поддерживает детей, попавших в экстремальные ситуации;
оздоровление психосоциальной среды развития ребенка;
просветительская деятельность в вопросах обучения и воспитания, половозрастной специфики соматического и психического развития детей и подростков, направленная на повышение уровня компетентности взаимодействующих с ребенком взрослых;
предупреждение психологических перегрузок в процессе обучения, оказывающих негативное влияние на психику ребенка;
проведение социального закаливания детей и подростков с целью подготовки их к стрессовым ситуациям, обучение их рациональным способам снятия психо-эмоционального напряжения в проблемных ситуациях;
психолого-педагогическое изучение и отслеживание ребенка на протяжении всего периода его обучения в школе, своевременное выявление состояния учащихся, нервно-психических и психосоматических нарушений. Организация психолого-педагогических консилиумов с целью анализа поведения и развития школьников, условий для более полного раскрытия их возможностей;
совместные семинары для учащихся и их родителей, посвященные проблемам девиантного поведения. Формы совместной коррекционной работы:
информирование учащихся и их родителей о тех видах помощи, которую могут получить школьники и их родители в школе и учреждениях, оказывающих различные виды помощи вне школы;
проведение психолого-педагогических практикумов с детьми и их родителями, где обсуждаются вопросы отклонения в поведении, их причины, пути преодоления и способы коррекции;
выявление причин девиантного поведения конкретного ученика или группы школьников;
разработка программ коррекционной работы, как на индивидуальном, так и на групповом уровне;
взаимодействует с центрами психологической поддержки и реабилитации детей и подростков с девиантным поведением. Психолог:
изучает личность учащегося и коллектива класса; анализирует адаптацию ребенка в среде; выявляет дезадаптированных учащихся;
изучает взаимоотношения детей с взрослыми и сверстниками;
подбирает пакет диагностических методик для организации профилактической и коррекционной работы;
выявляет и развивает интересы, склонности и способности школьников;
осуществляет психологическую поддержку нуждающихся в ней детей.
Школьный врач:
исследует физическое и психическое здоровье учащихся; организует помощь детям, имеющим проблемы со здоровьем;
разрабатывает рекомендации педагогам по организации работы с детьми, имеющими различные заболевания;
взаимодействует с лечебными учреждениями. Исходя из решаемых задач, можно назвать и общие формы профилактической и коррекционной работы на уровне школы.
Организуя профилактическую работу, можно использовать следующие формы:
комплексные консультации специалистов для школьников и их родителей, проводимые на основании данных социально-психологической, психолого-педагогической и медицинской диагностики, как отдельных учащихся, так и класса в целом;
Эффективность реализации указанных задач комплексной группой специалистов на уровне школы и организация профилактической и коррекционной работы с девиантным поведением детей и подростков во многом зависит от грамотно организованного процесса изучения личности ребенка и его ближайшего окружения. Результаты такого изучения должны быть основой разработки программ профилактической и коррекционной работы с девиантным поведением школьников. Изучение личности школьников проводится с использованием карты личности школьника.
«Карта личности школьника» заполняется классным руководителем, социальным педагогом, психологом, школьным врачом. Оценка предложенных качеств личности и условий ближайшего окружения происходит на основе наблюдения за школьником, изучения его взаимоотношений со сверстниками, друзьями, учителями, родителями, а также в результате бесед и сбора независимых характеристик, которые даются учащемуся его друзьями, товарищами по классу, педагогами и другими взрослыми. На основании заполненных карт организуются группы детей и их родителей, с которыми необходимо проводить профилактическую работу, и группы, требующие коррекционной работы, а также выделяются дети, нуждающиеся в индивидуальной профилактической и коррекционной работе.
21.(5) 5. Атом Водорода. Модель Бора и его историческая роль. Спектр излучения атомарного водорода. Состояние электрона в многоэлектронном атоме(квантовые числа). Принцип Паули. Периодич-сист. эл-в Менделеева.
Н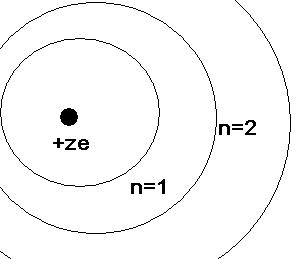 а
основе планет. модели атома Бор разработал
теорию атома водорода и атомов
изоэлектронного ряда водорода
(изоэлектронный ряд водорода – это
атомы или ионы имеющие в электронной
оболочке 1 единственный электрон). Теория
Бора позволила объяснить известные к
тому времени спектральные закономерности
этих атомов и предсказать другие спектр.
закон-ти которые были обнаружены позднее.
В основе теории Бора лежат несколько
постулатов. Во-первых предполагается,
что 1 единственный электрон данного
атома совершает движение по круговой
орбите.
I-постулат
Бора
утверждает, что устойчивыми орбитами
на которых и может находиться электрон
явл-ся круговой орбитой, удовлет-щей
условиям
а
основе планет. модели атома Бор разработал
теорию атома водорода и атомов
изоэлектронного ряда водорода
(изоэлектронный ряд водорода – это
атомы или ионы имеющие в электронной
оболочке 1 единственный электрон). Теория
Бора позволила объяснить известные к
тому времени спектральные закономерности
этих атомов и предсказать другие спектр.
закон-ти которые были обнаружены позднее.
В основе теории Бора лежат несколько
постулатов. Во-первых предполагается,
что 1 единственный электрон данного
атома совершает движение по круговой
орбите.
I-постулат
Бора
утверждает, что устойчивыми орбитами
на которых и может находиться электрон
явл-ся круговой орбитой, удовлет-щей
условиям
![]() ,
где n=1,2,3…
L
– вектор момента импульса мат. точки.
,
где n=1,2,3…
L
– вектор момента импульса мат. точки.
![]()
![]() т.к. круговая орбита то
т.к. круговая орбита то
![]()
![]()
![]() ;
II-
постулат Бора
утверждает, что движущийся ускоренно
по круговой орбите электрон не излучает
эл/магн. волну и не теряет свою энергию.
Равномерное движение по круговой орбите
является ускоренным (из кинематики).
III-
постулат Бора
утверждает, что излучение и поглощение
одной порции энергии или иначе кванта
энергии происходит при кратковременном
перескоке с одной боровской орбиты в
другую
;
II-
постулат Бора
утверждает, что движущийся ускоренно
по круговой орбите электрон не излучает
эл/магн. волну и не теряет свою энергию.
Равномерное движение по круговой орбите
является ускоренным (из кинематики).
III-
постулат Бора
утверждает, что излучение и поглощение
одной порции энергии или иначе кванта
энергии происходит при кратковременном
перескоке с одной боровской орбиты в
другую
![]() т.к.
т.к.
![]() и
и
![]()
![]() .
Из данных постулатов можно выйти на
спектры
.
Из данных постулатов можно выйти на
спектры
![]() ,
здесь q1=-e,
q2=ze,
а r
= rn.
Запишем ещё
,
здесь q1=-e,
q2=ze,
а r
= rn.
Запишем ещё
![]() и приравняем правые части, получим
и приравняем правые части, получим
![]() выразим
выразим
![]() разделим это выражение на
разделим это выражение на
![]() получим
получим
![]() где n=
1,2,3… Получается
где n=
1,2,3… Получается
![]() где n=
1,2,3…
где n=
1,2,3…
![]() то
то
![]() Выведем формулу для r
т.к.
то
Выведем формулу для r
т.к.
то
![]() т.е.
т.е.
![]()
![]() то
то
![]()
![]()
![]()

![]()
![]()
![]()
![]() для
водорода z=1,
то
для
водорода z=1,
то
![]() (*)
(*)![]() Для
описания состояния электрона в атоме
удобно использовать энергетическую
диаграмму. Из (*) следует: E1=-13,6
эв, то E2=-3,4
E1=-1,51эв
E1=-0,75эв
…если n=∞,
то E∞=0.
Энергетическая диаграмма – это одноосная
диаграмма min
энергия E1(см.
рис) Из III
постулата следует что
Для
описания состояния электрона в атоме
удобно использовать энергетическую
диаграмму. Из (*) следует: E1=-13,6
эв, то E2=-3,4
E1=-1,51эв
E1=-0,75эв
…если n=∞,
то E∞=0.
Энергетическая диаграмма – это одноосная
диаграмма min
энергия E1(см.
рис) Из III
постулата следует что
![]()
![]() заменим
заменим
![]()
![]() R-
постоянная Ридберга, R=1,09677*107
м-1.
По теории Бора электрон может находиться
в одной из стационарных орбит. Для того
чтобы атом начал испускать надо его
возбудить, т.е. передать какую-то энергию
за счет какого-то процесса. атом находится
в возб. сост. некоторое время
R-
постоянная Ридберга, R=1,09677*107
м-1.
По теории Бора электрон может находиться
в одной из стационарных орбит. Для того
чтобы атом начал испускать надо его
возбудить, т.е. передать какую-то энергию
за счет какого-то процесса. атом находится
в возб. сост. некоторое время
![]() .
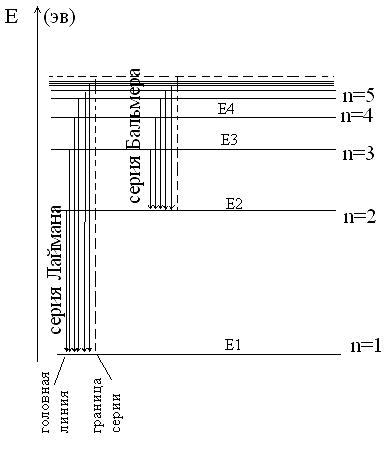
Излучение или поглощение происходит
при переходе с одной стац. орбиты в
другую (по III
постулату). Все переходы с какого-то
верхнего уровня на самый нижний формируют
серию спектральных линий, которая была
предсказана Бором и экспериментально
обнаружен в 1903 г. Лайманом, а все переходы
с верхних на второй уровень формирует
серию линий, часть которых находится в
видимой области – серия Бальмера.
Следующая серия была исследована Пашеном
в 1913 г. – серия Пашена. Для атомарного
водорода: серия Лаймана к→1
.
Излучение или поглощение происходит
при переходе с одной стац. орбиты в
другую (по III
постулату). Все переходы с какого-то
верхнего уровня на самый нижний формируют
серию спектральных линий, которая была
предсказана Бором и экспериментально
обнаружен в 1903 г. Лайманом, а все переходы
с верхних на второй уровень формирует
серию линий, часть которых находится в
видимой области – серия Бальмера.
Следующая серия была исследована Пашеном
в 1913 г. – серия Пашена. Для атомарного
водорода: серия Лаймана к→1
![]()
![]()
![]() ;
серия Бальмера: к→2
;
серия Бальмера: к→2
![]() ,
где 3646 – длина граничной линии, а вторая
головной. Серия Б. расположена в видимой
и ближней к ней УФ части спектра; серия
Пашена: к→3
,
где 3646 – длина граничной линии, а вторая
головной. Серия Б. расположена в видимой
и ближней к ней УФ части спектра; серия
Пашена: к→3
![]()
![]() Серия П. располагается в ближней ИК
области спектра и т.д. Рассмотрим вопрос
о заселенности энергетич. уровней, и о
невозможности получения серии Бальмера
поглощения в обычных условиях.
распределение ч-ц по эенргетич. уровням
выражается ф-лой Больцмана. если атом
возбужден, то
Серия П. располагается в ближней ИК
области спектра и т.д. Рассмотрим вопрос
о заселенности энергетич. уровней, и о
невозможности получения серии Бальмера
поглощения в обычных условиях.
распределение ч-ц по эенргетич. уровням
выражается ф-лой Больцмана. если атом
возбужден, то
![]() -
распределение по энергии Больцмана,
-
распределение по энергии Больцмана,
![]() Т=300 К, кТ=0,025 эВ Е2-Е1=10,2
эВ
Т=300 К, кТ=0,025 эВ Е2-Е1=10,2
эВ![]() т.о.
даже второй уровень практически не
заселен. Рассмотрим вопрос о поглощении
света. Серия Лаймана проявляется в
поглощении водородом находящемся при
комнатной температуре, потому что очень
велика заселенность нижнего Лаймановского
уровня, а это – осн. условие возможности
поглощения. Второе условие состоит в
том, чтобы в пучке излучения содержались
кванты соответствующих энергий. Серию
в которой проявляется поглощение
называют главн.серией. Серия Бальмера
не проявляется в поглощении при комн.
тем-рах, потому что бальмеровский уровень
при комнатной тем-ре оказ-ся незаселенным.
т.о.
даже второй уровень практически не
заселен. Рассмотрим вопрос о поглощении
света. Серия Лаймана проявляется в
поглощении водородом находящемся при
комнатной температуре, потому что очень
велика заселенность нижнего Лаймановского
уровня, а это – осн. условие возможности
поглощения. Второе условие состоит в
том, чтобы в пучке излучения содержались
кванты соответствующих энергий. Серию
в которой проявляется поглощение
называют главн.серией. Серия Бальмера
не проявляется в поглощении при комн.
тем-рах, потому что бальмеровский уровень
при комнатной тем-ре оказ-ся незаселенным.
П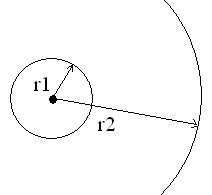
 о
квантовой теории состояние электрона
в атоме хар-ся не одним квантовым числом,
несколькими. рассмотрим эти квант.
числа. 1.
главное квантовое число
– n.
Во многоэлектронной оболочке электроны
группируются слоями, в пределах одного
слоя эл-ны имеют примерно одинаковую
энергию. Гл. кв. число хар-ет принадлежность
эл-на к данному слою и вместе с тем хар-ет
осн. часть энергии эл-на
о
квантовой теории состояние электрона
в атоме хар-ся не одним квантовым числом,
несколькими. рассмотрим эти квант.
числа. 1.
главное квантовое число
– n.
Во многоэлектронной оболочке электроны
группируются слоями, в пределах одного
слоя эл-ны имеют примерно одинаковую
энергию. Гл. кв. число хар-ет принадлежность
эл-на к данному слою и вместе с тем хар-ет
осн. часть энергии эл-на
![]() если 1 то К-оболочка, если 2, то L-оболочка,
и т.д. M,
N,
O.
2. Азимутальное
кв. число –
l(эл).
При данном значении n:
если 1 то К-оболочка, если 2, то L-оболочка,
и т.д. M,
N,
O.
2. Азимутальное
кв. число –
l(эл).
При данном значении n:
![]() (n-значений)
при 0 – s-состояние,
при 1- p-состояние,
и т.д. d,
f.
(n-значений)
при 0 – s-состояние,
при 1- p-состояние,
и т.д. d,
f.
![]() ,
,
![]() -
момент импульса орбитального движения
Эта формула выражает квантование момента
импульса. 3.
«магнитное» квант. число орбитального
движения-
-
момент импульса орбитального движения
Эта формула выражает квантование момента
импульса. 3.
«магнитное» квант. число орбитального
движения-![]() При
данном значении l
может принимать одно из значений:
При
данном значении l
может принимать одно из значений:
![]() где
(2l+1)
различных значений
где
(2l+1)
различных значений
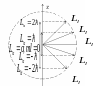
![]()
![]() -
проекция вектора
на
преимущественное направление. Таким
преимущ-м напр-м может явл-ся направление
внешнего магнитного поля (или внутр.).
Оказывается вектор момента импульса
орбитального движения
во
внешнем поле может быть ориентирован
в пространстве только в нескольких
строго определенных избранных
направлениях. Другие направления простр.
ориентации оказываются запрещенными.
4. спиновое
квантовое число – S.
S=1/2
-
проекция вектора
на
преимущественное направление. Таким
преимущ-м напр-м может явл-ся направление
внешнего магнитного поля (или внутр.).
Оказывается вектор момента импульса
орбитального движения
во
внешнем поле может быть ориентирован
в пространстве только в нескольких
строго определенных избранных
направлениях. Другие направления простр.
ориентации оказываются запрещенными.
4. спиновое
квантовое число – S.
S=1/2
![]() где
где
![]() -
спин электрона или момент импульса
собственного движения эл-на. Понятие
спина выдвинули в 1925 году Уленбек и
Гаудстит. 5.
магнитое квантовое число
-
-
спин электрона или момент импульса
собственного движения эл-на. Понятие
спина выдвинули в 1925 году Уленбек и
Гаудстит. 5.
магнитое квантовое число
-
![]() .
при данном S=1/2:
.
при данном S=1/2:
![]()
![]() эта формула выражает явление
пространственного квантования спина.
Существ. 2 возможных направления
ориентации спинового момента.
эта формула выражает явление
пространственного квантования спина.
Существ. 2 возможных направления
ориентации спинового момента.![]()
![]() Если преписать этому явлению клссическую
модель, то надо предположить, что наряду
с орбит. Движением существует ещё и
собственное, подобное суточному вращению
планеты (Земли). 6.
внутреннее кв. число –J.
При данных
l
и s
может принимать
Если преписать этому явлению клссическую
модель, то надо предположить, что наряду
с орбит. Движением существует ещё и
собственное, подобное суточному вращению
планеты (Земли). 6.
внутреннее кв. число –J.
При данных
l
и s
может принимать
![]() - здесь (2s+1)
различных значений. Пусть l=1,
s=1/2
J=1/2;
3/2.
- здесь (2s+1)
различных значений. Пусть l=1,
s=1/2
J=1/2;
3/2.
![]()
![]() -определяет
суммарный мех. момент импульса орбитального
и спинового дв-я электрона. 7.
магнитное квантовое число суммарного
момента импульса. -
-определяет
суммарный мех. момент импульса орбитального
и спинового дв-я электрона. 7.
магнитное квантовое число суммарного
момента импульса. -![]()
![]() здесь
здесь
![]() -значений.
-значений.
![]() где
где![]() -
проекция суммарного мех.момента на
преимущественное направление. Она
выражает явление пространственного
квантования суммарного момента импульса.
Теория Бора хорошо описывает спектры
атомарного водорода и изоэлектронного
ряда, также состояния электрона. Однако
теория Бора оказалось не в состоянии
описать оптические спектры ни одного
другого атома гелия, лития и др. Значит
поведение эл-в во многоэлктронной
системе взаимодействующих эл-в подчиняется
каким-то другим законам. Эти законы были
раскрыты квантовой механикой. Одним из
важных принципов явл-ся принцип Паули.
Принцип Паули утверждает, что в
многоэлектроноой системе взаимодействующих
электронов не может быть одинаковых
электронов. хотя бы одной из своих
квантовых характеристик электроны
должны различаться. А этими характеристиками
явл-ся 4 квантовых числа: n,
l,
,
.Можно
подсчитать сколько возможных значений
различных состояний при данном n.
Оказалось
-
проекция суммарного мех.момента на
преимущественное направление. Она
выражает явление пространственного
квантования суммарного момента импульса.
Теория Бора хорошо описывает спектры
атомарного водорода и изоэлектронного
ряда, также состояния электрона. Однако
теория Бора оказалось не в состоянии
описать оптические спектры ни одного
другого атома гелия, лития и др. Значит
поведение эл-в во многоэлктронной
системе взаимодействующих эл-в подчиняется
каким-то другим законам. Эти законы были
раскрыты квантовой механикой. Одним из
важных принципов явл-ся принцип Паули.
Принцип Паули утверждает, что в
многоэлектроноой системе взаимодействующих
электронов не может быть одинаковых
электронов. хотя бы одной из своих
квантовых характеристик электроны
должны различаться. А этими характеристиками
явл-ся 4 квантовых числа: n,
l,
,
.Можно
подсчитать сколько возможных значений
различных состояний при данном n.
Оказалось
![]() где
где![]() -число
разл. состояний при фиксированном гл.
кв. числе. Принцип Паули объясняет
закономерности таблицы Менделеева.
Основная закономерность – это
периодичность хим. и оптич. свойств. И
те и др. определяются состоянием валентных
внешних электронов. Периодичность св-в
эл-в таблицы Менделеева можно понять
исходя из принципа Паули и учитывая,
что при переходе от данного элемента к
следующему появляется ещё один электрон.
Если при этом застройка данной оболочки
заканчивается, то возникает очень
прочная система взаимодействующих
эл-в, такие атомы плохо взаимодействуют
с др. атомами – это инертные газы(аргон,
гелий и т.д.). В атоме следующего элемента
появляется единственный электрон во
внешней оболочке, который активно
участвует в химических процессах и в
образовании спектров (Li,
K,
Cu).
Рассмотрим структуру таблицы Менделеева
исходя из пр. Паули. n=1-
одноквантовая оболочка (K-оболочка)
l=0,
=0,
=±1/2
(почему см. выше).т.о. n=1,
l=0,
=0,
=±1/2-всего
2 состояния.
n=2-
двухквантовая оболочка (L-оболочка)
здесь уже
l=0,1,
если l=0,
то
=0,
=±1/2
– 2 состояния за счет пространственного
квантования спина,
а если l=1,
то
=1,
0, -1;
=±1/2
– 6 состояний p-состояние
(p-электрон).Значит
для двух атомной оболочки:
-число
разл. состояний при фиксированном гл.
кв. числе. Принцип Паули объясняет
закономерности таблицы Менделеева.
Основная закономерность – это
периодичность хим. и оптич. свойств. И
те и др. определяются состоянием валентных
внешних электронов. Периодичность св-в
эл-в таблицы Менделеева можно понять
исходя из принципа Паули и учитывая,
что при переходе от данного элемента к
следующему появляется ещё один электрон.
Если при этом застройка данной оболочки
заканчивается, то возникает очень
прочная система взаимодействующих
эл-в, такие атомы плохо взаимодействуют
с др. атомами – это инертные газы(аргон,
гелий и т.д.). В атоме следующего элемента
появляется единственный электрон во
внешней оболочке, который активно
участвует в химических процессах и в
образовании спектров (Li,
K,
Cu).
Рассмотрим структуру таблицы Менделеева
исходя из пр. Паули. n=1-
одноквантовая оболочка (K-оболочка)
l=0,
=0,
=±1/2
(почему см. выше).т.о. n=1,
l=0,
=0,
=±1/2-всего
2 состояния.
n=2-
двухквантовая оболочка (L-оболочка)
здесь уже
l=0,1,
если l=0,
то
=0,
=±1/2
– 2 состояния за счет пространственного
квантования спина,
а если l=1,
то
=1,
0, -1;
=±1/2
– 6 состояний p-состояние
(p-электрон).Значит
для двух атомной оболочки:
![]() (здесь
1-это К-оболочка, а 2 - L-оболочка).
n=3-
трехквантовая оболочка (M-оболочка)
(здесь
1-это К-оболочка, а 2 - L-оболочка).
n=3-
трехквантовая оболочка (M-оболочка)
![]() (здесь
1-это К-оболочка, 2 - L-оболочка,
3 - M-оболочка(помещается
18 электронов)).
(здесь
1-это К-оболочка, 2 - L-оболочка,
3 - M-оболочка(помещается
18 электронов)).
Методика. Раскрыть значение изучения данной темы в школьном курсе физики. Раскрыть методику изучения одного из основных элементов системы знаний об атоме модель атома, постулаты Бора, линейчатые спектры.
Квантовые постулаты Бора.
На примере изучения строения атома учащимся показывают, как и для чего создают модели объектов для физического исследования, подчеркивают ограниченность каждой модели, раскрывают путь познания истины через последовательное уточнение модельных представлений. Это имеет важное значение для развития научного мировоззрения школьников. Действительно, в молекулярно-кинетической теории газов используются шарики как модель атома. При попытке разобраться в структуре атома была создана модель атома, которая, по образному выражению физиков, выглядела как пирог с изюмом (модель Томсона). Опыты Резерфорда опровергли эту модель и привели к создания планетарной модели атома. Однако эта модель также несовершенна: согласно классической теории, электрон, двигаясь по круговой орбите и, следовательно, обладая ускорением, должен излучать энергию; в результате электрон упадет на ядро и атом прекратит свое существование. Кроме того, согласно этой модели спектр излучения атома должен быть сплошным, между тем опыты показывают, что он линейчатый. Поэтому предположенная Резерфордом модель атома нуждалась в дальнейшем уточнении. Это была сделано в 1913 г. Бором.
Н. Бор увидел за этими «неправильностями» в поведении электрона в атоме своеобразие законов, которым подчиняются микрочастицы. Он сформулировал постулаты, которые согласовывали модель атома Резерфорда с экспериментальными фактами (стабильность атома, дискретный характер излучаемой им энергии).
Постулаты Бора необходимо не только сформулировать, но и пояснить. Первый постулат (постулат стационарных состоянии) формулируют так: атом может находиться только в особых стационарных состояниях, каждому из которых соответствует определенная энергия; в стационарном состоянии атом энергии не излучает. Этот постулат требует пояснений. Энергия атома квантуется, т. е. может принимать ряд дискретных значений. Наименьшим значением энергии атом обладает тогда, когда его электрон находится на ближайшей к ядру орбите. Чем больше радиус орбиты, тем больше энергия соответствующего стационарного состояния. В стационарном состоянии атом энергии не излучает.
Если хорошо усвоен первый постулат Бора, школьники легко усваивают и второй постулат (правило частот): при переходе атома из одного стационарного состояния в другое атом испускает или поглощает один фотон, энергия которого равна разности энергий стационарных состояний:
![]()
Этот постулат обосновывает квантовый характер излучения факт, установленный М. Планком и развитый А. Эйнштейном.
При
изложении теории Бора возникает вопрос:
нужно ли знакомить
школьников с правилом квантования орбит
- третьим (специальным)
постулатом Бора? Ведь момент импульса
- понятие, незнакомое учащимся. Они его
не изучали в механике. Поэтому ряд
методистов
считает, что с третьим постулатом Бора
учащихся лучше не
знакомить. Однако третий постулат
указывает на правило квантования орбит,
и без него нельзя вывести значение
энергии в стационарных
состояниях. Поэтому отказ от ознакомления
школьников с
третьим постулатом Бора влечет за собой
поверхностное их ознакомление с атомом
водорода и его спектрами и приводит к
слабому усвоению материала. Поэтому,
несмотря на известную трудность, лучше
ознакомить учащихся и с третьим постулатом
Бора. Вводят
третий постулат Бора на основе следующих
рассуждений:
Н. Бору надо было найти радиусы разрешенных
орбит для определения
энергии атома в стационарных состояниях.
Для этого нужно
было указать правило квантования. Он
предположил, что какая-то
величина должна быть кратной постоянной
Планка Н.
Постоянная
Планка выражается в джоуль-секундах.
Но так же в
единицах
СИ выражается широко используемая в
механике величина
-
![]() (само
понятие момента импульса при этом можно
не
вводить).
(само
понятие момента импульса при этом можно
не
вводить).
Естественно было предположить, что должно выполняться соотношение,
![]()
![]() или
или
![]() где
т
- масса,
v
-
скорость,
r
- радиус
орбиты электрона, а
где
т
- масса,
v
-
скорость,
r
- радиус
орбиты электрона, а
После этого постулаты Бора используют для объяснения строения атома водорода.
Вывод формулы энергии, которой атом водорода обладает в различных стационарных состояниях,
![]()
не представляет трудности. При анализе ее важно подчеркнуть, что эта энергия обратно пропорциональна квадрату квантового, числа п:
![]()
и отрицательна, а это соответствует притяжению электронов к ядру. Желательно подсчитать энергию атомов в основном состоянии (первый энергетический уровень):
![]()
а затем энергию, соответствующую второму, третьему, четвертому уровням:
Е2=-1/4 Е1= -3,39эВ,
Е3 =1/9 Е1 =-1,51 эВ,
Е4 = 1/16 Е1=-0,85 эВ.
 Энергия
атома при
Энергия
атома при
![]() стремится к
нулю. Это дает возможность построить
диаграмму
энергетических уровней атома водорода
следующим образом. Сверху проводят
линию, соответствующую нулевому
значению энергии. В произвольном
масштабе откладывают от
этой линии вниз значение энергии
что по мере увеличения числа п
расстояние
между уровнями уменьшается.
стремится к
нулю. Это дает возможность построить
диаграмму
энергетических уровней атома водорода
следующим образом. Сверху проводят
линию, соответствующую нулевому
значению энергии. В произвольном
масштабе откладывают от
этой линии вниз значение энергии
что по мере увеличения числа п
расстояние
между уровнями уменьшается.
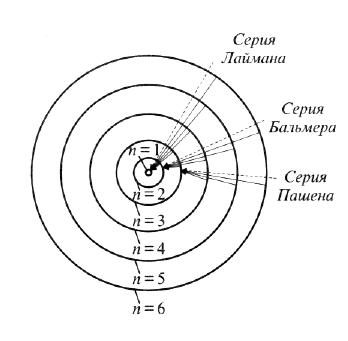 уровни
постепенно сближаются, интервалы
между ними становятся исчезающе малыми,
дискретность «смазывается»; возникает
квазинепрерывность, т. е. при больших
квантовых
числах квантово-механическое описание
системы эквивалентно
классическому.
уровни
постепенно сближаются, интервалы
между ними становятся исчезающе малыми,
дискретность «смазывается»; возникает
квазинепрерывность, т. е. при больших
квантовых
числах квантово-механическое описание
системы эквивалентно
классическому.
Необходимо подчеркнуть, что теория атома Бора не была последовательной. Используя классические законы для описания движения электрона в атоме, она накладывала на них некоторые ограничения. Но даже эта далеко еще не совершенная теория знаменовала собой дальнейший шаг на пути отказа от универсальности классических представлений (первые были сделаны М. Планком и А. Эйнштейном) и позволила достаточно хорошо объяснить строение атома водорода и его спектры.
