
Питання до екзамену з фізики. Розділ. Атомна і ядерна фізика.
1.ДОСЛІДИ РЕЗЕРФОРДА. ЯДЕРНА МОДЕЛЬ АТОМА. КВАНТОВІ ПОСТУЛАТИ БОРА. ПОГЛИНАННЯ ТА ВИПРОМІНЮВАННЯ СВІТЛА АТОМОМ
Наприкінці ХIX - на початку XX ст. у фізиці було отримано кілька визначних дослідних фактів, які привернули увагу вчених до мікросвіту. Це відкриття: Х-променів (1895 р., В. К. Рентген, І. Пулюй), названих згодом рентгеніаським випромінюванням, радіоактивності (І896 p., А. Беккерель), електрона (1897 p., Дж. Дж. Томсон). Вони ставили під сумнів Уявлення давніх учених про неподільність атома, суперечили усталеним класичним уявленням про будову речовини, спонукали до поглиблення знань про явища, які відбуваються в мікросвіті. Так зародилася атомна фізика, яка вивчає будову і властивості атомів, процеси на атомному рівні.
Для атомної фізики характерні відстані, сумірні з розміром атома (~10-10 м), та енергія порядку 10-19(Г19 Дж (кілька еВ) БУДОВА АТОМА. ДОСЛІДИ РЕЗЕРФОРДА У 1897 р. англійський фізик Дж. Дж. Томсон експериментально відкрив електрон як складову частинку атома, що має найменший електричний заряд. Він припустив, що атом — це позитивно заряджена куля, всередині якої містяться негативно заряджені електрони. Рівномірність їх розподілу в об'ємі кулі та рівність гюзитивного і негативного зарядів забезпечують електричну нейтральність атома.
Модель атома Томсона називавють «пудинговою» — за аналогією з традиційним британський пирогом з родзинками
Проте така модель атома мала свої обмеження і не відповідала дослідним фактам, отриманим на той час фізиками. Запропонувати більш реальну модель атома вдалося лише після дослідів Е. Резерфорда і формулювання квантових постулатів Н. Бором.
Альфа-частинки — це позитивно заряджені частинки, заряд яких дорівнює двом зарядам електрона, а маса приблизно в чотири рази більша за масу атома Гідрогену, тобто це ядра атома Гелію
У 1911 р. англійський фізик Е. Резерфорд, досліджуючи разом зі своїми співробітниками бомбардування альфа-частинками тонких металевих пластинок, встановив, що вони певним чином розсіюються в речовині (мал. 7.1).
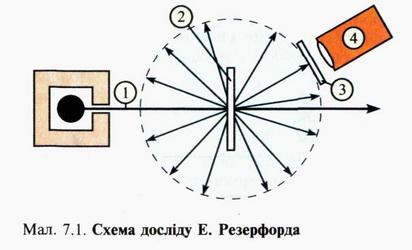
Вузький пучок швидких альфа-частинок 1 спрямовувався на тонку золоту чи платинову пластинку 2, за якою розміщувався екран 3, здатний фіксувати їх попадання на екран спалахами. За допомогою спеціального оптичного пристрою 4 можна була спостерігати і вимірювати кут відхилення ф альфачастинок.
Дослід Е. Резерфорда започаткував основи сучасних уявлень про будову атома
Більшість із них рухалася майже прямолінійно (кут відхилення ф становив 1—2°). Проте незначна їх частка відхилялася на більші кути; були зафіксовані навіть такі альфачастинки, які після розсіювання змінювали свій напрямок руху на протилежний (ф > 90°).
Щоб пояснити одержані результати, Е. Резерфорд припустив, що атом має складну будову, схожу на Сонячну систему: всередині його міститься позитивно заряджене ядро, навколо якого обертаються електрони (мал. 7.2).
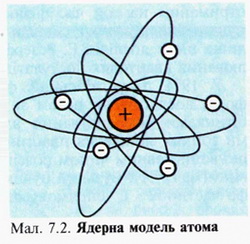
Його розрахунки довели, що в ядрі зосереджена практично вся маса атома, але його розміри набагато менші за сам атом. Вимірювання показали, що лінійні розміри атома становлять приблизно 10-10 м, а радіус його ядра дорівнює близько 10-15 м. Зрозуміло, що схематичні зображення атомів тут і в інших книгах подаються без дотримання масштабів.
Отже, на підставі одержаних експериментальних даних Е. Резерфорд запропонував ядерну модель атома, яка узгоджувалася з результатами дослідів і пояснювала багато інших явищ, пов'язаних з будовою атома.
Справді, швидкі альфа-частинки легко долають простір електронних оболонок атомів, не зазнаючи з їхнього боку значного впливу, і тому майже не відхиляються від прямолінійної траєкторії руху. Проте коли вони пролітають досить близько від позитивно зарядженого ядра атома, кулонівська взаємодія між ядром і частинками змушує їх викривляти траєкторію і відхилятися на певний кут (мал. 7.3).
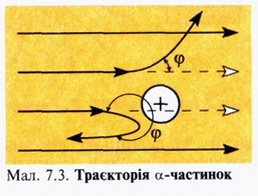
Е. Резерфорд на основі законів електромагнітної взаємодії вивів формулу, яка дає змогу обчислити кількістьа-частинок, розсіяних на кут ф, залежно від їх енергії і хімічної природи досліджуваного матеріалу. Пізніше ця теоретично виведена формула була експериментально підтверджена й остаточно утвердила в фізиці ядерну модель атома.
Радикальні висновки про будову атома, що слідували з дослідів Резерфорда,змушували багатьох вчених сумніватися в їх справедливості. Не був винятком і сам Резерфорд, який опублікував результати своїх досліджень тільки в 1911 р. через два роки після виконання перших експериментів. Спираючись накласичні уявлення про рух мікрочастинок, Резерфорд запропонувавпланетарну модель атома. Відповідно до цієї моделі, в центрі атомарозташовується позитивно заряджене ядро, в якому зосереджена майже всямаса атома. Атом в цілому нейтральний. Навколо ядра, подібно планетам, піддією кулонівських сил з боку ядра обертаються електрони (рис. 6.1.4).Перебувати в стані спокою електрони не можуть, так як вони впали б на ядро
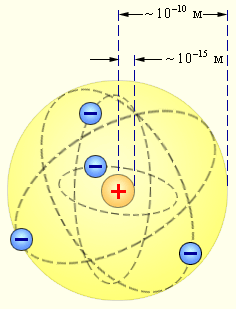
Планетарна модель атома, запропонована Резерфордом, безсумнівно стала великим кроком вперед у розвитку знань про будову атома. Вона булаабсолютно необхідною для пояснення дослідів з розсіювання α-частинок, проте виявилася нездатною пояснити сам факт тривалого існування атома, т.е. його стійкість. За законами класичної електродинаміки, що рухається з прискоренням заряд повинен випромінювати електромагнітні хвилі, що забирають енергію. За короткий час (близько 10-8 с) всі електрони в атоміРезерфорда повинні розтринькати всю свою енергію і впасти на ядро. Те, що цього не відбувається в стійких станах атома, показує, що внутрішні процесив атомі не підкоряються класичним законам.
Ізотопи — нукліди одного і того самого хімічного елементу, які мають різне число нейтронів, а, отже, різну атомну масу.
Ізотопи позначають тими самими символами, що і хімічний елемент, додаючи зверху з лівого боку символу масове число, наприклад, ізотопи хлору позначають: 35Cl і 37Cl, чи масове число слідує за назвою чи символом елементу, наприклад: уран-233 чи Pu-239.
Ізотопи даного хімічного елементу мають однаковий заряд атомного ядра, тобто один порядковий номер, і займають те ж саме місце в періодичній системі, мають однакову кількість протонів в ядрі атома, але відрізняються один від одного кількістю нейтронів. Так, в атомному ядрі ізотопу хлору 35Cl міститься 17 протонів, оскільки порядковий номер хлору 17, і 18 нейтронів (35—17=18), а в ядрі ізотопу хлору 37Cl — 17 протонів і 20 нейтронів (37—17 = 20).
Деякі хімічні елементи мають невелику кількість стабільних ізотопів. Так, для Оксигену відомо три стабільні ізотопи: 16O (ядро складається з 8 протонів і 8 нейтронів), 17O (ядро складається з 8 протонів і 9 нейтронів) і 18О (ядро складається з 8 протонів і 10 нейтронів). Для водню відомо теж три ізотопи: 1H (ядро складається лише з одного протона), 2H (ядро складається з одного протона і одного нейтрона), 3H (ядро складається з одного протона і двох нейтронів). Деякі ж хімічні елементи складаються з досить великої кількості ізотопів. Наприклад, ксенон має 9 ізотопів, олово — 10 і т. д.
Переважна більшість ізотопів не має спеціальних назв, але для ізотопів деяких елементів, зокрема для ізотопів водню, існують спеціальні назви і навіть спеціальні символи. Так, ізотоп водню 1H називають протій, ізотоп 2H — дейтерій і позначають символом D а ізотоп 3Н — тритій (символ T). Деякі ізотопи в природі досить поширені, як, наприклад, ізотоп кисню 16O і ізотоп водню 1Н, а інші ізотопи зустрічаються в дуже мізерних кількостях, як ізотопи кисню 17O і 18O і ізотопи водню 2H і 3H.
За хімічними властивостями всі ізотопи даного елементу дуже близькі, тому різниці між ними при хімічних реакціях не проводять. Виняток становлять лише ізотопи водню, які за своїми властивостями помітно відрізняються один від одного.
Атомна маса ізотопу, виражена у вуглецевих одиницях, називається його масовим числом. Масові числа ізотопів є цілими числами.
