
- •1) Основные положения молекулярно-кинетической теории и их опытное обоснование
- •2) Диффузия
- •3) Броуновское движение
- •4) Масса молекул
- •5) Количество вещества. Постоянная Авогадро
- •6) Размеры молекул
- •7) Идеальный газ
- •8) Скорости молекул газов
- •9) Основное уравнение мкт идеального газа
- •10) Температура и тепловое равновесие системы
- •11) Измерение температуры
- •12)Абсолютная температурная шкала. Абсолютный нуль.
- •13)Уравнение состояния идеального газа
- •14)Частые случаи уравн. Состояния идеал. Газа
- •15) Термодинамический подход к изучению физических процессов
- •16)Термодинамические параметры состояния тела
- •17) Внутренняя энергия тел
- •18)Измерение внутренней энергии
- •19)Количестао теплоты
- •20)Работа в термодинамике
- •21) Первый закон термодинамики
- •22)Применение 1-го закона термодинамики к различным тепловым процессам.
- •23)Адиобатный процесс
- •24) Теплоемкости при постоянном давлении и постоянном объеме
- •25) Обратимые и необратимые процессы. Необратимость тепловых процессов.
- •26)Тепловые двигатели. Принцип их действия.
- •27) Кпд теплавого двигателя.
- •28) Роль тепловых двигателей в развитии теплоэнергетики и транспорта. Тепловые двигатели и охрана природы
- •29) Испарение и конденсация
- •30) Насыщенные и ненасыщенные пары и их свойства
- •31) Кипение жидкостей. Зависимость температуры кипения от давления
- •32) Влажность воздуха. Точка росы. Психрометр. Гигрометр
- •33) Свойства жидкостей
- •34) Поверхностная энергия
- •35) Поверхностное натяжение
- •36) Смачивание. Капиллярные явления
8) Скорости молекул газов
Движение молекул газа подчиняется законам статистической физики. В каждый момент времени скорости отдельных молекул могут значительно отличаться друг от друга, но их средние значения одинаковы и при расчетах используются не мгновенные скорости отдельных молекул, а некоторые средние значения. Различают среднюю арифметическую <u> и среднюю квадратичную <Uкв> скорость хаотического движения молекул.
Пусть имеется N молекул, скорости которых соответственно u1, u2,…., un. Средняя арифметическая скорость хаотического движения молекул по модулю равна

Средняя квадратичная скорость хаотического движения молекул
![]()
где<υ^2>-средний
квадрат скорости движ. молекул.Его не
следует с квадратом средней скорости<
υ ^2>≠(< υ >)^2.Как показывают
расчеты ;
;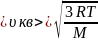 ;R-универ.газ
постоянная.R=8.31Дж/моль*К;
R=KNa
;
;R-универ.газ
постоянная.R=8.31Дж/моль*К;
R=KNa
;
9) Основное уравнение мкт идеального газа
Это уравнение связывает между собой параметры состояния идеального газа и характеристики движения его молекул. Для вывода основного уравнения МКТ рассмотрим одноатомный идеальный газ, находящийся в термодинамическом равновесии.
Представим себе сосуд в виде куба с длиной ребра / (рис.6.4), в котором беспорядочно движутся Л' молекул массой то каждая. Стенки сосуда подвергаются непрерывной бомбардировке молекулами. Удары молекул обуславливают давление газа на стенки. В виду беспорядочности движения молекул, результат их удара о стенки таков, как если бы 1/3 всех молекул двигалась прямолинейно между правой и левой стенками (вдоль оси х), 1/3 молекул — между передней и задней стенками (вдоль оси у) и 1/3 молекул — между верхней и нижней стенками (вдоль оси г). Отдельная молекула, летящая перпендикулярно к одной из стенок, например, к правой со скоростью у в результате упругого удара отскочит назад и ее импульс изменится на Ар = р – ро или в проекциях: Ар = тoи - (-mou )= 2mou
продолжительность удара. Р=1/3nm0<v^2>;vкен=m0<v^2>/2; Р=2/3nWкен=nKT;-Уравнение МКТ. n- конц.молекул, К-кофициэнт, постоянная Вольцмана.К=1.38*10^-23Дж/К. Wкен=3/2KT.
10) Температура и тепловое равновесие системы
Если два тела разной температуры привести в соприкосновение, то, как показывает опыт, между ними будет происходить теплообмен -— передача энергии от более нагретого тела к менее нагретому, и тела придут в состояние теплового равновесия, температуры у них будут одинаковые.
Тепловым равновесием называют такое состояние системы, при котором все макроскопические параметры (P,V,T) остаются неизменными.
Любая термодинамическая система может находиться в различных состояниях теплового равновесия. В каждом из этих состояний давление и объем могут быть различны (но постоянны), а температура имеет строго определенное значение, и она одинакова во всех частях системы. Следовательно, температура характеризует состояние теплового равновесия термодинамической системы. Если привести в соприкосновение два газа с различными значениями средней кинетической энергии молекул, то молекулы, движущиеся с большими скоростями, сталкиваясь с молекулами другого газа, будут их ускорять, сами при этом замедляясь. Происходит передача энергии, пока не наступит момент, когда средние кинетические энергии молекул обоих газов выравняются. Это и есть состояние теплового равновесия, при котором переход внутренней энергии от одного газа к другому прекращается, хотя столкновения беспорядочно движущихся молекул обоих газов будет продолжаться.
Температура характеризует тепловое равновесие:
P=2/3n<WK>=2/3n/V*<WK>: 2/3*<WK>=PV/N: PV/N=KT: <WK>=3/2*KT
Абсалютная Т есть мера <Wкен>поступательного движ. молекул.
