
- •2. Вторичная кристаллизация (изменения в твердом состоянии устойчивой кристаллической решетки.)
- •11. Классификация арматуры для ж/б конструкций.
- •13. Виды сварных соединений и швов
- •Вопрос 20.
- •Механические свойства и способы определения их количественных характеристик: твердость, вязкость, усталостная прочность
- •Твердость по Бринеллю ( гост 9012)
- •М етод Виккерса
- •Правила безопасной работы при производстве сварочных работ
- •Взято из СанПиН. СанПиН 2.2.3.1384-03. Гигиенические требования к организации строительного производства и строительных работ
- •22. Гигиенические требования к производству сварочных работ и резке
Билет 1. РОЛЬ МЕТАЛЛОВ В РАЗВИТИИ ЦИВИЛИЗАЦИИ.
В настоящее время металл можно без преувеличения назвать самым распространенным материалом, используемым человечеством в быту и производстве. И если в первобытные времена, когда люди еще только-только научились использовать металлы в своей деятельности, без их использования можно было легко обойтись, то сегодня без металла немыслимо существование человечества, ведь различные его виды необходимы в машиностроении, в дорожном и жилищном строительстве и других отраслях.
Долгое время самыми распространенными видами металлов, широко используемыми в промышленности и быту, были железо, медь, золото, серебро, олово, ртуть и свинец. До начала XVIII столетия люди полагали, что только эти материалы являются металлами и не знали о существовании иных.
Алхимики были уверены в том, что все металлы имеют сложную структуру, в которую входят начала «металличности» и «горючести». В 1789 году количество металлов было расширено до семнадцати, весь их список был опубликован в руководстве по химии А.Л. Лавуазье. По мере развития химии увеличивалось и число известных металлов, в первой половине девятнадцатого века были созданы щелочные и щёлочноземельные металлы, для чего был использован электролиз.
В конце XIX века были экспериментально подтверждены заключения Д.И. Менделеева, который определил их существование, основываясь на периодическом законе. В это же время начинается поиск природных радиоактивных металлов, а в середине двадцатого столетия путем ядерных превращений были созданы еще некоторые из них.
С развитием и изучением металлов тесно связаны такие отрасли человеческой жизнедеятельности как строительство, промышленность, искусство, ремесла. Несмотря на появление и открытие новых видов металлов, материалы, известные еще со Средних веков, продолжают использоваться человечеством в ювелирном деле, скульптуре, декоративно-прикладном искусстве и в отдельных отраслях промышленности.
Особенно значима роль металла в промышленности, производства транспорта и строительстве зданий и дорог. Только представьте, что отсутствие металла привело бы к тому, что мы вынуждены были бы отказаться от любого современного транспорта (автомобилей, поездов, самолетов и т.д.), вернуться в дома, построенные из дерева, отказаться от возведения мостов и т.д.
Долгие столетия металл развивался и совершенствовался, вместе с развитием и прогрессом человеческой цивилизации. Открытие и создание новых видов металлов, совершенствование их свойств путем изготовления сплавов привело к тому, что они постоянно становятся все более и более совершенными.
ПРОИЗВОДСТВО ЧЕРНЫХ МЕТАЛЛОВ.

Билет 2. КРИСТАЛЛИЧЕСКОЕ СТРОЕНИЕ МЕТАЛЛОВ
Характеристика 3х агрегатных состояний
Агрегатные состояния: твердое, жидкое, газообразное
Газообразное: нет закономерности в расположении частиц
В жидкости: частицы сохраняют ближний порядок
Существуют вещества, которые при определенных условиях переходят из твердого состояния в газообразное(сублимация)
В твердом состоянии: порядок расположения четко определен.
Твердые вещества: кристаллические, аморфные.
Твердое стекло при нагреве размягчается и становится жидким (аморфное).
У аморфных тел не существует температуры перехода от жидкого состояния к твердому, отсюда следует – нет точки перехода различных свойств.
Кристаллические тела имеют температуру плавления, которая является постоянной для данного вещества.
Схема кристаллической структуры тела:
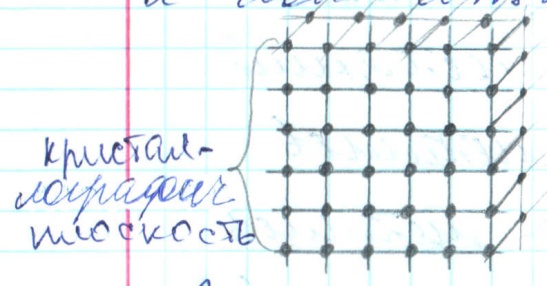
Расстояние между центрами соседних атомов в кристаллографической плоскости называется ангстремом.
Элементарные кристаллические решетки
Объемно - центрированная кубическая решетка (К.О-Ц)
Параметр «а» определяет размеры
В вершинах находится 8 атомов и 1 атом находится в центре куба
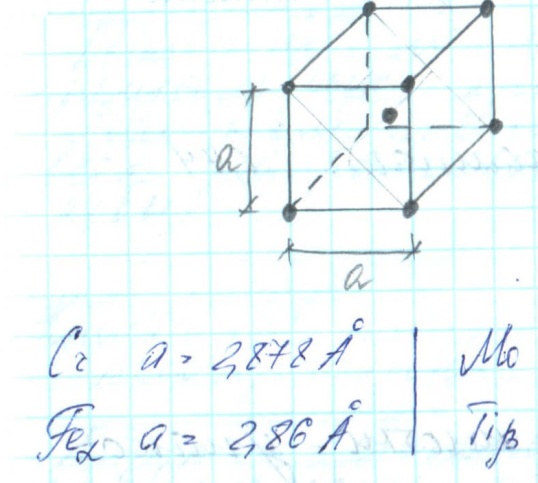
КОЭФИЦИЕНТ КОМПАКТНОСТИ – отношение объема, занимаемого атомом, ко всему объему. Характеризует плотность упаковки. К.О-Ц 068
КООРДИНАЦИОННОЕ ЧИСЛО – число атомов, находящихся на более близком равном расстоянии от данного атома. К=8
БАЗИС КРИСТАЛЛИЧЕСКОЙ РЕШЕТКИ – число атомов, приходящихся на 1 элементарную ячейку. 1/8*8+1=2
Кубическая гранецентрированная
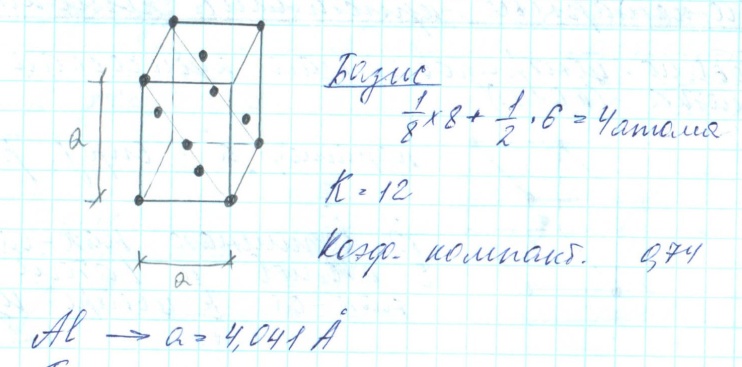
Гексагональная плотноупакованная
Реальное строение кристаллических металлов
Тела состоят из кристаллов
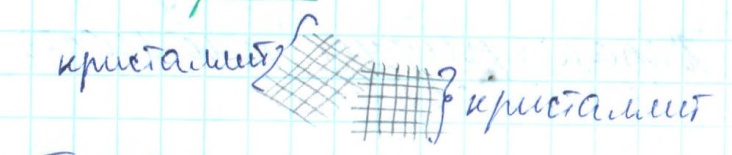
Анизотропия свойств кристаллов
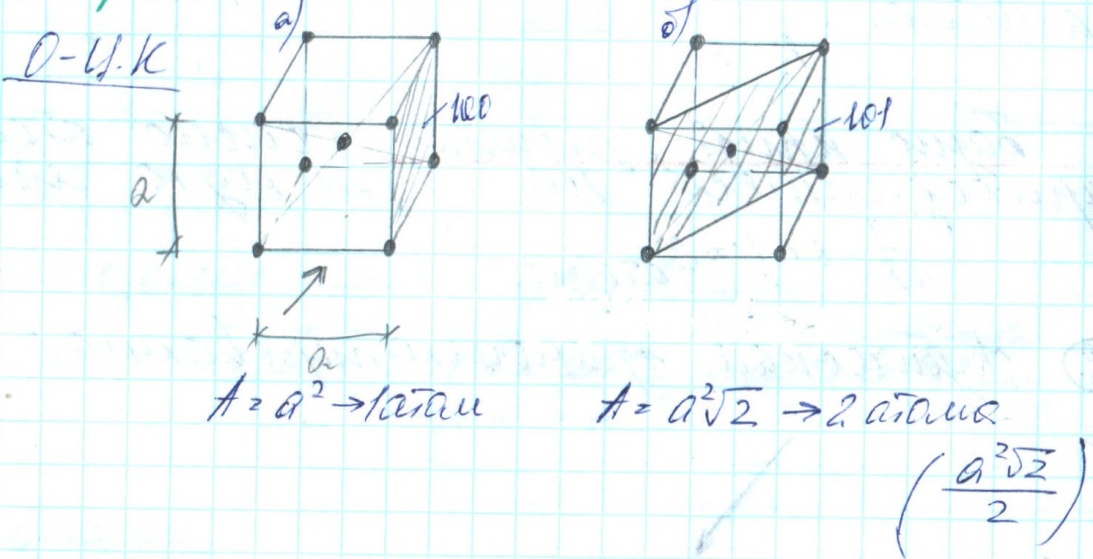
АНИЗОТРОПИЯ – различие свойств в зависимости от направления (приложения нагрузки), следует, что все кристаллы анизотропные.
Реальный металл состоит из произвольных кристаллов.
Реальный металл изотропен (во всех направлениях свойства одинаковые)
Кристаллы, имеющие некоторые несовершенства
Характер и степень
нарушения правильности кристаллического
строения определяют свойства металлов.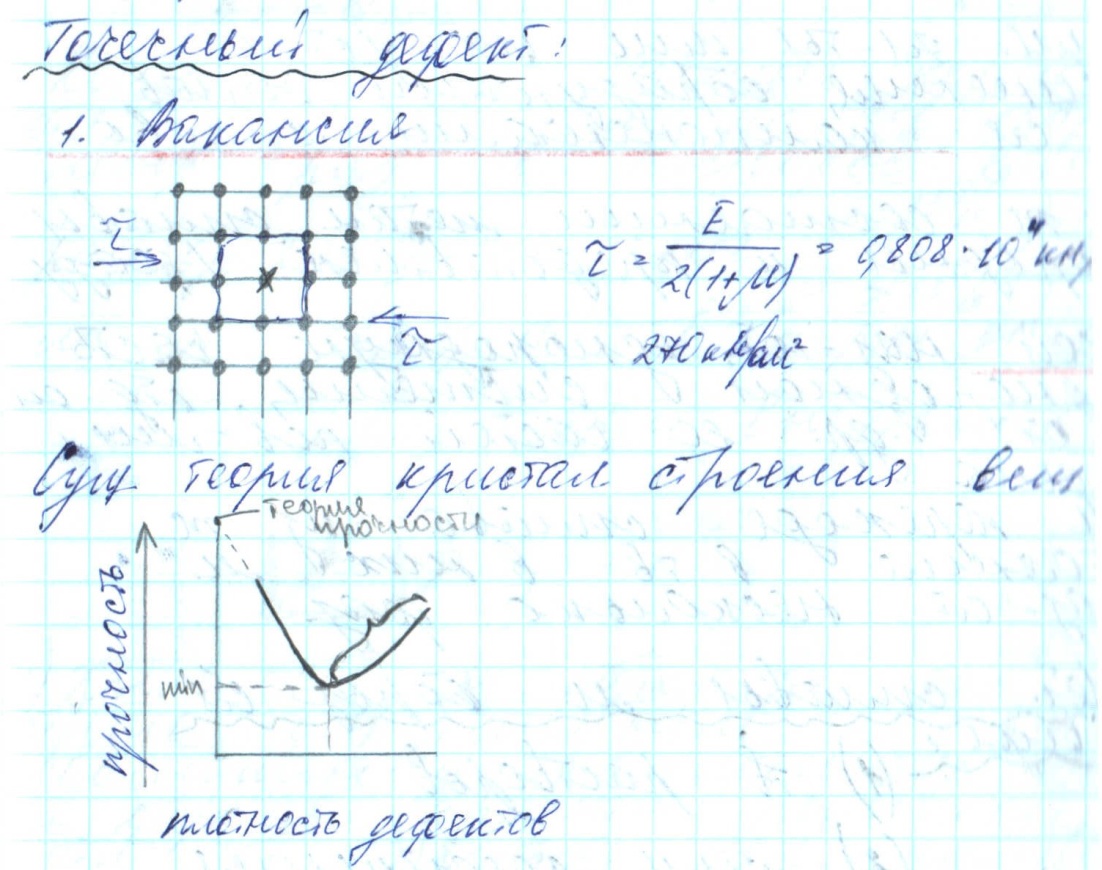
Билет 3. СТРОЕНИЕ ЖЕЛЕЗОУГЛЕРОДИСТЫХ СПЛАВОВ. ПРЕВРАЩЕНИЯ В ТВЕРДОМ СОСТОЯНИИ.
1. МЕТАЛЛИЧЕСКИМИ СПЛАВАМИ называют сложные по составу вещества, образующиеся в результате взаимодействия 2х или нескольких металлов, либо металлов с некоторыми неметаллами.
Химические элементы или их соединения, образующие сплав, называются КОМПОНЕНТАМИ СПЛАВА.
В жидком состоянии металлические сплавы однородны и представляют 1 фазу.
ФАЗОЙ называют однородную часть неоднородной системы, отделенной от других ее частей поверхностью раздела.
При переходе сплава из жидкого состояния в твердое в них может образоваться несколько фаз.
Металлические сплавы могут образовываться в виде: твердых растворов, хим. Соединений, механической смеси.
1)ТВЕРДЫМИ РАСТВОРАМИ называют сплавы из 2х или более компонентов, в которых атомы растворимого компонента располагаются в кристаллической решетке компонента растворителя.
РАСТВОРИТЕЛЕМ называют тот металл, кристаллическая решетка которого сохраняется как основа.
2 типа тв. растворов: замещение и внедрение

Компоненты, у которых атомные периоды отличаются не более, чем на 8%, образуют неограниченный ряд твердых растворов замещения. 8-15% - твердые
Растворы замещения с ограниченной растворимостью - >15% не могут образовывать твердые растворы замещения.
2) Химические соединения образуются при строго определенном количественном соотношении компонентов сплава и характеризующейся кристаллической решеткой, отличающейся от решеток исходных компонентов.
3) Механические смеси образуются при одновременном выпадении из жидкого расплава при его кристаллизации кристаллов, составляющие его компоненты.
Эвтектоидные смеси – эвтектики.
Механические смеси могут состоять из: чистых компонентов, твердых соединений, химических соединений.
2. Вторичная кристаллизация (изменения в твердом состоянии устойчивой кристаллической решетки.)
Существование одного и того же сплава металла с несколькими кристаллическими формами с различным расположением атомов в элементарной ячейке носит название АЛЛОТРОПИЯ или ПОЛИФОРМИЗМ.
Поэтому различные кристаллические формы одного и того же металла в различных металлических формах называют полиморфными или аллотропическими формами(α,β,γ и т.д), которые в виде индексов добавляются к символу, обозначающему металл.
Аллотропическая форма, установленная при самой низкой температуре обозначается «α».
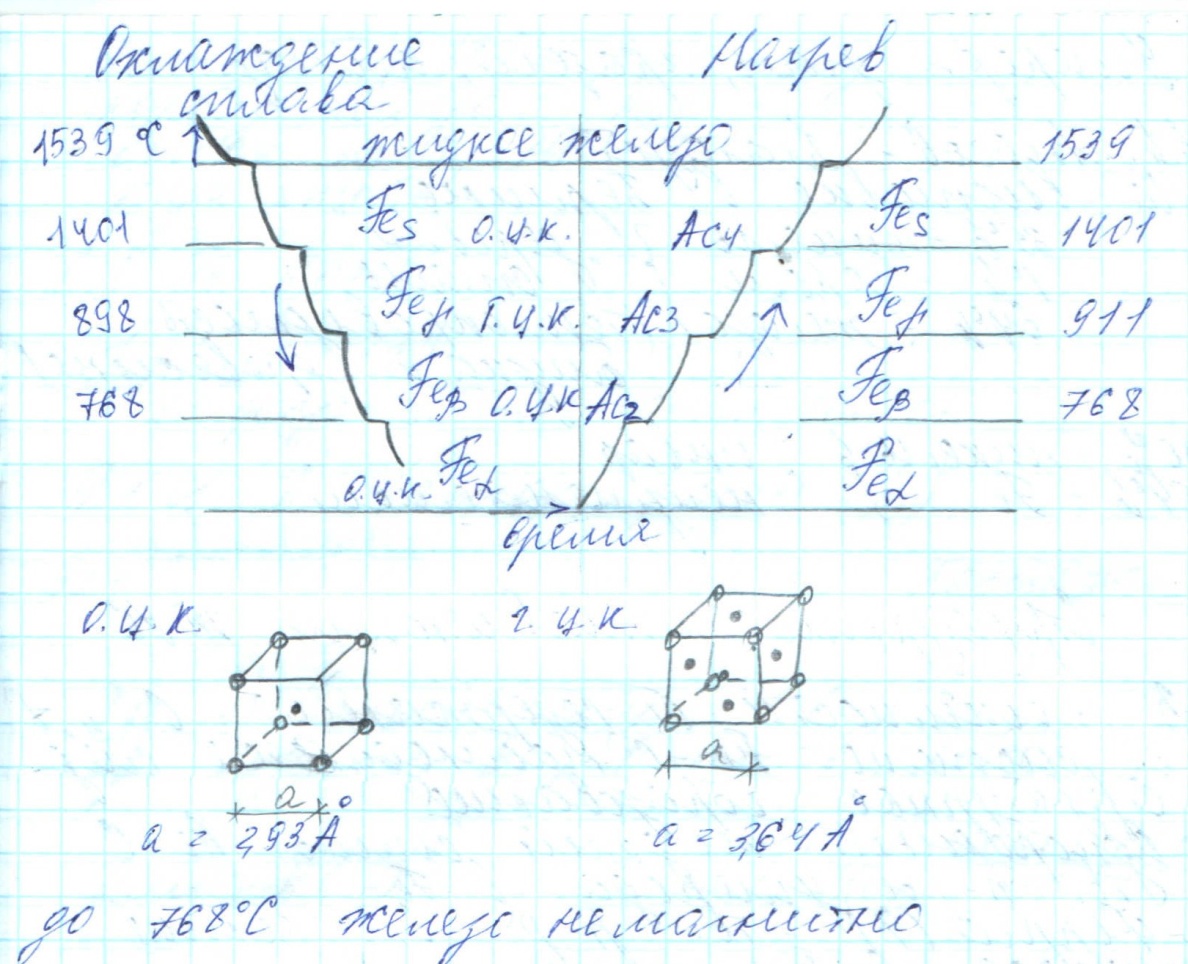
Температуры, при которых происходят аллотропические превращения, называются КРИТИЧЕСКИМИ ТЕМПЕРАТУРАМИ (А)
с – нагрев, r – остывание.
Ac2 |
Ac3 |
Ac4 |
Ar2 |
Ar3 |
Ar4 |
Билет 4. Структура сталей. Химический состав сталей.
В зависимости от содержания углерода и температуры в системе Fe-C наблюдаются следующие структурные образования:
Однородный жидкий сплав fe-C – тв. растворы углерода в Fe.
Феррит (Ф) –твердый раствор внедрения углерода в Feαс предельной концентрацией углерода 0.02% при температуре 727°С;сталь со структурой феррита ферромагнитна вплоть до температуры Кюри 770°С
Объемно-центрированная кубическая решетка (К О-Ц), магнитен, низкая прочность, высокая плотность.
Σb= 250 Мпа, σ0.2 =120Мпа, Hb = 80-100, δ(относительное удлинение) = 50%, ψ=80%
Аустенит (А )- твердый раствор внедрения углерода в FeЈс предельной концентрацией углерода 2.14% при температуре 1147°С; с понижением температуры до 727°С концентрация углерода понижается до 0.8%
Кубически- гранецентрированный (Г.Ц.К), твердость небольшая, высокие пластичность и вязкость, не магнитен.
Hb = 160, δ(относительное удлинение) = 40-50% - не ржавеет
Цементит (Ц)- химическое соединение Fe3C (карбид железа)
Высокая прочность, Hb>80, низкая плотность, ферромагнитен до температуры Кюри 210°С
С в Fe 6.67%
Имеет высокие твердость и хрупкость.
Пермит (П) – Механическая (эвтектоид) смесь феррита и цементита (Ф+Ц=П), образующаяся при эвтектоидном распаде аустенита (0.8% С)
Высокопрочен, тверд.
727 гр.Цельсия – образуется в процессе распада А! (естественное охлаждение)
Ледебурит (4.3% С) – механическая смесь (эвтектика) аустенита и цементита; ниже температуры 727°С аустенит превращается в перлит, при этом образуется смесь перлита и цементита – превращенный ледебурит.
По химическому составу стали делятся на углеродистые и легированные.
Углеродистые стали могут быть низкоуглеродистыми (С<=0.09…0.25%), среднеуглеродистыми (С<=0.25…0.45%) и высокоуглеродистыми (С<=0.45…0.75%)
Легированные стали условно подразделяются на низколегированную с содержанием легирующих элементов 2.5%; среднелегированные от 2.5-10% и высоколегированные – более 10%
Билет 5. Влияние химических компонентов стали на ее свойства.
На свойства железоуглеродистых сплавов влияет наличие в них постоянных примесей (вредных – серы, фосфора, кислорода, азота, водород; полезных –кремния, марганца и др.) Эти примеси могут попадать в сплав из природных соединений (руд), например, сера и фосфор; из металлического лома – хром, никель и др.; в процессе выплавки и раскисления – углерод, кремний и марганец.
Углерод находится главным образом в связанном состоянии в виде цементита. С увеличение содержания углерода в сталях возрастают твердость, прочность и уменьшается пластичность.
Сера является вредной примесью. Она образует легкоплавкую эвтектику FeS + Fe, которая при кристаллизации сплава располагается по границам зерен и при повторном нагреве расплавляется, что приводит к образованию трещин и надрывов. Это явление носит название красноломкости. Содержание серы дб менее 0.06%
Фосфор ухудшает пластические св-ва сплава, вызывая явление хладноломкости. Его содержание в стали не должно превышать 0,08%.
Азот, кислород и водород присутствуют в сплавах в составе оксидов FeO, SiO2,Al2O3, нитридов Fe4N или в свободном состоянии, при этом они располагаются в дефектных местах в виде молекулярного и атомного газов. Оксиды и нитриды служат концентраторами напряжений и могут снижать механические св-ва(прочность, пластичность).
Водород растворяется в стали при расплавлении. При охлаждении сплава растворимость водорода уменьшается, он накапливается в микропорах под высоким давлением и может стать причиной образования внутренних надрывов в металле (флокенов) и трещин.
Кремний и марганец попадают в железоуглеродистый сплав при его выплавке и в процессе раскисления. Кремний повышает предел текучести и уменьшает склонность к хладноломкости. Марганец образует твердый раствор с железом и немного повышает твердость и прочность феррита
Билет 6. Дефекты кристаллической решетки и их влияния на мех.св-ва металлов.
Дефекты внутреннего строения подразделяют на: точечные, линейные и плоскостные.(рис. 1.2)
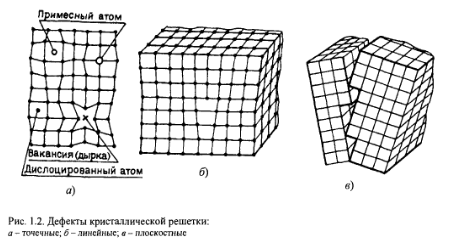
К точечным относятся вакансии (когда отдельные узлы кристаллической решетки не заняты атомами);дислоцированные атомы (если отдельные атомы оказываются в междоузлиях) или примесные атомы,количество которых даже в чистых металлах велико. Около таких дефектов решетка будет упруго искаженной на расстоянии одного-двух периодов (рис 1.2 а). Хотя относительная концентрация точечных дефектов невелика, все же это может вызвать большие изменения физических свойств кристалла. Например, тысячные доли атомного процента примесей к чистым полупроводниковым кристаллам изменяют их электрическое сопротивление в 105 – 106 раз.
Линейные дефекты малы в двух измерениях и достаточно велики в третьем. К таким дефектам относятся смещение атомных плоскостей или дислокаций и цепочки вакансий (рис. 1.2 б). Важнейшими свойствами таких дефектов являются их подвижность внутри кристалла и активное взаимодействие между собой и с другими дефектами. Плотность дислокаций в кристаллах велика: в недеформированных кристаллах их количество на 1 см2 достигает 106 -108; при пластической деформации происходит возникновение новых дислокаций, и это число может увеличиться на несколько порядков – до 1012.
Плоскостные (двухмерные ) дефекты характерны для поликристаллических материалов, т.е для материалов, состоящих из большого количества кристаллов, различно ориентированных в пространстве. Границы между ними обычно представляют собой скопление дислокаций (рис 1.2 в). Плоскостные дефекты малы только в одном направлении; в других они могут достигать размеров кристалла.
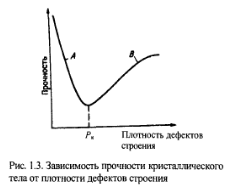
Влияние дефектов строения на прочностные характеристики металлов не однозначно. Если прочность практически бездефектных кристаллов, так называемых «усов», очень велика (рис. 1.3), то увеличение плотности дефектов до определенного количества приводит к ее резкому снижению (ветвь А). Точно Ркхарактеризует прочность металлов, которые принято называть технически чистыми. Дальнейшее увеличение плотности дефектов, например, введением в расплав легирующих компонентов, или специальными методами искажения кристаллической решетки повышает реальную прочность металлов (ветвь В)
Дефекты оказывают влияние на протекание процессов диффузии и самодиффузии , которые определяют скорость хим.реакций в тв. теле, а так же ионную проводимость кристаллов.
Билет 7. Сталь. Классификация сталей. Сталь - деформируемый (ковкий) сплав железа с углеродом (до 2,14%) и другими элементами. Получают, главным образом, из смеси чугуна со стальным ломом в кислородных конвертерах, мартеновских печах и электропечах. Сплав железа с углеродом, содержащий более 2,14% углерода, называют чугуном.
Классификация сталей и сплавов производится:
- по химическому составу;
- по структурному составу;
- по качеству (по способу производства и содержанию вредных примесей);
- по степени раскисления и характеру затвердевания металла в изложнице;
- по назначению.
По химическому составу — углеродистые и легированные. По концентрации углерода те и другие подразделяют на низкоуглеродистые (<0,3 % С), средне-углеродистые (0,3—0,6 %)С и высокоуглеродистые (>0,6 % С).
Для улучшения технологических свойств стали легируют. Легированной называется сталь, в которой, кроме обычных примесей, содержатся специально вводимые в определенных сочетаниях легирующие элементы (Cr, Ni, Mo, Wo, V, Al, B, Ti и др.), а также Мn и Si в количествах, превышающих их обычное содержание как технологических примесей (1% и выше). Как правило, лучшие свойства обеспечивает комплексное легирование. По количеству введенных элементов их разделяют на низко-, средне- и высоколегированные (содержание легирующих элементов до 5 %, от 5 до 10 % и более 10 % соответственно).
Углерод повышает прочность, понижает пластичность, ухудшает свариваемость.
По качеству — стали обыкновенного качества, качественные, высококачественные и особокачественные. Под качеством стали понимают совокупность свойств, определяемых металлургическим процессом ее производства.
Однородность химического состава, строения и свойств стали, а также ее технологичность во многом зависят от содержания газов (кислорода, водорода, азота) и вредных примесей — серы и фосфора.
Стали обыкновенного качества содержат до 0,055 % S и 0,045 % Р, качественные — не более 0,04 % S и 0,035 % Р, высококачественные — не более 0,025 % S и 0,025 % Р, особокачественные — не более 0,015 % S и 0,025 % Р.
По степени раскисления и характеру затвердевания — стали спокойные, полуспокойные и кипящие.
Спокойные стали раскисляют марганцем, кремнием и алюминием. Они содержат мало кислорода и затвердевают спокойно без газовыделения.
Кипящие стали раскисляют только марганцем.
Полуспокойные стали по степени раскисления занимают промежуточное положение между спокойными и кипящими.
По прочности – Стали обычной прочности (σт=24кН/см^2; σвр=38кН/см^2; δ=25-27%); повышенной прочности (σт=34кН/см^2; σвр=45кН/см^2; δ=16-18%); высокой прочности (σ0,2=44кН/см^2; σвр=60кН/см^2; δ=14-16%).
Билет 8. Чугун. Классификация чугунов. Чугун — сплав Fe (основа) с С (обычно 2...4 %), содержащий постоянные примеси (Si, Mn, S, Р), а иногда и легирующие элементы (Cr, Ni, V. А1 и др.); как правило, хрупок.
Чугуны: - белые. Углерод находится в химически связанном состоянии. Белые чугуны редко используются в народном хозяйстве в качестве конструкционных материалов, так как из-за большого содержания цементита очень хрупкие и твердые, с трудом отливаются и обрабатываются инструментом. Из них делают детали гидромашин, пескометов и других конструкций, работающие в условиях повышенного абразивного изнашивания. Для увеличения износостойкости белые чугуны легируют хромом, ванадием, молибденом и другими карбидообразующими элементами.
- серые. Углерод в свободном состоянии. Структура серого (литейного) чугуна состоит из металлической основы с графитом пластинчатой формы, вкрапленным в эту основу. Такая структура образуется непосредственно при кристаллизации чугуна в отливке в соответствии с диаграммой состояния системы Fe—С (стабильной). Причем, чем больше углерода и кремния в сплаве и чем ниже скорость его охлаждения, тем выше вероятность кристаллизации по этой диаграмме с образованием графитной эвтектики. При низком содержании углерода и кремния чугун модифицируют небольшими дозами некоторых элементов (например, алюминий, кальций, церий). На долю серого чугуна с пластинчатым графитом приходится около 80 % общего производства чугунных отливок. Серые чугуны обладают высокими литейными качествами (жидкотекучесть, малая усадка, незначительный пригар металла к форме и др.), хорошо обрабатываются и сопротивляются износу, однако из-за низких прочности и пластических свойств в основном используются для неответственных деталей.
- ковкие. Хлопьевидный графит. Ковкие чугуны с хлопьевидной формой графита получают из белых доэвтектических чугунов, подвергая их специальному графитизирующему отжигу. Графитизирующий отжиг белого чугуна основан на метастабильности цементита и состоит обычно из двух стадий: Первая стадия (950...1050 °С) подбирается по длительности такой, чтобы весь цементит, находящийся в структуре отливки, распался на аустенит и хлопьевидный графит. Процесс графитообразования облегчается при модифицировании (например, алюминием и бором). Чугун, полученный таким образом, называется модифицированным.
На второй стадии графитизирущего отжига при температуре эвтектоидного превращения формируется металлическая основа ковкого чугуна. В зависимости от режимов охлаждения ковкие чугуны могут иметь перлитную (непрерывное охлаждение), ферритную (очень медленное охлаждение в интервале 760...720 °С или изотермическая выдержка при 720...700 °С) или ферритно-перлитную (сокращение продолжительности второй стадии отжига) металлические основы. Для получения в модифицированном ковком чугуне перлитной основы рекомендуется увеличивать содержание марганца, хрома и некоторых других элементов, которые повышают устойчивость цементита к распаду на феррит и пластинчатый графит в области температур эвтектоидного превращения.
Ковкие чугуны, обладая высокими пластическими свойствами, находят применение при изготовлении разнообразных тонкостенных (до 50 мм) деталей, работающих при ударных и вибрационных нагрузках, — фланцы, муфты, картеры, ступицы и др.
Для повышения твердости, износостойкости и прочности изделий из ковкого чугуна иногда применяют нормализацию или закалку. Закалка с последующим высоким отпуском позволяет получить структуру зернистого перлита.
- высокопрочный. Шаровидный графит. Высокопрочный чугун (ЧШГ — чугун с шаровидным графитом) получают модифицированием жидкими присадками (0,1...0,5 °о магния от массы обрабатываемой порции чугуна, 0,2...0,3 °о церия, иттрия и некоторых других элементов). При этом перед вводом модификаторов необходимо снизить содержание серы до 0,02...0,03 %.
Рекомендуемый химический состав высокопрочного чугуна (2,7...3,7 % С; 0,5...3,8 % Si) выбирается в зависимости от толщины стенок отливки (чем тоньше стенка, тем больше углерода и кремния).
Структура высокопрочного чугуна состоит из металлической основы (феррит, перлит) и включений графита шаровидной формы. Высокопрочные чугуны обладают хорошими литейными и потребительскими свойствами (обрабатываемость резанием, способность гасить вибрации, высокая износостоикость и др.). Они используются для массивных отливок взамен стальных литых и кованых деталей. Для повышения механических свойств (пластичности и вязкости) и снятия внутренних напряжений отливки подвергают термической обработке (отжигу, нормализации, закалке и отпуску).
Билет 9. Термическая обработка сталей. Термическая (тепловая) обработка состоит в изменении структуры металлов и сплавов путем нагревания их и последующего охлаждения с той или иной скоростью; при этом достигаются существенные изменения свойств при том же химическом составе сплава (термическая обработка делается для получения прочности, при сохранении пластичности).
При рассмотрении разных видов термообработки железо-углеродистых сплавов (стали, чугуны) используются следующие условные обозначения критических точек этих сплавов.
К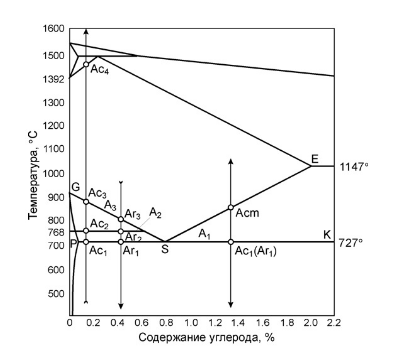 ритические
точки А1 лежат на линии PSK (727 °C). Критические
точки А2 находятся на линии МО (768 °C).
Критические точки А3 лежат на линии GS,
а критические точки Аcm — на линии SE.
Вследствие теплового гистерезиса
превращения при нагреве и охлаждении
проходят при разных температурах.
Поэтому для обозначения критических
точек при нагреве и охлаждении используют
дополнительные индексы: буквы «с» в
случае нагрева и «r» в случае охлаждения.
Например, АС1, АС3, Аr1, Аr3.
ритические
точки А1 лежат на линии PSK (727 °C). Критические
точки А2 находятся на линии МО (768 °C).
Критические точки А3 лежат на линии GS,
а критические точки Аcm — на линии SE.
Вследствие теплового гистерезиса
превращения при нагреве и охлаждении
проходят при разных температурах.
Поэтому для обозначения критических
точек при нагреве и охлаждении используют
дополнительные индексы: буквы «с» в
случае нагрева и «r» в случае охлаждения.
Например, АС1, АС3, Аr1, Аr3.
Ас1 – превращение перлита в аустенит [Feα + Fe3C] → Feγ;
Аr1 – превращение аустенита в перлит Feγ → [Feα + Fe3C];
Ас2 – превращение магнитного феррита в немагнитный Feα → Feβ;
Аr2 – превращение немагнитного феррита в магнитный Feβ → Feα;
Ас3 – переход последних кристаллов Feα в Feγ;
Аr3 – появление первых кристаллов Feα из Feγ;
Асm –переход Fe3C (II) ↔ Feγ.
аустенит – твердый раствор углерода в γ- железе (Feγ); мартенсит(0-200град.); бейнит (200-250град); троостит(500-580град.); сорбит (590-640град.); перлит (650-670град.).
Термическая обработка стали: термическое воздействие (отжиг, закалка, отпуск), тепловые воздействия ТХО, тепловые воздействия ТМО.
Термическая обработка, заключающаяся в нагреве металла, находящегося в результате каких-либо предшествующих воздействий в неравновесном состоянии, и приводящая его в более равновесное состояние, называется отжигом. Охлаждение после отжига производится вместе с печью. Нагрев при отжиге может производиться ниже и выше температур фазовых превращений в зависимости от целей отжига. Отжиг, при котором нагрев и выдержка металла производится с целью приведения его в однородное (равновесное) состояние за счет уменьшения (устранения) химической неоднородности, снятия внутренних напряжений и рекристаллизации называется отжигом первого рода. Его проведение не связано с прохождением фазовых превращений. Он возможен для любых металлов и сплавов.
В зависимости от того, какие отклонения от равновесного состояния устраняются существуют следующие разновидности отжига 1-го рода: гомогенизационный, рекристаллизационный и уменьшающий напряжения отжиг.
Гомогенизационный (диффузионный) отжиг — это термическая обработка, при которой главным процессом является устранение последствий дендритной ликвации (химической неоднородности).
Рекристаллизационный отжиг — это термическая обработка деформированного металла, при которой главным процессом является рекристаллизация металла.
Отжиг, уменьшающий напряжения — это термическая обработка, при которой главным процессом является полная или частичная релаксация остаточных напряжений.
Отжиг, при котором нагрев производится выше температур фазовых превращений с последующим медленным охлаждением для получения структурно равновесного состояния, называется отжигом второго рода или перекристаллизацией.
Если после нагрева выше температур фазовых превращений охлаждение ведется не в печи, а на воздухе, то такой отжиг называется нормализацией, которая является переходной ступенью от отжига к закалке. Существуют два вида закалки: закалка без полиморфного превращения и закалка с полиморфным превращением. Закалка без полиморфного превращения заключается в нагреве металла или сплава до температур растворения избыточной фазы, выдержке при этой температуре с целью получения однородного пересыщенного твердого раствора, и в фиксации полученного пересыщенного твердого раствора за счет быстрого охлаждения в сильном охладителе (вода, масло и др.). В результате этого сплав имеет структурно неустойчивое состояние. Этот вид закалки характерен для сплавов алюминия с медью — дуралюминов.
Термическая обработка, заключающаяся в нагреве металла выше температур фазовых превращений (на 30-50 град.) с последующим быстрым охлаждением для получения структурно неравновесного состояния, называется закалкой с полиморфным превращением. Этот вид закалки характерен для сплавов железа с углеродом (стали). После закалки в стали образуется структура пересыщенного твердого раствора углерода в a -железе, которая называется мартенситом. Состояние закаленного сплава характеризуется особой неустойчивостью. Процессы, приближающие его к равновесному состоянию, могут идти даже при комнатной температуре и резко ускоряются при нагрева.
Термическая обработка, представляющая собой нагрев закаленного сплава ниже температур фазовых превращений (ниже АС1) для приближения его структуры к более устойчивому состоянию, называется отпуском. Отпуск является операцией, проводимой после закалки стали (закалки с полиморфным превращением). Между отпуском и отжигом 1-го рода много общего. Разница в том, что отпуск — всегда вторичная операция после закалки.
Самопроизвольный отпуск, происходящий после закалки без полиморфного превращения, в результате длительной выдержки при комнатной температуре, или отпуск при сравнительно небольшом подогреве, называется старением.
Тепловые воздействия ТХО: цементация, азотирование, борирование, ционирование.
Тепловые воздействия ТМО: высокотемпературное ВТМО, низкотемпературное НТМО, механ.-термич. обраб.
Билет 10. Сортамент стального проката

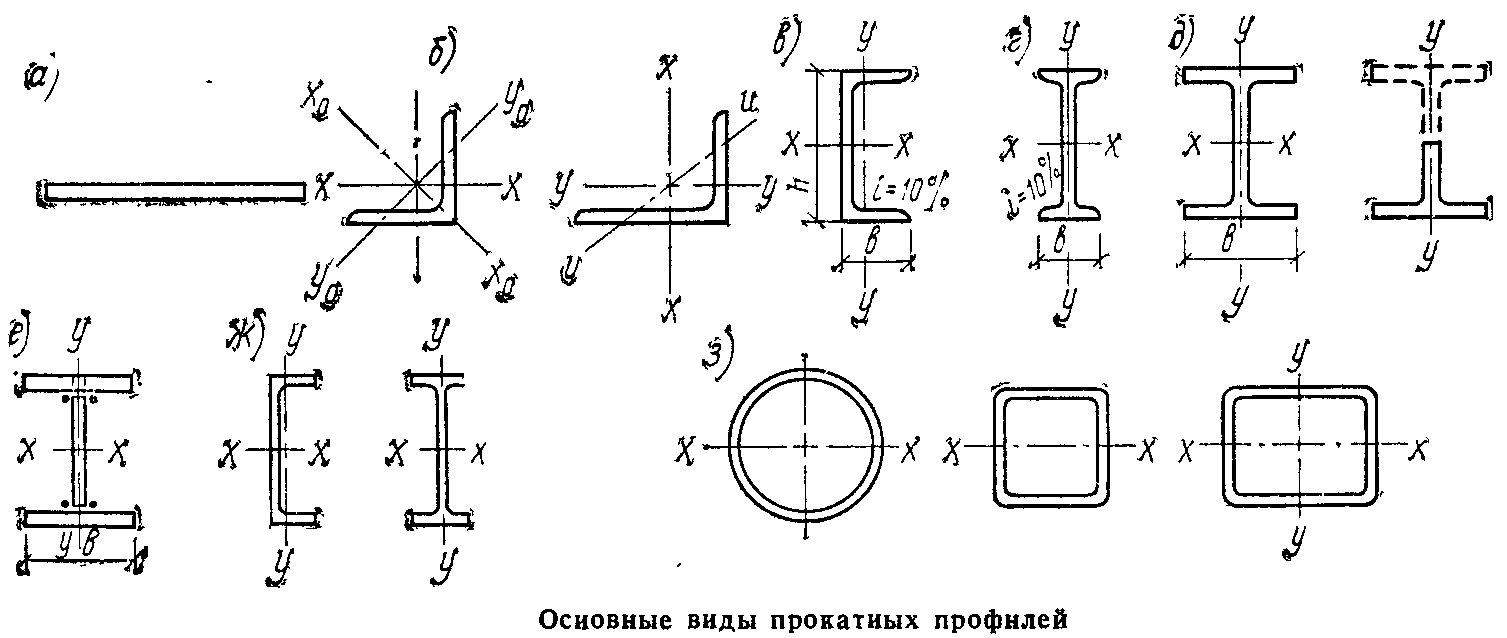
Сталь листовая: сталь толстолистовая, сталь тонколистовая, сталь широкополочная универсальная.
Уголковые профили: равнополочные уголки, неравнополочные уголки
Швеллеры: геом. хар-ки опред-ся номером, кот. соотв. высоте стенки [см]. Сортамент включает шв. с уклоном внутренних граней полок и шв. с параллельными гранями полок.
Двутавры: балки двутавровые обыкновенные (с уклоном внутр. граней полок), балки двутавровые широкополочные (с парал. гранями полок). Двутавры – основной балочный профиль.
Тонкостенные профили: тонкостенные двутавры и швеллеры (прокатываются на непрерывном стане с особо тонкими стенками). Экономичнее обычных профилей на 20%.
Трубы: круглые (горячекатаные и электросварные), п/у и квадратного сечения (электросварные)
Холодногнутые профили: равнополочные и неравнополочные уголки; швеллеры «С»-образные, зетовые, замкнутые, кв. и п/у сечения.
Разные профили: профили для оконных и фонарных переплётов, крановые рельсы, стальные канаты, проволока, профилированный настил
