
- •Методические указания к лабораторной работе № 1
- •Новороссийск
- •Председатель методического совета нпи________________ в.В. Дьяченко Содержание
- •Общие правила работы в лабораториях во время занятий с учащимися [1]
- •Требования безопасности при работе с кислотами и щелочами [1]
- •Растворять твердые щелочи следует путем медленного прибавления их небольшими кусочками к воде при непрерывном перемешивании. Кусочки щелочи нужно брать только щипцами.
- •Правила безопасности работы с химической посудой и ампулами [1]
- •Дисперсные системы [2] Основные определения
- •Дисперсность
- •Классификация дисперсных систем [2, 5 – 7] Классификация по дисперсности
- •Классификация по агрегатному состоянию дисперсной фазы и дисперсионной среды
- •Классификация, учитывающая различие в форме частиц
- •Классификация по термодинамической устойчивости и характеру образования
- •Получение дисперсных систем [2, 5]
- •Условия образования новой фазы
- •Влияние способа получения на строение порошковых частиц
- •Строение коллоидной мицеллы
- •«Получение золей и их характеристика»
- •Выполнение работы
- •Контрольные вопросы
- •Литература
Условия образования новой фазы
Новая фаза образуется в пересыщенных системах. Осторожно приводя систему к пересыщению, можно добиться того, что при определенной степени пересыщения новая фаза не возникает. О таких системах говорят, что они находятся в метастабильном состоянии, т. е. устойчивы к очень малым воздействиям и претерпевают необратимые изменения при более значительных изменениях параметров.
Первый этап образования новой фазы появление зародышей, являющихся минимальным скоплением новой фазы и находящихся в равновесии со средой. Известны два механизма образования зародышей:
а) гомогенный, при котором новая фаза зарождается в однородной старой фазе;
б) гетерогенный, при котором зарождение происходит в местах неоднородностей фазы.
Примесями, служащими центрами конденсации по гетерогенному механизму, могут быть отдельные пылинки или заряженные частицы.
Образование зародышей по гомогенному механизму объясняется местным повышением концентраций в результате теплового движения молекул (флуктуации концентраций).
Термодинамические расчеты, проведенные Дж. У. Гиббсом и М. Фольмером, показывают, что работа, затраченная на образование равновесного зародыша по гетерогенному механизму, меньше, чем по гомогенному. Этот вывод подтверждается экспериментально: в системе, содержащей гетерогенные примеси, конденсация протекает значительно легче.
Второй этап конденсационного образования новой фазы рост кристаллов. Скорость роста кристаллов определяется разностью действующей концентрации вещества в растворе и равновесной концентрации этого вещества при той же температуре. Чем больше разность, тем быстрее растут кристаллы.
Скорость роста кристаллов может значительно замедляться примесями, содержащимися в системе. Замедляющее действие примесей связано с их способностью захватываться поверхностью растущего кристалла. Располагаясь на поверхности, они затрудняют доступ молекул или ионов кристаллизующего соединения.
Влияние способа получения на строение порошковых частиц
Известные способы получения применяемых в промышленности металлических порошков заключаются в том, что куски диспергируемого металла помещают в заполненную диэлектрической жидкостью емкость и посредством электродов или индуктора подают на них импульсы напряжения. Недостатком этих методов является то, что диспергирование в жидкости приводит к загрязнению конечного порошка продуктами реакции металла и жидкости, а в некоторых случаях исходный материал полностью отличается от конечного вещества.
Металлические порошки можно получать и другим способом, который заключается в следующем. Расплавленный металл изливается струями по специальным насадкам из плавильной емкости, а затем распадается на капли.
Формирование капель осуществляется с помощью механических или электромагнитных воздействий. При этом металл должен постоянно находиться в расплавленном состоянии, что связано со значительными техническими трудностями.
Избежать таких трудностей можно, применяя способ безэлектродного электроэрозионного диспергирования в газах. В этом случае (особенно, если диспергирование проводить в инертных газах) полностью исключается возможность химической реакции металла с окружающей средой, вследствие чего конечный и исходный продукты не отличаются по своему составу [9].


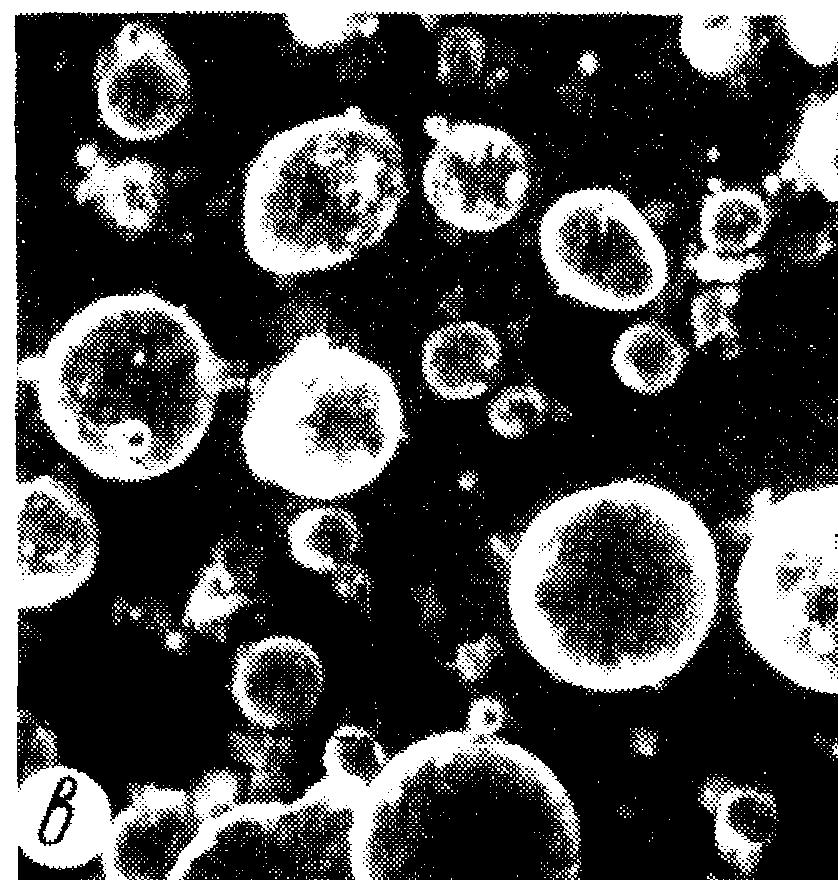

Рисунок 3 – Порошки алюминия (а, б) и меди (б, г), диспергированные в гелии (а – в) и воздухе (г). Увеличение: 108 (а), 120 (б). 528 (в), 300 (г) [9].
Порошки алюмината магния получают прокаливанием смеси чистых оксидов магния и алюминия в присутствии 2 % хлорида магния при температуре 1600 – 1750 оС в течение 4 часов в электропечи. Возможно проведение реакции соосаждения гидроксидов магния и алюминия из растворов алюмината натрия и соли магния, позволяющий получить алюминат магния при температуре около 1000 оС в течение 1 часа. Чтобы получить алюминат магния в виде сферических зерен, суспензию гидроксидов магния и алюминия распыляют через сопло в зону, нагретую до 1050 – 1100 оС [10].


а б
Рисунок 4 – Внешний вид порошка (а) и частицы порошка (б) алюмината магния, полученного прокаливанием при 1400 °С в течение 4 ч в печи. Увеличение: 75 (а), 750 (б) [10].


а б
Рисунок 5 – Внешний вид порошка алюмината магния, полученного распылительным прокаливанием при температуре 1000 (а) и 1600 °С (б). 100 [10].
Методы распыления расплавов позволяют получать порошки металлов и сплавов, частицы которых имеют форму от правильной сферической до осколочной.
В процессе диспергирования расплава образовавшиеся капли металла (пряди) произвольной, неправильной формы под действием сил поверхностного натяжения стремятся принять форму шара, поверхность которого минимальна при постоянном объеме, что соответствует минимуму свободной энергии. При этом форма частиц порошка определяется отношением времени пребывания капли в жидком состоянии ко времени ее сфероидизации. Известны выражения, связывающие длительность охлаждения и сфероидизации капель с физическими свойствами расплава и энергоносителя. Судя по этим соотношениям, чтобы увеличить отклонение формы частиц от сферической, необходимо снижать поверхностное натяжение расплава, повышать его вязкость, увеличивать эффективную плотность энергоносителя и коэффициент теплоотдачи. Последние два условия реализуются при замене газообразного энергоносителя жидким, например водой [11].

Рисунок 6 – форма частиц порошка стали, распыленного водой под давлением 5,6 МПа, 290 [11].
Металлические, например медные, порошки, полученные электрохимическим методом, имеют форму дендритов, рисунок 7.

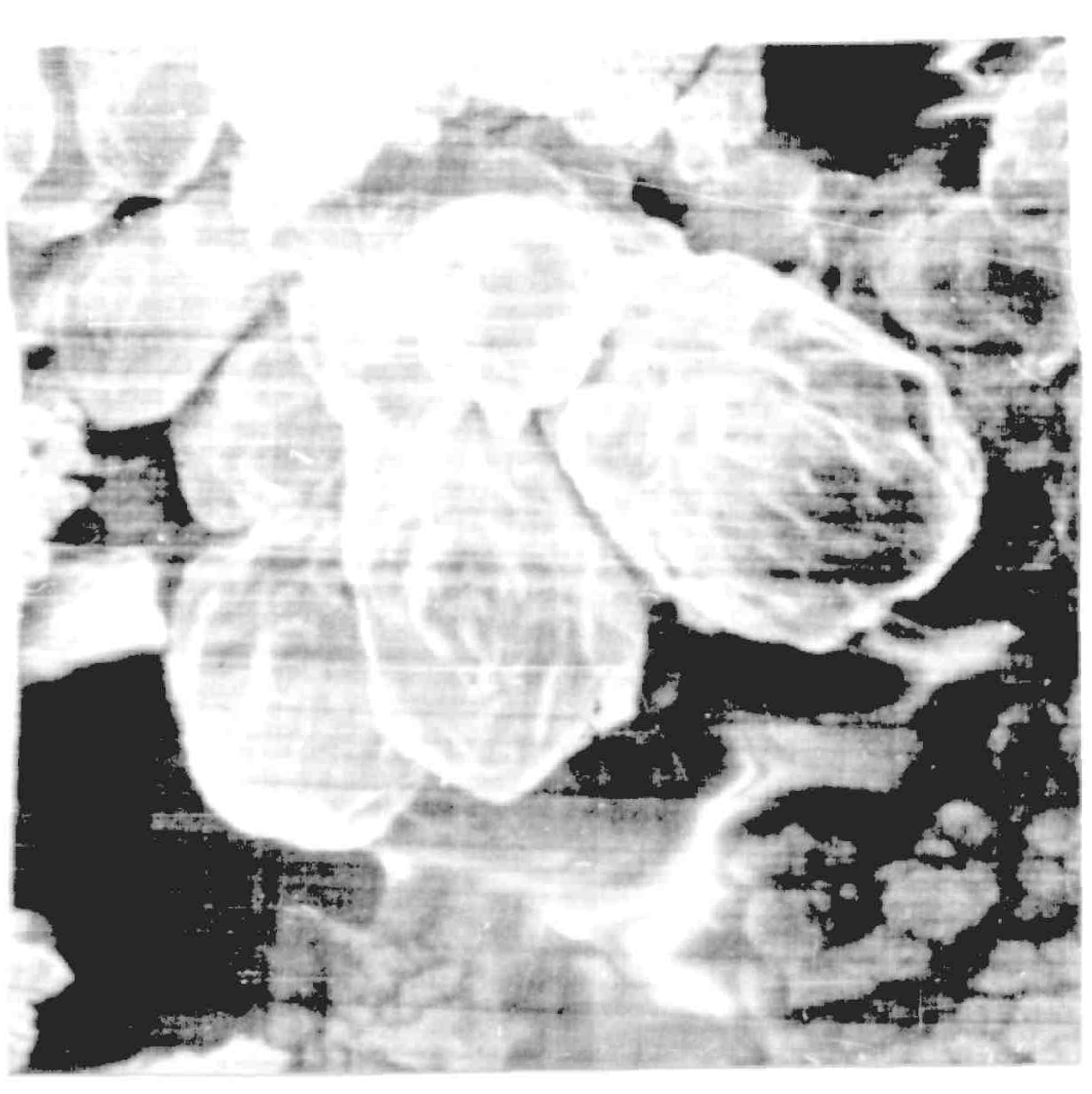
а б
Рисунок 7 – Внешний вид частиц порошка меди марки ПМС-I, (электролитический дендритный осадок)
Увеличение: 500 (а), 1000 (б).
