
1.3. Биосинтез липидов, построенных из изопренильных фрагментов
Вторая важная и весьма разнообразная группа липидов берет свое происхождение от изопентенилпирофосфата и изомерного ему диметилаллилпирофосфата. Схема их образования представлена на Рис. 9 .1.
Исходным соединением и в этом случае является ацетилкофермент А. Первая стадия — образование ацетоацетилкофермента А — является обращением последней стадии деструкции жирных кислот, катализируемой ацетил-СоА-ацетилтрансферазой. За ней следует взаимодействие с метильной группой ацетильного остатка третьей молекулы ацетилкофермента А, причем атакуется атом СЗ кетогруппы ацетоацетильного остатка (стадия 1 Рис. 9 .1). Процесс сопровождается гидролизом тиоэфирной связи между атакующим ацетильным остатком и SH-группой кофермента. Нетрудно заметить, что реакция сходна с образованием лимонной кислоты в цитратсинтазной реакции. Продуктом является в данном случае З-окси-3-метилглутарилкофермент А. Фермент, катализирующий реакцию, называется оксиметилглутарилкофермент А синтаза. Следующая стадия (2) — двукратное восстановление тиоэфирной группы до SH-группы свободного кофермента А и оксигруппы с помощью NADPH — приводит к образованию 3,5-диокси-З-метилвалерата или мевалоната (соль мевалоновой кислоты). Эта стадия катализируется оксиметилглутарилкофермент А редуктазой.
Мевалонат далее подвергается фосфорилированию по 5-оксигруппе с помощью мевалонат киназы и повторному фосфорилированию по фосфату с помощью 5-фосфомевалонат киназы (стадия 3). Фосфорилирующим реагентом в обеих стадиях является АТР. За этим следует декарбоксилирование мевалонат-5-дифосфата, осуществляемое с помощью фермента пирофосфомевалонат декарбоксилазы (стадия 4). В реакции принимает участие АТР, который, по-видимому, является донором фосфата для образования промежуточного З-фосфо-5-дифосфомевалоната, далее декарбоксилирующегося с элиминацией 3-фосфата и образованием изопентенилпирофосфата. Последний с помощью изопентенилдифосфат--изомеразы частично превращается в диметилаллилпирофосфат (стадия 5). Эти два пирофосфата являются предшественниками ряда линейных и циклических гидрофобных структур.
Ниже основное внимание будет уделено чрезвычайно важному для животных и человека и наиболее сложному пути превращения этих предшественников — биосинтезу стероидов.
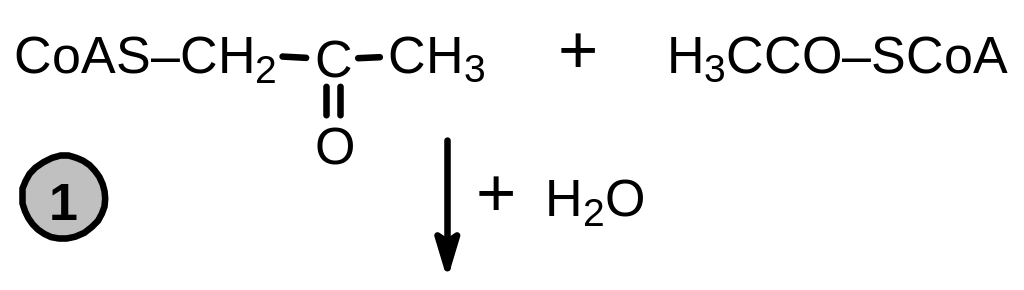
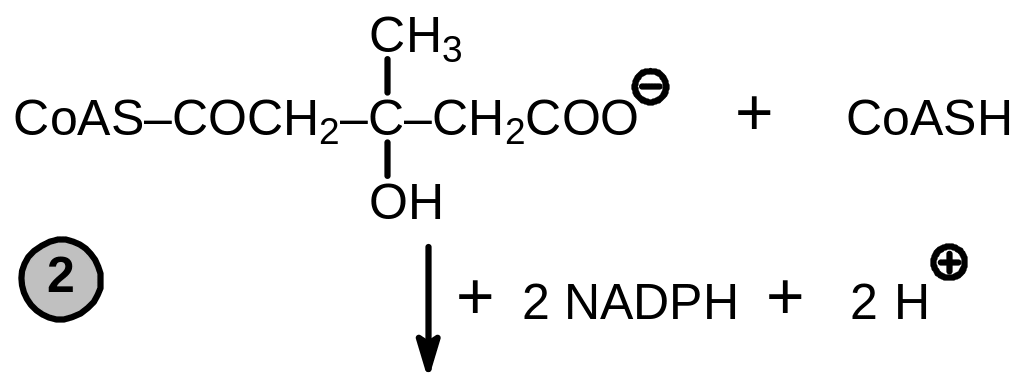
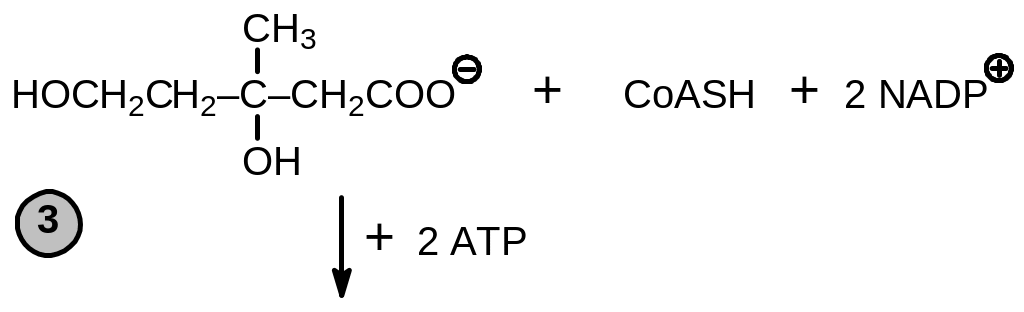

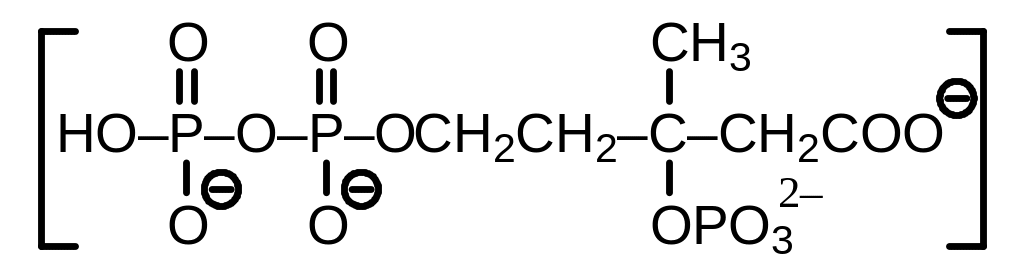
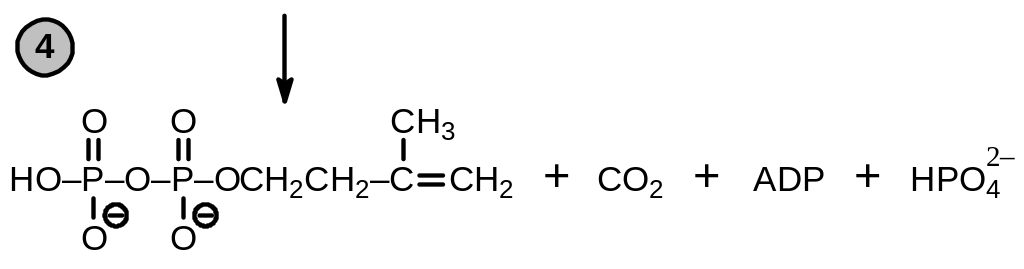
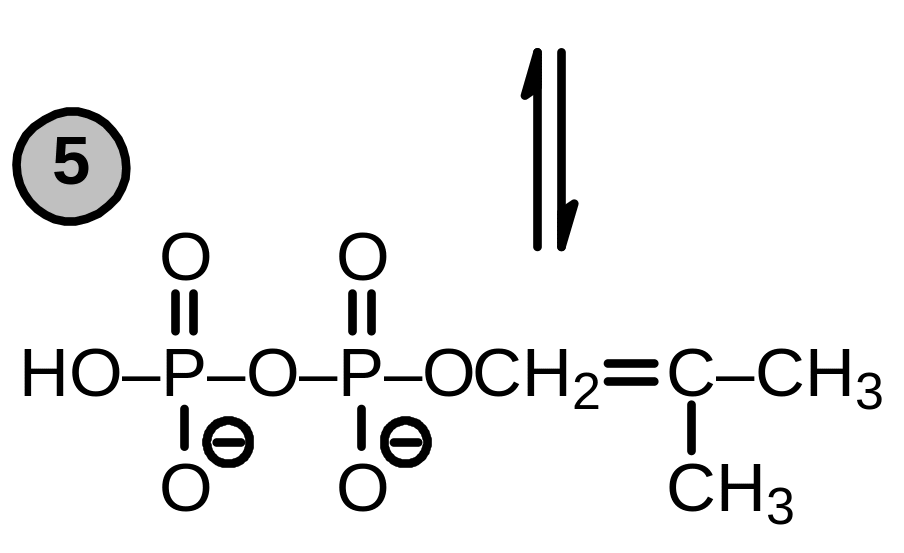
Рис. 9.1. Схема образования изопентилпирофосфата и димитилаллилпирофосфата. Номера на схеме соответствуют тескту
Процесс начинается с взаимодействия изопентенил- и диметилаллилпирофосфатов по реакции, которая приводит к образованию гераниолпирофосфата и катализируется диметилаллилтрансферазой. Далее совершенно аналогичная реакция с еще одной молекулой изопентенилпирофосфата, катализируемая геранилтран-сферазой, приводит к фарнезилпирофосфатуError: Reference source not found.
Дальнейшее превращение состоит в соединении двух углеводородных остатков фарнезилпирофосфата с образованием углеводорода сквалена.
Схема процесса образования сквалена приведена на Рис. 9 .2. Промежуточным соединением является прескваленпирофосфат, который образуется при участии фермента прескваленсинтазы. В своей полимерной форме этот фермент способен также проводить реакцию восстановления двойной связи в пресквалене с помощью NADPH, что приводит к образованию сквалена.
Характерная для стероидов циклопентанпергидрофенантреновая структура образуется в результате сложного процесса, который претерпевает 2,3-эпоксисквален, превращающийся при этом в соединение, имеющее характерную для стероидов систему конденсированных гетероциклов — ланостерин. На Рис. 9 .3 представлены углеродные скелеты сквалена, 2,3-эпоксисквалена и ланостерина. У последнего нумерация атомов приведена в виде, принятом для стероидов, и поэтому не совпадает с естественной нумерацией для сквалена. Из сравнения приведенных структур видно, что в ходе реакции, катализируемой скваленоксидициклазои, происходит атака атома С2 сквалена на атом С7, атома С6 на атом С11, атома С10 на атом С15 и атома С14 на атом С18.
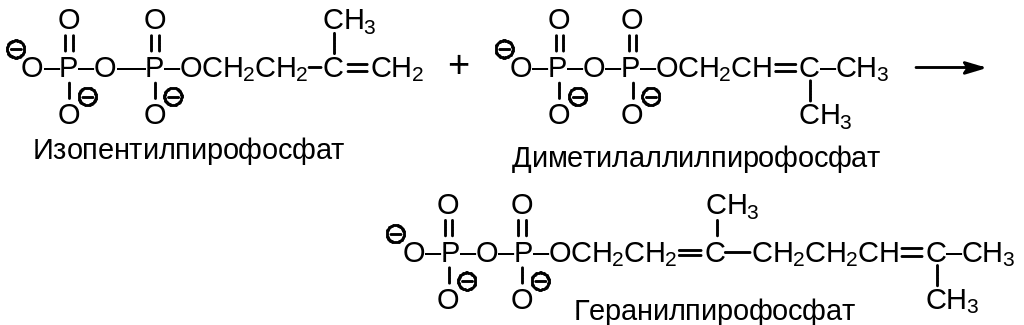
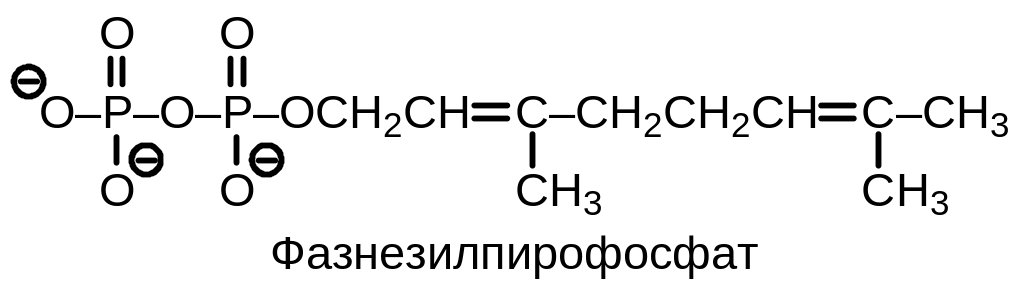
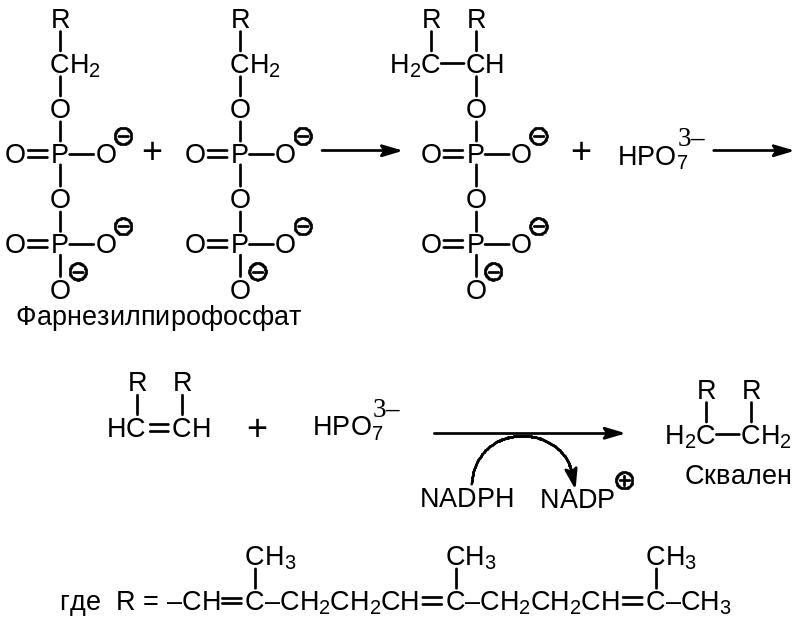
Рис. 9.2. Схема образования сквалена
Этот процесс нетрудно представить себе как последовательное или синхронное взаимодействие карбокатионов, образующихся при атакующих атомах, и индуцированное протонированием эпоксидного кольца. Однако, судя по конечному итогу, циклизация дополнительно осложнена миграцией метальной группы из положения 10 по нумерации для сквалена (положение 8 в стероидной нумерации) в положение 14 и двойной связи из положения С18–С19 в положение С10–С11 в нумерации для сквалена (С8–С9 в стероидной нумерации). Процесс катализируется ферментом ланостеринсинтазой.
Если сравнить структуру ланостерина со структурой холестерина и некоторых половых стероидных гормонов, то видно, что уже для получения холестерина из ланостерина нужны довольно глубокие и заведомо многостадийные превращения.
Рис.
9.3. Структура
сквалена, 2,3-эпоксисквалена и ланостерина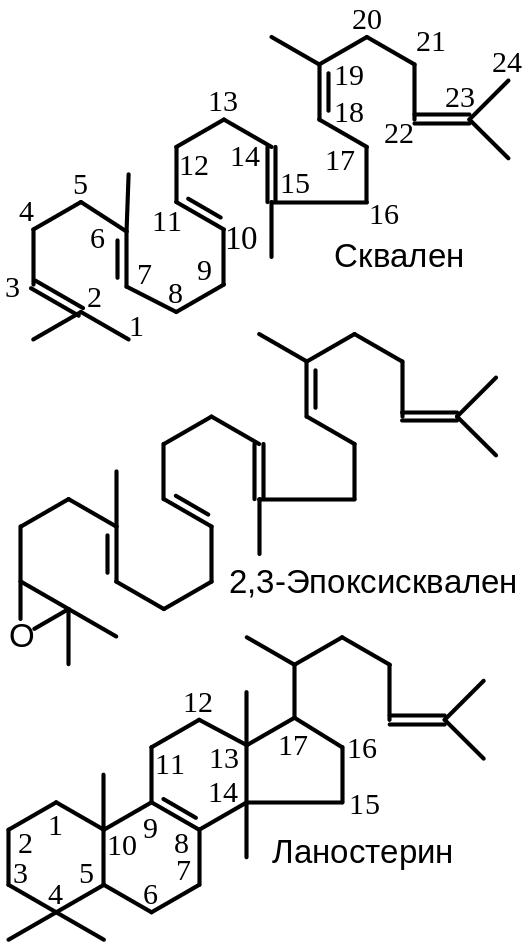
Как уже говорилось, изопентенильные фрагменты используются для образования широкого спектра гидрофобных структур.
Полимеризация изопентенилпирофосфата приводит к образованию природного каучука в каучуконосных растениях, которое катализируется ферментом каучук цис-полипренил-цис-трансферазой. Наконец, присоединение нескольких изопентенильных фрагментов используется для придания гидрофобности ряду важных молекул, участвующих в переносе электронов и функционирующих в мембранных системах: пластохинону, убихинону, хлорофиллу (боковой радикал фитол).
