
- •Реферат
- •Содержание
- •Глава 1. Экстракция кислот реагентами группы диантипирилметана в органические растворители (литературный обзор) 6
- •1.1. Свойства реагентов группы диантипирилметана 6
- •1.2. Закономерности экстракции кислот реагентами группы диантипирилметана в органические растворители 10
- •Глава 2.Условия проведения и техника эксперимента 28
- •2.1. Реактивы, растворы и их приготовление 28
- •2.2. Приборы 29
- •2. 3.Техника эксперимента 29
- •Глава 3. Исследование совместной экстракции хлороводородной и бензойной кислот диантипирилалканами в системе без органического растворителя 30
- •Список сокращений
- •Введение
- •Глава 1. Экстракция кислот реагентами группы диантипирилметана в органические растворители (литературный обзор)
- •1.1. Свойства реагентов группы диантипирилметана
- •1.2. Закономерности экстракции кислот реагентами группы диантипирилметана в органические растворители
- •1.2.1. Экстракция минеральных кислот
- •1.2.1.1. Экстракция фтороводородной кислоты
- •1.2.1.2. Экстракция хлороводородной кислоты
- •1.2.1.3. Экстракция других галогенводородных кислот
- •1.2.1.4. Экстракция хлорной кислоты
- •1.2.1.5. Экстракция азотной и серной кислот
- •1.2.2. Экстракция органических кислот
- •1.2.2.1. Экстракция щавелевой кислоты
- •1.2.2.2. Экстракция замещенных уксусных кислот
- •1.2.2.3. Экстракция нафталин-2-сульфокислоты из бинарных смесей
- •Глава 2.Условия проведения и техника эксперимента
- •2.1. Реактивы, растворы и их приготовление
- •2.2. Приборы
- •2. 3.Техника эксперимента
- •Глава 3. Исследование совместной экстракции хлороводородной и бензойной кислот диантипирилалканами в системе без органического растворителя
- •Список литературы
1.2. Закономерности экстракции кислот реагентами группы диантипирилметана в органические растворители
1.2.1. Экстракция минеральных кислот
1.2.1.1. Экстракция фтороводородной кислоты
Фтороводородная кислота является слабой кислотой (Кдис = 6,7·10-4), степень её диссоциации в 1 и 10 моль/л растворах равна соответственно 2,5 и 0,8 %. Характерной особенностью HF является наличие водородных связей между молекулами, которые приводят к образованию прочных ассоциатов [11]. Такие особенности фтористоводородной кислоты сказываются на ее экстракции производными пиразолона в органические растворители.
Экстракция HF хлороформным раствором ДАМ возрастает монотонно (табл. 1.2). При кислотности водной фазы до 8 моль/л НF ДАМ и ГДАМ практически полностью находятся в органической фазе. При концентрации HF в водной фазе, равной 4 – 4,5 моль/л, в органическую фазу переходит однокислотная соль ДАМ·HF. Дальнейшее увеличение кислотности водной фазы приводит к повышенному извлечению HF и при СHF = 8,0 моль/л в хлороформ переходит более чем двухкислотная соль реагента.
Таблица 1.2
Экстракция фтороводородной кислоты растворами ДАА в хлороформе
(Vв = Vo = 20 мл; [ДАА] = 0,1 моль/л)
[HF]исх, моль/л |
Отношение HF:R в экстракте |
||
ДАМ |
ПДАМ |
ГДАМ |
|
0,25 |
0,045 |
0,06 |
0,045 |
0,50 |
0,085 |
0,10 |
0,10 |
1,0 |
0,022 |
0,26 |
0,21 |
2,0 |
0,52 |
0,56 |
0,43 |
4,0 |
0,86 |
2,08 |
1,83 |
6,0 |
1,49 |
3,40 |
3,13 |
8,0 |
2,33 |
4,08 |
4,42 |
Гомологи ДАМ, которые являются более сильными основаниями, экстрагируют значительно большее количество HF. Так, ПДАМ при концентрации HF в водной фазе 4 моль/л извлекает два эквивалента кислоты R·2HF (где R – ПДАМ), а при 8 моль/л – более четырех. Реагент с большим алкильным радикалом (ГДАМ) также обеспечивает извлечение двух и более кислотных фторидов. При концентрации HF, равной 8 моль/л, отношение HF:ГДАМ > 4:1. Учитывая слабые кислотные свойства фтористоводородной кислоты, невозможно допустить существования поликислотных солей, поэтому значительная экстракция фтористоводородной кислоты обусловлена извлечением ассоциатов RH+F-∙∙∙(HF∙∙∙HF)n.
В работе [11] приведены сведения об экстракции фтороводородной кислоты ДАМ и ГДАМ в 1,2-дихлорэтан. Как и следовало ожидать, максимальное отношение HF:R в экстракте достигается при меньших концентрациях HF в водной фазе по сравнению с хлороформом. Так, для ДАМ отношение HF:R = 3:2 наблюдается при HFв = 5 моль/л, аналогичное отношение – для ГДАМ – при 3 моль/л. Поэтому лучшим экстрагентом для извлечения фтористоводородной кислоты является дихлорэтановый раствор ГДАМ [1].
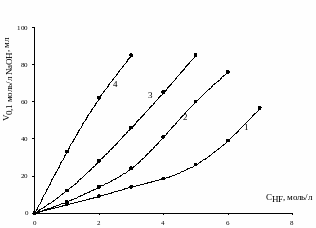
Рис.1.1. Экстракция HF ДАМ и ГДАМ в хлороформ и 1,2-дихлорэтан (СДАА = 0,0125 моль/л, Vо = Vв = 25 мл). 1, 3 – ДАМ и ГДАМ в хлороформ; 2, 4 – ДАМ и ГДАМ в 1,2-дихлорэтан
С практической точки зрения наиболее значительными следует считать результаты экстракции кислот из смешанных растворов HF – HCl и HF – H2SO4.
В работе [7] была изучена экстракция фтороводородной кислоты ДАМ и его гомологами в 1,2-дихлорэтан из ее смесей хлороводородной кислотой. Концентрация фтороводородной кислоты была постоянной и равной 2 моль/л, а концентрация хлороводородной кислоты менялась от 0,1 до 8,0 моль/л. Оказалось, что в некотором интервале кислотности присутствие фтороводородной кислоты практически не влияет на извлечение хлороводородной кислоты, а вот увеличение концентрации хлороводородной кислоты приводило к подавлению экстракции фтороводородной кислоты.
Таблица 1.3
Экстракция HCl и HF из их смесей растворами ДАА в хлороформе
(СДАА = 0,1 моль/л, СHF = 2 моль/л; Vв = Vо = 20 мл)
[HCl]исх.(в) моль/л |
Содержание кислоты в экстракте в мл 0,1 моль/л |
|||||
ДАМ |
ПДАМ |
ГДАМ |
||||
HCl |
HF |
HCl |
HF |
HCl |
HF |
|
0,25 |
4,25 |
7,53 |
0,00 |
16,6 |
6,5 |
14,5 |
0,50 |
7,25 |
6,90 |
16,2 |
11,5 |
0,2 |
23,7 |
1,0 |
11,23 |
6,10 |
29,0 |
8,2 |
5,2 |
26,2 |
2,0 |
25,80 |
4,93 |
39,4 |
9,3 |
12,5 |
25,3 |
4,0 |
25,39 |
3,22 |
40,6 |
6,0 |
17,3 |
23,9 |
6,0 |
7,97 |
4,30 |
41,1 |
8,4 |
17,3 |
25,0 |
8,0 |
0,00 |
1,43 |
41,0 |
10,4 |
26,2 |
23,3 |
Таблица 1.4
Экстракция H2SO4 и HF из их смесей растворами ДАА (0,1 моль/л)
в хлороформе (СHF = 2 моль/л; Vв = Vо = 20 мл)
[H2SO4]исх.(в), моль/л |
Содержание кислоты в экстракте в мл 0,1 моль/л |
|||||||
ДАМ |
ПДАМ |
ГДАМ |
||||||
H2SO4 |
HF |
H2SO4 |
HF |
H2SO4 |
HF |
|||
0,125 |
2,7 |
3,9 |
0,0 |
11,1 |
3,45 |
3,6 |
||
0,25 |
4,6 |
3,3 |
2,65 |
9,8 |
1,25 |
10,7 |
||
0,50 |
3,9 |
2,8 |
2,30 |
11,4 |
0,05 |
13,2 |
||
1,0 |
4,2 |
2,8 |
14,80 |
8,3 |
0,05 |
30,4 |
||
2,0 |
5,2 |
3,5 |
30,20 |
9,1 |
16,5 |
24,5 |
||
3,0 |
0,0 |
4,4 |
30,70 |
9,1 |
19,3 |
24,8 |
||
4,0 |
1,9 |
5,2 |
31,40 |
14,3 |
22,7 |
17,2 |
||
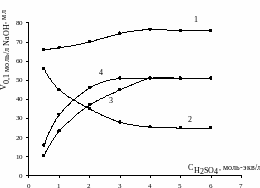
Рис. 1.2. Влияние концентрации серной кислоты на экстракцию фтороводородной кислоты ГДАМ в 1,2-дихлорэтан (СГДАм = 0,0125 моль/л, Vо = Vв = 25 мл, СHF = 2 моль/л). 1 – общая кислотность; 2 – содержание HF в экстракте; 3 – содержание H2SO4 в экстракте; 4 – экстракция H2SO4 в отсутствие HF
Экстракция фтороводородной кислоты ДАМ в 1,2-дихлорэтан из ее смесей серной кислотой была изучена в работе [7]. Обращает на себя внимание увеличение экстракции серной кислоты ДАМ и то, что в условиях 2 моль/л H2SO4 отношение Н+:ДАМ приближается к 0,26 (табл. 1.4). Экстракция HF при этом уменьшается.
