
- •Углеводы
- •Введение
- •I. Моносахариды
- •I.1. Типы моносахаридов и их номенклатура
- •I.2. Стереохимия моносахаридов
- •I.3. Вывод конфигураций альдоз d-ряда
- •I.4. Доказательство конфигураций пентоз и гексоз d-ряда
- •I.5. Таутомерия моносахаридов
- •I.6. Мутаротация
- •1.7. Конформации моносахаридов
- •I.8. Химические свойства моносахаридов
- •Реакции нециклических форм
- •Б. Реакции циклических форм
- •I.9. Производные моносахаридов
- •II. Олигосахариды
- •II.2. Свойства дисахаридов
- •II.3. Производные дисахаридов
- •III. Полисахариды
- •III.1. Гомополисахариды
- •III.2. Гетерополисахариды
- •Контрольные вопросы
- •III.3. Смешанные углеводсодержащие полимеры
- •Список литературы
I.5. Таутомерия моносахаридов
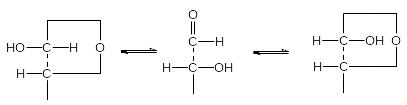
Альдозы и кетозы, как и обычные альдегиды и кетоны, способны к енолизации под действием агентов основного характера (разбавленных щелочей, гидроокисей щелочноземельных металлов, пиридина и хинолина; под действием крепких щелочей моносахариды разлагаются). Этот процесс называется кето-енольной таутомерией.
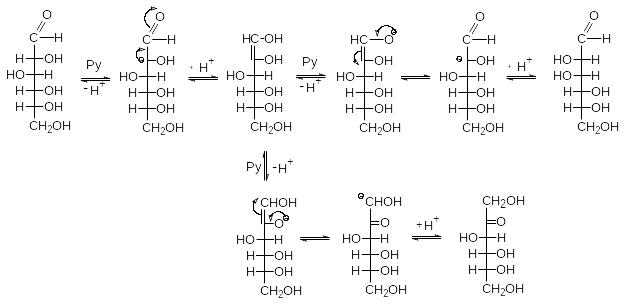
Глюкоза (64%) Манноза (2,5%)
Фруктоза (31%)
Таким образом, из глюкозы в присутствии основания образуются манноза и фруктоза. Такое взаимопревращение глюкозы, маннозы и фруктозы, являющихся эпимерами (соединениями, различающимися конфигурацией только при одном асимметрическом центре), называется эпимеризацией.
Енольные формы альдегидов и кетонов неустойчивы (правило Эльтекова-Эрленмейера). По этой причине образовавшийся ендиол легко претерпевает миграцию протона одной из гидроксильных групп и переходит в исходные карбонильные соединения. Когда мигрирует протон гидроксильной группы, связанной с первым углеродным атомом, образуются с равной степенью вероятности манноза и глюкоза, поскольку винильный фрагмент плоский и протон может атаковать его с любой стороны. При миграции протона гидроксильной группы, свя-занной со вторым атомом углерода, всегда образуется фруктоза и новых асимметрических атомов при этом не возникает. Обращает на себя внимание тот факт, что енолизация фруктозы происходит за счет отщепления протона от атома углерода первичноспиртовой, а не вторичноспиртовой группы. Возможно, это объясняется пространственными факторами (меньшей экранированностью первого из них).
Было установлено, что пентозы и гексозы в кристаллическом состоянии представляют собой внутренние циклические полуацетали, т.е. для них характерна кольчато-цепная или цикло-оксо-таутомерия. При этом одна из гидроксильных групп в молекуле внутримолекулярно взаимодействует с карбонильной группой, давая циклический полуацеталь.
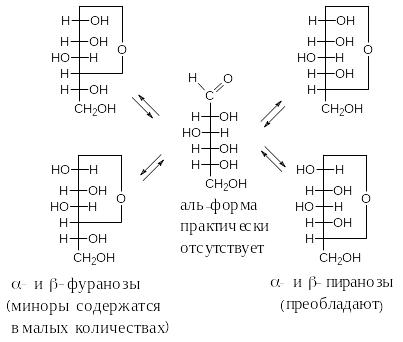
Справедливость таких предположений подтверждается тем, что циклические полуацетали устойчивы, когда кислородсодержащий цикл пяти- или шестичленный. Было показано, что в равновесных смесях, которые дают данные моносахариды, циклические формы преобладают. При этом пятичленное оксидное кольцо назвали фуранозным, а шестичленное – пиранозным в соответствии с названиями пяти- и шестичленных кислородсодержащих гетероциклов – фурана и пирана (соответственно):

П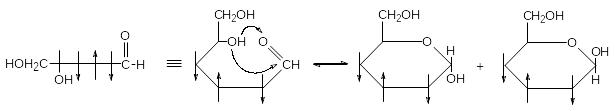 риведенные
выше циклические формулы моносахаридов
неудобны в обращении, часто не дают
возможности правильно судить о
действительном пространственном
расположении атомов в молекуле. Особенно
трудно представить, какое место в
пространстве относительно других атомов
занимает, например, атом кислорода. В
связи с этим было предложено изображать
молекулы пиранозных и фуранозных форм
моносахаридов с помощью так называемых
перспективных формул (Хеуорз), т.е. таким
образом, чтобы оксидное кольцо в них
располагалось перпендикулярно плоскости
рисунка.
риведенные
выше циклические формулы моносахаридов
неудобны в обращении, часто не дают
возможности правильно судить о
действительном пространственном
расположении атомов в молекуле. Особенно
трудно представить, какое место в
пространстве относительно других атомов
занимает, например, атом кислорода. В
связи с этим было предложено изображать
молекулы пиранозных и фуранозных форм
моносахаридов с помощью так называемых
перспективных формул (Хеуорз), т.е. таким
образом, чтобы оксидное кольцо в них
располагалось перпендикулярно плоскости
рисунка.
пиранозные формы глюкозы
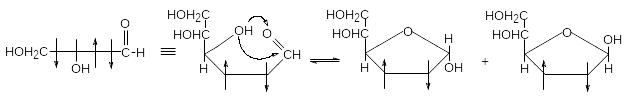
фуранозные формы глюкозы
Превращение альдегидной формы моносахаридов в циклическую сопровождается появлением нового асимметрического атома углерода. Поскольку в каждом случае при образовании циклического полуацеталя гидроксил может атаковать атом углерода карбонильной группы с обеих сторон, такая циклизация приводит к смеси стереоизомеров с различной конфигурацией у вновь образовавшегося асимметрического атома углерода.
Т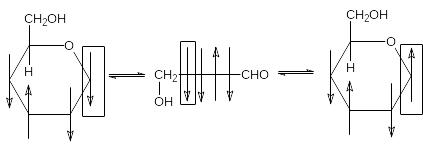 акие
диастереомеры стали называть аномерами
(от греческого «ано» – вверху).
Рассмотренные превращения, сопровождающие
обращение конфигурации у С1,
обратимы. В случае D-глюкозы,
например, они могут быть представлены
следующим образом:
акие
диастереомеры стали называть аномерами
(от греческого «ано» – вверху).
Рассмотренные превращения, сопровождающие
обращение конфигурации у С1,
обратимы. В случае D-глюкозы,
например, они могут быть представлены
следующим образом:
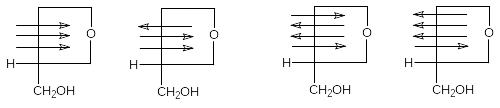
-аномер -аномер
Аномер моносахарида D-ряда, у которого гидроксил у вновь образовавшегося асимметрического атома углерода располагается под плоскостью цикла, называется –аномером.
Используя такой подход, нетрудно написать формулы – и –аномеров любых пентоз и гексоз:
- Рибоза - - Манноза -
С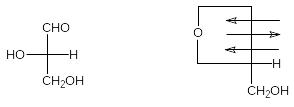 ледует
отметить, что в проекции Фишера -аномеры
моносахаридов L-ряда
будут содержать полуацетальный гидроксил
над плоскостью цикла. Например:
ледует
отметить, что в проекции Фишера -аномеры
моносахаридов L-ряда
будут содержать полуацетальный гидроксил
над плоскостью цикла. Например:
L-глицериновый -аномер
альдегид L-арабинозы
Контрольные вопросы
1. Напишите структурную формулу любой альдопентозы. Нарисуйте полуацеталь фуранозы в - и -формах.
2. Напишите проекционные формулы -D-глюкофуранозы, -D-фруктофуранозы, -D-маннофуранозы, -L-галактопиранозы.
3. Как можно доказать наличие циклической формы у D-фруктозы.
4.Написать уравнения реакций, с помощью которых можно превратить альдогексозу в альдопентозу и альдопентозу в альдогексозу.
5. Что происходит с D-галактозой в присутствии гидрооксида кальция.
6. Приведите для -D-глюкопиранозы строение ее аномера, энантиомера, эпимера по С2, эпимера по С4. Изобразите его пиранозную и фуранозную формы.
7. Изобразите схему перехода в водном растворе 2-дезокси--D-рибофуранозы в таутомер, обладающий восстановительными свойствами.
