
- •Курсовая работа
- •Реферат
- •Содержание
- •Введение
- •1 Основная часть
- •Биоповреждения материалов и изделий и их вид
- •1.1.1 Виды бактериальных биоповреждений и их характеристика
- •1.1.2 Факторы, влияющие на биоповреждения объектов
- •1.1.3 Механизмы бактериальных биоповреждений
- •Характеристика микроорганизмов-декструкторов
- •1.2.1 Хемолитотрофные микроорганизмы (тионовые, нитрифицирующие, железобактерии)
- •1.2.2 Гетеротрофные бактерии (протеолитические, липолитические, гликолитические)
- •1.2.3 Метаногенные бактерии и их характеристика
- •1.3 Методы обнаружения бактерий и идентификации микроорганизмов
- •1.3.1 Методы обнаружения бактерий и определения их численности
- •1.3.2 Методы-выделения микроорганизмов-деструкторов
- •1.3.3 Методы определения активности микроорганизмов и продуктов их метаболизма
- •1.4 Способы защиты материалов и изделий от биоповреждений м/о
- •1.4.1 Использование защитных покрытий
- •1.4.2 Полимерные материалы с антимикробными свойствами
- •1.5 Методы оценки биостойкости материалов и защитных покрытий
- •1.5.1 Почвенный метод
- •1.5.2 Метод агаровых сеток
- •1.5.3 Метод агаровых блоков
- •1.5.4 Методы оценки адаптации бактерий к антимикробным веществам
- •2 Экспериментальная часть
- •2.1 Материалы и оборудование
- •2.2 Микроорганизмы и питательные среды
- •2.2.1Питательные среды для культивирования грибов
- •2.2.2 Выделение чистых культур бактерий
- •2.3 Методы анализа
- •2.3.1 Определение общего количества бактерий методом культивирования
- •2.3.2 Построение калибровочных зависимостей микроорганизмов по спектру мутности
- •2.3.3 Анализ физиологической активности бактерий редуктазным методом
- •2.3.4 Метод определения эффективных концентраций биоцидов
- •2.3.5 Оценка защитного действия биоцидных веществ методом «агаровой сетки» и «агаровых блоков»
- •2.3.6 Оценка защитного действия биоцидных веществ микрокалориметричеким методом
- •2.4 Результаты исследований и их обсуждение
- •2.4.1 Оценки биостойкости материалов по гост 9.048
- •2.4.2 Анализ биостойкости материалов по методу «агаровой сетки» и агаровых блоков
- •2.4.3 Характеристика биостойкости материалов микрокалориметрическим методом
- •Заключение
- •Используемая литература
2.3 Методы анализа
2.3.1 Определение общего количества бактерий методом культивирования
Применение метода культивирования микроорганизмов может осуществляться для достижения следующих целей:
1) накопления клеток;
2) обогащения смешанной популяции представителями определенной группы;
3) получения чистой культуры;
4) получения целевого продукта;
5) перевода клеток в нужную фазу роста и т. д.
Культивирование микроорганизмов сопровождается увеличением их количества и массы.
Для реализации метода культивирования на практике осуществляют получение суточной культуры, представляющей собой суспензию клеток в жидкой питательной среде. В ней достигается максимальная концентрация микроорганизмов и популяция обычно находится в стационарной фазе роста.
Обязательным условием получения суточной культуры является подготовка контроля за соблюдением правил асептики. Для получения суточной культуры бактерий поступают следующим образом. В две стерильные пробирки вносят по 2 мл питательного агара. Затем в одну из них бактериологической петлей засевают изолированную колонию бактерий. Помещают посевы в термостат и инкубируют 16–18 часов [19].
Результаты, полученные при определении общего количества бактерий методом культивирования, представлены в таблице 2.
Таблица 2 – Результаты определения бактерий
а |
f |
v |
Ni, кл/мл |
Ncp, кл/мл |
СКО, кл/мл |
ε, % |
||||||||
75 |
60 |
0 |
1 |
75 |
60 |
6,8*101 |
7,5 |
11,1 |
||||||
62 |
50 |
1 |
1 |
6,2*102 |
5,0*102 |
5,6*102 |
60 |
10,7 |
||||||
43 |
38 |
2 |
1 |
4,3*103 |
3,8*103 |
4,1*103 |
250 |
6,2 |
||||||
2.3.2 Построение калибровочных зависимостей микроорганизмов по спектру мутности
На рисунке 5 представлена калибровочная зависимость бактерий.
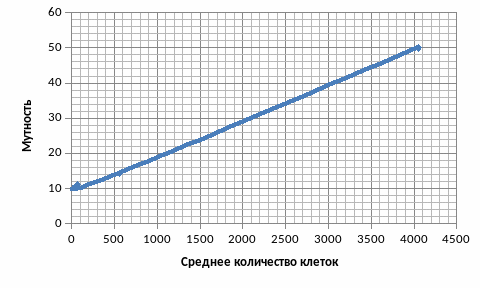
Рисунок 5 – Калибровочная зависимость бактерий по спектру мутности
2.3.3 Анализ физиологической активности бактерий редуктазным методом
Анализ физиологической активности бактерий можно осуществлять редуктазным методом.
Сущность данного метода заключается в установлении физиологической активности бактерий, продуцирующих фермент редуктазу, которая способна обесцвечивать некоторые краски, в частности метиленовую синь. Этой способностью обладают также лейкоциты, аскорбиновая кислота и некоторые другие вещества, содержащиеся в молоке. В основу метода положено определение времени, необходимого для обесцвечивания метиленовой сини. Для постановки редуктазной пробы в пробирку 20 мл молока добавляют 1 мл рабочего раствора метиленовой сини и плотно закрывают пробкой. После перемешивания пробирку помещают в водяную баню при температуре 37–40 °С, наблюдая за временем обесцвечивания метиленовой сини через 20 мин, 2 и 5,5 ч. Для приготовления рабочего раствора берут 5 мл насыщенного спиртового раствора метиленовой сини и добавляют 195 мл дистиллированной воды.
Молоко относят к I классу, если обесцвечивание метиленовой сини происходит через 5,5 ч. В молоке II класса обесцвечивание происходит за 2-5,5 ч. Молоко III класса обесцвечивается в период от 20 мин до 2 ч. Время наступления обесцвечивания содержимого пробирки указывает на приблизительное количество в исследуемом молоке микроорганизмов, продуцирующих фермент редуктазу.
Проведенные исследования позволили отнести испытуемое молоко к I классу.
Преимущество редуктазной пробы в сравнении с прямым бактериологическим методом состоит в быстроте получения результате (примерно через 5,5 ч). Однако не все микроорганизмы обладают редуцирующей активностью. В большей степени это свойство имеют молочнокислые стрептококки, кишечные палочки, маслянокислые и гнилостные бактерии, несколько меньше - сальмонеллы и стафилококки, а возбудители мастита стрептококковой этиологии лишены этой способности. Поэтому молоко может содержать большое количество стрептококков, вызывающих мастит, а по редуктазной пробе оно будет отнесено к первому классу. Кроме того, эта проба дает завышенные результаты летом и почти бесполезна зимой. Другими словами, молоко II и III класса после двухсуточного охлаждения при 4–5 °С по редуктазной пробе дает показатели I класса. Следовательно, редуктазная проба с метиленовой синью дает весьма неточное представление о степени бактериальной обсемененности молока и его санитарном качестве. Поэтому показатели редуктазной пробы необходимо учитывать в комплексе с другими результатами исследований.
