
- •Молекулалық-кинетикалық теорияның негiзгi ұғымдары
- •Э Бағыттаушы жүйе лектр тогы
- •Электр заряды
- •Ішкі энергия
- •Диффузия. Броун
- •Электрлік сыйымдылық
- •Температура және жылулық тепе-теңдік.
- •Қаныққан және қанықпаған бу. Қайнау кризистік температура. Сұйықтардың беттік керілуі.
- •Электр қозғаушы күші. Толық тізбек үшін Ом заңы. Тоқтардың түйіндері. Кирхгоф ережесі.
- •Газ тәрізді, сұйық және қатты денелердің құрылысы. Қатты денелер.
- •Магнит өрісі. Ампер. Ток элементі.
- •Электростатикалық өріс жұмысы. Потенциалдық энергия. Потенциал. Потенциалдар айырымы, өлшем бірлігі Зарядтың орынауыстыруы кезiнде электр өрiсiнiң жұмысы
- •Гравитациялық өрiспен ұқсастығы.
- •Бүкіләлемдік тартылы заңы. Гравитациялық өрістегі дененің потенциалдық энергиясы.
- •Кеңістік торлар. Деформация түрлер. Юнг модулі. Гук заңы.
- •Электр өрісі. Электр өрісінің негізгі қасиеттері. Кернеулігі. Өрістің суперпозициялық принципі.
- •Элементар электр зарядын тәжірибе жүзінде анықтау. Милликен-Иоффе тәж.
- •Тоқ күшімен кернеуді өлшеу. Реостат. Потенциометр. Шунт және қосымша кедергі.
- •Электр тогы. Токтың әсері. Ток күші. Металл өткізгіштегі электрондардың реттелген қозғалысының жылдамдығы. Электр тогының бар болу шарттары.
- •Капилярлық құбылыстар.
- •Газ заңдары
- •Ауаның салыстырмалы ылғалдылығы. Психометр. Гигромет. Ылғалдылықтың маңызы.
- •Тоқтардың өзара әсері. Магнит өрісі. Магнит индукциясының векторы және сызықтары. Құйынды өріс.
- •Жылу қозғалтқыштары. Пәк
- •Электростатикалық өрістегі диэлектриктер.
- •Магнит индукция векторының модулі. Ампер күші, заңы. Элекрт өлшеуіш приборлар. Ампер заңын қолдану.
- •Жартылай өткізгіштердегі электр тогы.
- •Лоренц күші
- •Жылу мөлшері. Меншікті жылусыйымдылық. Меншікті булану және балқу жылуы.
- •Заттардың магниттік қасиеттері. Ампер гипотезасы. Магнит өтімділік. Ферромагнетиктер
- •Траекторияның қисықтық радиусы
- •Вольт-амперлік сипаттама. Кедергі. Электр тізбегі. Өткізгіштерді тібектей және параллель қосу. Шартты белгілер
- •Ілгермелі қозғалыс динамикасы. Импульс түрінде жазылған Ньютонның іі заңы.
- •2. Жартылай өткізгіштегі электр тогы
- •Элекролиттегі электр тогы. Фарадей
- •2. Термодинамиканың і заңын әртүрлі процестерге қолдану.
- •Жартылай өткізгіштердегі элект тогы. Диод. Транзистор
Температура және жылулық тепе-теңдік.
Температура: Жылулық тепе-теңдік кезінде барлық денелердің температуралары бірдей, сондықтан оны жылулық тепе-теңдік күйінің сипаттамасы деп есептеуге болады.
Температура деп жылулық тепе-теңдіктегі изоляцияланған жүйенің малекулаларының жылулық қозғалысының интенсивтілігін сипаттайтын және малекулалардың ілгерімелі қозғалысының орташа кинетикалық энелгиясына тура пропорционал скаляр шаманы айтамыз.
1. Фаренгейт шкаласы.1724 ж. Ұлыбританияда және Голландияда жұмыс істеген неміс физигі Фарангейт ұсынған. Реперлік нүктелер:
0 F -1709 ж. ерекше суық қыстың температурасы 32 гр F – мұздың еру температурасы 98 гр. F . бұл шкала бойынша судың қайнау температурасы 212 гр F . Фаренгейт шкаласын АҚШ-та пайдалана- ды.
2. Реомюр шкаласы. 1730 ж.француз жаратылыстанушысы Реомюр жасаған. Реперлік нүктелері : 0 гр. Р –мұздың еру температурасы:100 гр С-судың қайнау температурасы.
3. Цельсий шкаласы. 1742ж. швед астрономы және физигі Цельсий жасаған. Реперлік нүктелері: 0 гр С –мұздың еру температурасы; 100 гр С- судың қайнау температурасы.
Абсолют температуралар шкаласы. Тұңғыш рет температуралық шкаланы физикалық құбылыстың негізінде жасаған ғалым, ағыл- шын физигі 1848 жылы Томсон Уильям ғылыми жетістіктері үшін лорд Кельвин атанды. Цельсий шкаласы бойынша -237 гр С температураға 0 К сәйкеc келеді. Бұл мынадай байланыста болады. Т = t + 237
Газ
малекуласының кинетикалық энергиясы
мен температурасы арасындағы байланысы:
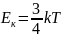 k-Больцман тұрақтысы(1,3807*10-23Дж/К)
k-Больцман тұрақтысы(1,3807*10-23Дж/К)
№5 БИЛЕТ
Қаныққан және қанықпаған бу. Қайнау кризистік температура. Сұйықтардың беттік керілуі.
Заттың сұйық күйден газ күйiне өту процесiн буға айналу деп атайды. Неғұрлым сұйықтың температурасы жоғары болса, соғұрлым сұйық тезiрек буға айналады.
Буға айналудың екi түрi бар: булану және қайнау. Кез келген температурада және тек сұйық бетiнен шығып бу күйiне айналуды – булану деп атайды. Бу – буланудың әсерiнен пайда болатын газ. Булану барысында сұйық салқындайды.
Буланған молекулалардың белгiлi бiр бөлiгi хаостық (ретсiз) қозғалыс жасай отырып қайтадан сұйық бетiне түсуi және оның молекулаларына айналуы керек. Соныменен, булану процессiмен қатар бiрмезгiлде конденсация деп аталатын керi процесс те жүредi.
Конденсация – бұл заттың салқындау немесе сығылуының салдарынан газ тектес күйден сұйық күйге айналу процессi. Сұйық бетiндегi будың қысымы неғұрлым жоғары болса, сол температурада конденсацияға ұшырайтын молекулалар саны да соғұрлым көп болады.
Бетi ашық ыдыстағы сұйықтың булану процесi конденсация процесiнен басым болып келедi. Ал бетi жабық ыдыста сұйық пен будың арасында, булану процесi мен конденсация процесстерi бiрiн-бiрi толықтыратындай, динамикалық тепе-теңдiк орнайды. Өз сұйығымен динамикалық тепе-теңдiкте болатын буды қаныққан бу деп атайды.
Температура тұрақты болған жағдайда қаныққан будың қысымы оның алатын көлемiне байланысты болмайды.
Егер сұйықтың булануы конденсациядан басым болса немесе сұйық толық буланып кетсе, онда оның устiндегi буды қанықпаған бу деп атайды. Буларға, тек бу қанықпай тұрған жағдайда ғана, идеалды газдар үшiн орныққан заңдарды қолдануға болады.
Көлем тұрақты болған жағдайда қаныққан будың қысымы температураға өте қатты тәуелдi болады, сондықтан Шарль заңын қаныққан буға қолдануға болмайды. Температура жоғарлаған сайын, будың конденсациялануына қарағанда, сұйық тезiрек буланады. Қысымның күрт өсуiне негiзiнен будың тығыздығының ұлғаюы тiкелей әсерiн тигiзедi.
Қайнау – бұл тек қана ашық беттегi сұйықтың интенсивтi булануы емес, сонымен қатар бу көпiршiктерiн түзетiн қуыс көлемiндегi сұйықтың да интенсивтi булануы.
Сұйық пен қаныққан бу арасындағы физикалық қасиеттерінің айырмашылыға жойылатын температура – кризистік.
Сұйық бетiн түзейтiн молекулалардың, сұйық көлемi iшiндегi басқа молекулаларға қарағанда потенциалдық энергиясының артық. Сұйықтың ашық бетiндегi молекулалардың артық потенциалдық энергиясы беттiк энергия деп аталады. Бiрлiк ауданның беттiк энергиясы σ - меншiктi беттiк энергия деп аталады: σ = W/S , мұндағы W – S ауданға жинақталған беттiк энергия. СИ өлшем бiрлiк жүйесiнде меншiктi беттiк энергия Дж/м2 – пен өлшенедi.
Беттiк қабаттың бөлшектерi, сұйық бетiне жанама жазықтықта жатқан және сұйық бетiнiң ауданын мейлiнше кiшiрейтуге бағытталған, (негiзделген) күштiң әсерiне ұшырайды. Бұл күштер – беттiк керiлу күштерi F деп аталады.
Оларды сандық жағынан бағалау үшiн беттiк керiлу коэффициентi деген ұғым енгiзiледi. Бұл коэффициент сұйықтың бос бетiнiң ауданын бiрлiкке изотермалық түрде арттыру үшiн жасалатын жұмыс ретiнде анықталады.
Жоғарыдағы айтылғанарды ескерсек: ΔW = -A =σΔS . Бұдан
σ = - A/ΔS (A<0) екендiгi шығады.
Егер сұйықтың ашық бетi тұйық сызықпен шектелген болса, онда бұл сызық - жұғылу периметрi деп аталады. Ондай беттер үшiн σ = F / L, СИ өлшем бiрлiк жүйесiнде σ шамасының өлшем бiрлiгi Н/м.
Беттiк керiлу коэффициентi меншiктi беттiк энергияның мағынасын бередi: 1 Н/м = 1 Дж/м2 . Беттiк күштi серпiмдiлiк күшiмен шатастыруға болмайды.
