
- •3.Опыты по рассеиванию -частиц: схема опыта, сущность и особенности эксперимента, значение.
- •8. Обобщённая формула Бальмера: формула, физический смысл.
- •11) Первый постулат Бо8/ра (постулат о стационарных состояниях): формулировка, диаграмма энергетических уровней.
- •12.Второй постулат Бора (условие частот): формулировка, формула, диаграмма энергетических уровней.
- •14. Доказательство дискретности значений энергии атома: опыт Франка и Герца.
- •15. Значение и недостатки теории Бора.
- •16. Предпосылки создания гипотезы Луи де Бройля.
- •17. Физическая сущность и формулировка гипотезы де Бройля.
- •18. Записать и пояснить физический смысл волновой функции.
- •19. Вывести выражение, определяющее длину волны де Бройля – д.
- •20. Как де Бройль обосновал правило квантования момента импульса в третьем постулате Бора?
- •21. Найдите зависимость длины волны электрона от ускоряющего напряжения электрического поля, в котором он находится.
- •22. Физические основы явления дифракции электронов в опытах к. Дэвиссона и л.Джермера (схема установки, выводы).
- •23. Анализ графика зависимости количества отражающихся от монокристалла электронов от их скорости движения.
- •24. Сравнительный анализ электронограммы в опытах по дифракции электронов с дифракционной картиной рентгеновских лучей.
- •25. Запись и анализ формулы для определения длины волны в опытах к. Дэвиссона и л.Джермера.
- •26. Применение дифракции частиц в медицине, фармации, технических приборах.
- •27.Устройство и принцип действия магнитной линзы
- •28.Устройство и принцип действия растрового электронного микроскопа.
- •29. Благодаря чему разрешающая способность электронного микроскопа выше, чем у оптического?
- •30. Как проявляются волновые свойства атомов и ионов?
- •31. Статистическая интерпретация волн де Бройля.
- •36.С оотношения неопределённостей
- •37. Физический смысл соотношений неопределённостей.
- •38. Какой смысл имеют величины, входящие в формулу е t h
- •40. Какое состояние называют стационарным, квазистационарным?
- •41. Как можно измерить среднее время жизни квазистационарного состояния атома?
- •42. Получите основное уравнение квантовой механики (уравнение Шрёдингера) для стационарных состояний?
- •47. Объясните, почему энергетический спектр для прямоугольной потенциальной ямы дискретен, я число уровней конечно.
- •49. Сравните поведение классической и квантово-механической частиц в потенциальной яме.
- •53. Перечислите основные положения, используемые при вычислении спектра гармонического осциллятора методом Шрёдингера
1.Квантовая физика – наука, изучающая окружающий мир на уровне микроявлений. В них на 1 месте выступают микрообъекты: молекулы, атомы, элементарные частицы.
В основе построения теорий выделяют 2 пути:
идея дискретности или непрерывности физических процессов. Основоположник Планк, который в 1900 г изучал излучение и поглощение энергии нагретыми телами.
Идея корпускулярно-волнового дуализма: при излучении и поглощении объект ведет себя как частица, а при распространении света как волна.
2. Модель атома Томсона:
Первая
попытка создания модели атома на основе
накопленных экспериментальных данных
принадлежит Дж. Дж.Томсону
(1902 г.).
Томсон
считал, что атом представляет собой
электронейтральную систему шарообразной
формы радиусом примерно равным ![]() м.
Положительный заряд атома равномерно
распределен по всему объему шара, а
отрицательно заряженные электроны
находятся внутри него. (кекс с изюмом)
м.
Положительный заряд атома равномерно
распределен по всему объему шара, а
отрицательно заряженные электроны
находятся внутри него. (кекс с изюмом)
Для объяснения линейчатых спектров испускания атомов Томсон пытался определить расположение электронов в атоме и рассчитать частоты их колебаний около положений равновесия. Однако эти попытки не увенчались успехом. Через несколько лет в опытах великого английского физикаЭ. Резерфорда было доказано, что модель Томсона неверна.
3.Опыты по рассеиванию -частиц: схема опыта, сущность и особенности эксперимента, значение.
Опыты Резерфорда, в котором использовались альфа-частицы, возникающие при распаде радия и некоторых других элементов, позволили более точно определить строение атома. Схема опыта Резерфорда, имеет следующий вид. Радиоактивный препарат помещается внутрь свинцового цилиндра. Сквозь узкий канал создается поток альфа частиц, которые бомбардируют золотую фольгу. Скорее это была не просто фольга, а сверхтонкая фольга из сусального золота. После рассеяния альфа-частицы попадали на прозрачный экран, покрытый сульфидом цинка. Столкновение каждой частицы с экраном сопровождалось вспышкой света, которую можно было наблюдать в микроскоп. Эта система могла свободно вращаться относительно точки на золотой фольге, в которую попадал поток альфа частиц. Естественно, чтобы не было влияния молекул воздуха, весь прибор был помещен в вакуум. Электроны, вследствие своей малой массы, не могут заметно изменить траекторию альфа-частицы. Рассеяние альфа-частиц может вызвать только положительно заряженная часть атома. Таким образом, по рассеянию альфа частиц можно определить характер распределения массы и положительных зарядов внутри атома.
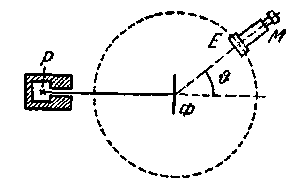
4. Планетарная модель атома Резерфорда: предпосылки создания, сущность, значение, противоречия.
Резерфорд сделал вывод: в случае резкого отклонения альфа-частиц они наталкиваются на тяжелое ядро, в котором сосредоточена почти вся масса атомов, при этом объем ядра маленький, т.к. отталкивающихся частиц очень мало и заряд у этого ядра «+». Отталкиваются одноименные заряды. Таким образом, Резерфорд предложил планетарную модель строения атома: В центре атома находится очень маленькое ядро во много раз меньше размеров самого атома. Ядро - это практически вся масса атома и заряжена «+». Вокруг ядра движутся электроны, число которых равно заряду ядра, размеры атома определяются траекторией движения электронов.
Выводы и противоречия:
Было
известно, что любая заряжена частица
при движении высвобождает энергию,
уменьшает собственную энергию движения
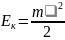
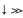 излучение
излучение
1.Если это так, то электрон с течением времени должен упасть на ядро, чего не происходит, говорят об устойчивости атома.
2. По Резерфорду спектр излучения атома должен быть сплошной.
3. Уравнение механики и электродинамики установлены в результате излучения движущихся заряженных частиц и справедливы только для макротел, но в поведении микрочастиц присутствуют другие их свойства, которые не нашли отражения в механике Ньютона и теории Максвелла.
5. Условие возникновения излучения атома, понятие о спектре и спектральной серии.
В определении особенных свойств заряженных микрочастиц сыграли закономерности, обнаруженные в спектре излучения водорода. В нормальном состоянии водород не излучает, но излучение можно возбудить в нем, если сообщать дополнительную энергию Чем больше энергии сообщается атому тел, тем более выражены в нем энергетические процессы, как излучение, так и поглощение. Наблюдения в сфере излучения водорода наблюдал Бальмер => спектр можно разбить на определенные группы линий, которые называются спектральными сериями. Совокупность спектральных линий, поглощение которых в спектре подчиняется определенным закономерностям называется спектральной серией. Линейчатый спектр атома представляет собой совокупность большого числа линий, разбросанных по всему спектру без всякого видимого порядка.
6. Спектральная серия Бальмера в спектре атома водорода: формула, физический смысл, значение.
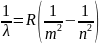 где λ —
длина волны, R ≈
1,097·107 м−1 — постоянная
Ридберга,
где λ —
длина волны, R ≈
1,097·107 м−1 — постоянная
Ридберга,
n = 3,4,5..кол-во спектральных линий в серии
При больших квантовых значениях спектр переходит в сплошной.
Значение n будет меняться при переходе одной спектральной серии к другой. У водорода 6 спектральных серий:
1.Серия Лаймана
2.Бальмера
3.Пашена
4.Пфунда
5.Хэмфри
7.Состав и закономерности в спектре излучения атомарного водорода: перечислить и записать формулы для основных серий излучения.
Лайман
m=1
, n=2,3,4…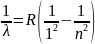
Бальмер
m=2,
n=3,4,5…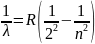
!остальные аналогично
