
- •V. Фотохимические реакции
- •5.1. Основные понятия и сущность фотохимии
- •5.2. Основные законы фотохимии
- •Первичные фотохимические реакции.
- •5.3. Кинетика первичного фотохимического процесса
- •VI. Цепные реакции
- •6.1. Основные понятия и сущность цепного процесса
- •К цепным реакциям относятся:
- •6.2. Механизм цепных химических реакций
- •6.2.1. Зарождение цепей
- •6.2.2. Продолжение цепей
- •Обрыв цепей
- •6.3. Кинетика неразветвленных цепных реакций
- •Принцип стационарности
- •Скорость цепной реакции
- •6.4. Горение и взрыв
VI. Цепные реакции
6.1. Основные понятия и сущность цепного процесса
Свободными радикалами называются частицы, которые содержат хотя бы один неспаренный электрон и поэтому обладающие ненасыщенными валентностями.
Первоначально дадим определение цепной реакции на основе понятия “элементарные реакции”.
Химические процессы, протекающие через регулярно повторяющиеся элементарные реакции с участием радикалов, атомов, ионов или возбужденных молекул, называются цепными реакциями.
Другое определение дается на основе понятия “активная частица”.
Цепными реакциями называются химические реакции, в которых появление активной частицы вызывает большое число превращений неактивных молекул вследствие регенерации активной частицы в каждом элементарном акте реакции.
Третье определение дается на основе понятия “продукты реакции”.
Цепная реакция – это самоподдерживающаяся химическая реакция, при которой первоначально образующиеся продукты принимают участие в образовании новых продуктов.
(Все определения даны для химических процессов)
Таким образом, в ходе цепной реакции, активирование одной частицы приводит к образованию продуктов реакции и возникновению новых активных частиц.
Активный центр (активная частица). Активными частицами могут служить свободные атомы, ионы, радикалы и возбужденные молекулы. Наиболее часто – это свободный радикал с высокой реакционной способностью.
Цепные реакции протекают обычно (но не обязательно) с большой скоростью и нередко имеют характер взрыва.
К цепным реакциям относятся:
Процессы, которые происходят в фотографических материалах.
Термический и инициированный крекинг или пиролиз всех классов органических соединений.
Реакции галогенирования предельных углеводородов.
Многие реакции окисления неорганических и органических соединений в газовой и жидкой фазах.
Реакции полимеризации и поликонденсации.
Реакции фотохимического распада и синтеза многих неорганических и органических веществ.
Процессы старения полимеров и их фотоокислительной деструкции.
Многие гетерогенно-каталитические реакции на поверхности идут как цепные с участием не только радикалов, но и ионов.
Процессы горения.
К цепным процессам можно отнести и некоторые явления, не связанные с химией: термоядерный синтез, развитие опухолей, размножение вирусов и другие явления химии, физики, биологии,
медицины и пр.
Во всякой цепной реакции можно выделить три стадии:
Зарождение (инициирования) цепи.
Развитие цепи.
Обрыв цепи.
Рассмотрим цепные реакции на примере наиболее распространенного случая подобных процессов – свободнорадикальных реакций.
Зарождение цепи начинается с возникновения частиц со “свободными валентностями” – радикалов, атомов, ионов.
Н апример: CBr4 CBr3· + Br· .
Этот процесс может происходить в результате термического распада молекул на атомы и радикалы, при столкновении молекул со стенками сосуда, поглощении фотона или в результате бимолекулярного акта взаимодействия.
Стадия развития цепи. На этой стадии промежуточные продукты реагируют с исходными реагентами, образуя новые интермедиаты и конечные продукты.
При рассмотрении данной стадии цепной реакции требуется ввести еще одно понятие – длина цепи.
Стадия развития цепных реакций повторяется много раз.
Длиной цепи называется число молекул данного исходного вещества, которые прореагировали в результате одного элементарного акта зарождения цепи.
Длина цепи зависит от соотношения между числом активных молекул, которые образуются в единицу времени, и расходуемых на получение продуктов реакции или дезактивацию.
Длина цепи указывает на число молекул продукта реакции, приходящихся на одну первоначально активированную частицу. Она может составлять 104-107.
З вено цепи (рассмотрим на примере реакции Cl2 + H2 hn 2НС1)
 Cl·
+ H2
HCl + H·
Cl·
+ H2
HCl + H·
H· + Cl2 HCl + Cl·
Стадия обрыва цепи. На этой стадии происходит окончательное расходование промежуточных продуктов или их разрушение.
Вследствие подобного действия реакция прекращается из-за исчезновения или дезактивации активных частиц. Реакция может оборваться самостоятельно (рекомбинация свободных радикалов, или под действием ингибиторов.
Ингибиторы - это вещества, которые уменьшают скорость химических реакций (в случае каталитических реакций – ингибиторы сами не изменяются в ходе процесса).
Катализаторы - это вещества, которые изменяют скорость реакции и не входят в состав конечных продуктов реакции.
Рассмотрим цепную реакцию на примере взаимодействия водорода с хлором в газовой фазе. На этом примере цепные реакции и были обнаружены в 1913 году Боденштейном. Процесс проводился фотокаталитически.
З арождение цепи { Cl2 hn Cl· + Cl·
 Развитие
цепи
Cl·
+ H2
HCl + H·
Развитие
цепи
Cl·
+ H2
HCl + H·
 H·
+ Cl2
HCl + Cl·
H·
+ Cl2
HCl + Cl·
О брыв цепи H· + H· H2 + Q
Cl· + Cl· Cl2 + Q
H· + Cl· HCl + Q
Q – энергия, которая выделяется в ходе реакции.
Энергия разрыва связей DEH2 = 436 кдж/моль (что соответствует излучению с длиной волны l = 276 нм) и DECl2 = 242,6 кдж/моль (что соответствует излучению с длиной волны l = 493 нм), поэтому при облучении видимым светом происходит гомолитическая диссоциация молекул Cl2 и процесс зарождения цепи происходит именно как указано выше. Кроме того, молекулы водорода не имеют поглощения даже в ультрафиолетовой области спектра, поэтому согласно первому закону фотохимии не реагируют со световым излучением вообще.
Известны две разновидности цепных реакций: с неразветвленными и разветвленными цепями. Первые возникают в том случае, если одна активная частица при своем взаимодействии вызывает образование только одной новой активной частицы. В данном случае число радикалов в системе остается постоянным. Например:
А В С А В С А В С А
А - это радикал, который начинает и заканчивает звено.
В и С - различные промежуточные радикалы.
Конкретный пример неразветвленной цепи – реакция образования фосгена:
С12
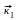 2С1·
–
процесс зарождения цепи;
2С1·
–
процесс зарождения цепи;
С О
+ С1·
О
+ С1·
 ·СОС1
·СОС1
·СОС1
+ С12
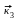 СОС12
+
С1·
Развитие цепи
СОС12
+
С1·
Развитие цепи
СО + С1· ·СОС1
· СОС1
+ С1·
СОС1
+ С1·
 СОС12
СОС12
С1·
+
С1·
![]() С12
обрыв цепи
С12
обрыв цепи
Скорость образования фосгена определяется эмпирическим уравнением:
-
d[COCl2]
= k[CO][Cl2]3/2
(6.1)
dt
Если в результате элементарного акта регенерируются две или более активных частиц, то осуществляется реакция с разветвленными цепями.
Примером может служить реакция кислорода с водородом.
Н 2 + О2 2ОН·
О Н· + Н2 Н2О + Н·
Н · + О2 ОН· + О·
О · + Н2 ОН· + Н·
Можно заметить, что в двух последних элементарных стадиях из одного радикала получается два.
Дадим определение.
Цепи, в которых число образующихся радикалов превышает число радикалов исчезнувших, носят название разветвленных.
 о
о
о о о о
о о о
о
Если разветвление происходит не при каждом элементарном акте реакции, то имеет место реакция с редкоразветвленной цепью.
Примером такой реакции может служить реакция окисления водорода при высоком давлении и температуре около 500 оС.
Н · + О2 НО2·
Н О2· + Н2 Н2О2 + Н·
Н · + О2 ОН· + О·
О Н· + Н2 Н2О + Н·
О · + Н2 ОН· + Н·
Иногда радикалы могут образовываться в результате распада малоустойчивых молекул промежуточного продукта реакции.
Такие реакции называются реакциями с вырожденным разветвлением.
Примером такой реакции является:
· СН3 + О2 СН3СОО·
С Н3ОО· + СН4 СН3ООН + ·СН3
С Н3ООН СН3О· + ·ОН (разветвление)
С Н3О· + СН4 СН3ОН + ·СН3
· ОН + СН4 ·СН3 + Н2О
Однако, образующийся пероксид может распадаться и другим путем.
С Н3ООН СН2О + Н2О
