
2.2. Молекулярная физика и термодинамика
Пример 2.1. (С2). В водонепроницаемый мешок, лежащий на дне моря на глубине 73,1 м, закачивается сверху воздух. Вода вытесняется из мешка через нижнее отверстие, и когда объем воздуха в мешке достигает 28,0 м, мешок всплывает вместе с прикрепленным к нему грузом. Масса оболочки мешка 2710 кг. Определите массу груза. Температура воды равна 7°С, атмосферное давление на уровне моря равно 10 Па. Объемом груза и стенок мешка пренебречь.
В основе решения этой задачи условие, при котором мешок с грузом начнет всплывать: ρVg = Mg + mrg + mвg, где М и mr — масса оболочки мешка и масса груза, V и mв — объем и масса воздуха в мешке, ρ — плотность воды. Следовательно, mr = ρV - М - mв.
Так
как мешок заполнен воздухом, то к его
состоянию применимо уравнение
Менделеева-Клапейрона: pV
=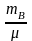 RT,
где давление воздуха на заданной глубине
h
можно выразить формулой р = р0+
ρgh,
где р0
— атмосферное давление.
RT,
где давление воздуха на заданной глубине
h
можно выразить формулой р = р0+
ρgh,
где р0
— атмосферное давление.
П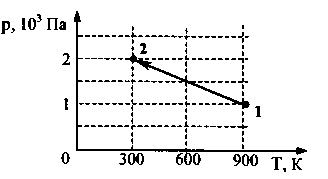 ример
2.2. (С2).
Bo
время опыта объем сосуда с воздухом
увеличился в 1,5 раза, и воздух перешел
из состояния 1 в состояние 2 (см. рисунок).
Кран у сосуда был закрыт неплотно, и
сквозь него мог просачиваться
воздух. Рассчитайте отношение
ример
2.2. (С2).
Bo
время опыта объем сосуда с воздухом
увеличился в 1,5 раза, и воздух перешел
из состояния 1 в состояние 2 (см. рисунок).
Кран у сосуда был закрыт неплотно, и
сквозь него мог просачиваться
воздух. Рассчитайте отношение
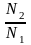 числа молекул газа в сосуде в конце и
в начале опыта. Воздух считать идеальным
газом.
числа молекул газа в сосуде в конце и
в начале опыта. Воздух считать идеальным
газом.
Основу
решения задач этого типа составило
уравнение состояния идеального газа в
виде р = nkT,
где n
= -
концентрации молекул газа. Отсюда легко
получить ответ в общем виде и числовой
ответ.
-
концентрации молекул газа. Отсюда легко
получить ответ в общем виде и числовой
ответ.
.
Пример 2.3. С(2). Сосуд разделен пористой перегородкой на две равные части. В начальный момент в одной части сосуда находится 2 моль гелия, а в другой - такое же количество аргона. Атомы гелия могут диффундировать (проникать) через перегородку, а для атомов аргона перегородка непроницаема. Температура гелия равна температуре аргона Т = 300 К. Определите отношение давлений газов на перегородку с разных сторон после установления термодинамического равновесия.
В решении такого рода задач необходимо было рассмотреть состояние системы после установления термодинамического равновесия: в каждой части сосуда окажется по 1 молю гелия. В результате в сосуде с аргоном окажется 3 моля смеси, а с другой стороны перегородки останется 1 моль гелия. Запись уравнения Клапейрона-Менделеева для каждой части сосуда позволит определить давление гелия и смеси: PHeV=RT и PHe+ArV = 3RT, где 2V – объем сосуда. Решение этих уравнений и приведет к ответу на заданный в задаче вопрос.
Пример 2.4. С(2). Цилиндрический сосуд, расположенный горизонтально, разделен тонким поршнем на две равные части. В одной части сосуда находится 1 кг гелия, а в другой - 1 кг аргона. В начальном состоянии поршень удерживается внешними силами. Поршень отпустили, и через некоторое время система пришла в состояние равновесия с окружающей средой, температура которой Т = 300 К. Какую часть цилиндра занимает гелий после установления равновесия? Трением поршня о стенки сосуда пренебречь.
Задача предполагает рассмотрение системы после установления механического и теплового равновесия: давление гелия и аргона на поршень должно быть одинаковым, и температура газов также одинакова рНe= рAr, = р, ТНе = ТAr = Т.
Применение
уравнения Клапейрона-Менделеева pVHe
=
νHeRT,
pVAr
=
νArRT,
где νAr=mAr/MAr,
νAr,
- число молей аргона, a
νHe=mHe/MHe
- число молей гелия, позволяет получить
отношение объемов (учитывая равенство
масс газов mНe
= mAг
= m):
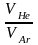 =
=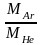 .
Но объем сосуда после установления
равновесия не изменился VHe
+ VAr=V,
поэтому легко найти искомое отношение
.
Но объем сосуда после установления
равновесия не изменился VHe
+ VAr=V,
поэтому легко найти искомое отношение
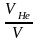 =
=
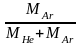 .
.
Решение следующего цикла задач было основано на понимании школьниками двух тем, вызывающих затруднения уже на уровне обязательного минимума содержания образования – «Первый закон термодинамики» и «Закон сохранения импульса» для случая неупругого соударения, рассмотренных нами выше. Результатом отсутствия понимания смысла этих законов на базовом уровне явилось причиной того, что ни один из участников экзамена не справился с такого рода задачами (пример 2.5).
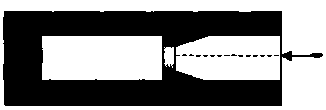 Пример
2.5. С(6.)
В
вакууме закреплен горизонтальный
цилиндр. В цилиндре находится 1 л
гелия, запертого поршнем, при давлении
100 кПа и температуре 300 К. Поршень
массой 90 г удерживается упорами и может
скользить влево вдоль стенок цилиндра
без трения. В поршень попадает пуля
массы 10 г, летящая горизонтально, и
застревает в нем. Температура гелия в
момент остановки поршня в крайнем левом
положении возрастает на 90 К. Какова
скорость пули? Считать, что за время
движения поршня газ не успевает обменяться
теплотой с цилиндром и поршнем.
Пример
2.5. С(6.)
В
вакууме закреплен горизонтальный
цилиндр. В цилиндре находится 1 л
гелия, запертого поршнем, при давлении
100 кПа и температуре 300 К. Поршень
массой 90 г удерживается упорами и может
скользить влево вдоль стенок цилиндра
без трения. В поршень попадает пуля
массы 10 г, летящая горизонтально, и
застревает в нем. Температура гелия в
момент остановки поршня в крайнем левом
положении возрастает на 90 К. Какова
скорость пули? Считать, что за время
движения поршня газ не успевает обменяться
теплотой с цилиндром и поршнем.
Решение
задачи основано на законе сохранения
импульса при неупругом соударении: mv0
= (m
+ M)vn.
Отсюда: vn=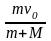 ,
где m
и М - соответственно масса пули и масса
поршня, v0
- скорость пули, vn
- скорость поршня после попадания пули.
,
где m
и М - соответственно масса пули и масса
поршня, v0
- скорость пули, vn
- скорость поршня после попадания пули.
Формула
для расчета внутренней энергии
одноатомного идеального газа U
=
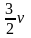 RT,
и учет того, что механическая энергия
поршня с пулей превращается во внутреннюю
энергию гелия, дает возможность рассчитать
ΔU:
ΔU
=
RΔT
=
RT,
и учет того, что механическая энергия
поршня с пулей превращается во внутреннюю
энергию гелия, дает возможность рассчитать
ΔU:
ΔU
=
RΔT
=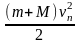 .
Из уравнения Менделеева – Клапейрона
следует, что νR
=
.
Из уравнения Менделеева – Клапейрона
следует, что νR
=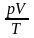 .
Решение системы уравнении дает: v0
=
.
Решение системы уравнении дает: v0
=
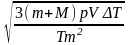 .
.
