
- •Лекция № 1. Введение. Общие сведения об условиях работы деталей стз.
- •Морское судно как объект изучения дисциплины
- •Эксплуатационные факторы, действующие на детали стс при их работе
- •Тип двигателя Рис. 1.7. Количественные соотношения и природа отказов для различных типов судовых дизелей
- •Время работы стс, тыс.Ч
- •(Формулы 1.1 и 1.2)
- •Лекция № 2. Тема: Идеальное и реальное строение материалов.
- •Лекция № 3. Тема: Механические свойства металлов и методы их определения.
- •Лекция №4. Деформация и механизм разрушения судовых деталей.
- •Особенности деформации поликристаллических тел.
- •Деформации и разрушение корпуса судна и деталей стс
- •Влияние температуры на строение и свойства материалов
- •Лекция № 5 Основы легирования материалов. Диаграмма состояния «железо углерод».
- •Лекция № 6 Тема: Основы термической обработки материалов.
- •Лекция №7 Тема: основные металлические конструкционные материалы в судостроении и судоремонте
- •Железоуглеродистые сплавы
- •Лекция № 8.
- •Лекция № 9. Тема: общая характеристика технологических процессов и операций.
- •Лекция №10 Тема: Физические основы сварки материалов.
- •Лекция № 11 Тема: Физическая сущность пайки и склеивания материалов.
- •Лекция № 12 Тема: Основы обработки материалов резанием.
- •Физические процессы при обработке резанием
- •Деформационные процессы в зоне резания
- •Тепловые явления при обработке резанием.
- •Изнашивание режущего инструмента
- •Станочная обработка резанием в условиях эксплуатации судна.
- •Лекция № 13 Тема: Обработка деталей в условиях эксплуатации судна. Восстановление деталей.
Лекция № 5 Основы легирования материалов. Диаграмма состояния «железо углерод».
Основные понятия теории сплавов
Одним из путей повышения конструкционной прочности является легирование - введение в расплавленный материал дополнительных элементов с целью изменения его свойств в заданном направлении. Результатом легирования является сплав.
В состав сплава входят компоненты и примеси (рис. 2.24). Компоненты - это вещества, которые введены в состав сплава специально, с целью получения необходимых свойств. Примеси попадают в сплав в ходе его получения случайно, обычно при выплавке27. Их подразделяют на полезные и вредные.
Среди компонентов сплава необходимо выделять основной элемент (матрицу сплава) - его содержится в сплаве более 50 %. В судостроении и судоремонте в качестве основы чаще всего используются железо, медь и алюминий. Остальные компоненты называются легирующими - в зависимости от решаемых задач это могут быть практически все элементы Периодической системы Д.А. Менделеева.
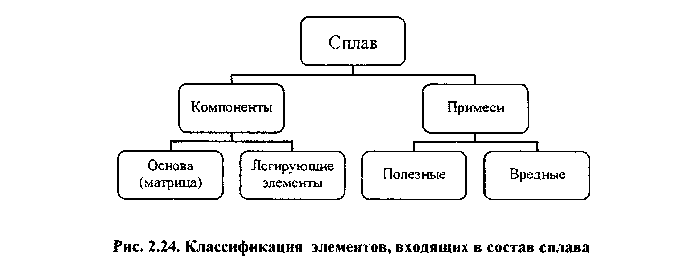
Входящие в состав сплавов элементы взаимодействуют между собой, образуя после затвердевания различные фазы (твердые растворы замещения и внедрения, химические соединения) и т.н. "механические" смеси. Фаза - это однородная часть системы, отделенная от другой границей раздела, при переходе через которую скачкообразно изменяются свойства.
Твердый раствор замещения представляет собой кристаллическую решетку, в которой атомы основного элемента А частично или полностью могут быть заменены атомами легирующего элемента В (см. рис. 2.6). Если такая замена возможна во всем интервале концентраций, то говорят о твердых растворах с неограниченной растворимостью в твердом состоянии (свойства атомов близки, а размеры отличаются не более чем на 8 %). Если же существует предел замещаемости, используют представление об ограниченной растворимости (различия в размерах - 8... 17 %).
Твердый раствор внедрения образуют атомы углерода, азота и других легирующих элементов с малыми размерами - они располагаются между атомами кристаллической решетки матрицы. Такие растворы, например, характерны для сплавов железа и углерода (диаметры атомов - 0,124 нм и 0,071 нм соответственно).
Химические соединения - результат взаимодействия, приводящего к возникновению сложного вещества типа AmBn„ с вполне определенным соотношением атомов, имеющего собственную кристаллическую решетку и резко отличающегося по свойствам от образующих его элементов.
Если при близких химических свойствах размеры атомов заметно отличаются, то это приводит к получению т.н. "механической" смеси. В этом случае каждый из элементов кристаллизуется отдельно, и лишь по границам зерен устанавливается неупорядоченное межатомное взаимодействие.
В материалах, используемых при постройке и ремонте судов, указанные сочетания встречаются достаточно часто. Так, коррозионностойкая сталь" представляет собой твердый раствор замещения атомами хрома атомов железа - основы сплава. Углерод в стали образует твердые растворы внедрения и химическое соединение - цементит. В свинцовистой бронзе медь (основа) и свинец (легирующий элемент) присутствуют в виде механической смеси.
Основные сведения о диаграммах состояния
Полную картину о взаимодействии элементов дает диаграмма состояния - графическое отображение зависимости между составом сплава, его температурой и строением в равновесном состоянии (отвечающем минимуму свободной энергии, достигается медленным охлаждением). С учетом природы образующих сплав элементов вид диаграммы может быть различным.
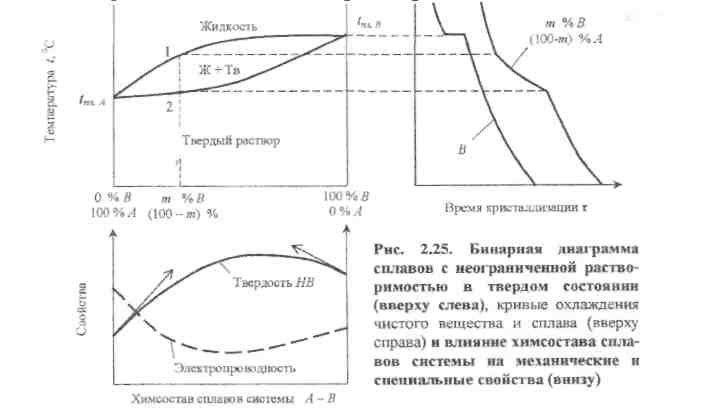
Рассмотрим, в качестве примера, наиболее простую бинарную диаграмму элементов А и В с неограниченной взаимной растворимостью в твердом состоянии (рис. 2.25). Состав сплавов системы отображается на оси абсцисс. Крайние точки соответствуют чистым компонентам А (левая) и В (правая). Между ними располагается семейство сплавов системы, в каждом из которых суммарное содержание компонентов равно 100 %. По оси ординат откладывается температура вещества.
Принципиально
важными для любой диаграммы являются
линии ликвидус и солидус. Выше
температур, образующих линию
ликвидус (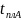 -
1-
-
1-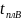 ),
все сплавы
системы однофазны и находятся в жидком
состоянии. Ниже линии
солидус (tплA
- 2 –
tплВ)
они
представляют собой твердые растворы.
Между ними система сплавов двухфазна
- наряду с жидкостью (расплавом) в
температурном интервале "1 - 2"
присутствуют и кристаллы твердого
раствора. Таким образом, сплошные линии
на диаграммах разделяют области диаграмм
с различным фазовым составом.
),
все сплавы
системы однофазны и находятся в жидком
состоянии. Ниже линии
солидус (tплA
- 2 –
tплВ)
они
представляют собой твердые растворы.
Между ними система сплавов двухфазна
- наряду с жидкостью (расплавом) в
температурном интервале "1 - 2"
присутствуют и кристаллы твердого
раствора. Таким образом, сплошные линии
на диаграммах разделяют области диаграмм
с различным фазовым составом.
Сравнение кривых охлаждения, построенных в системе координат "температура вещества - время" показывает, что в отличие от чистых веществ (кривая В), сплавы кристаллизуются (плавятся) в интервале температур.
Важнейшим качеством диаграмм состояния является тесная корреляция между составом и свойствами сплавов системы (рис. 2.24, внизу), что дает возможность прогнозировать поведение того или иного сплава с учетом механизма явления.
Рассмотрим это утверждение на примере твердости материала. Действительно, твердость характеризует способность материала подвергаться пластической деформации. Принимая во внимание, что легирование вещества А атомами вещества В означает повышение концентрации точечных дефектов (см. рис. 2.6, "в") и упрочнение материала (см. рис. 2.9), можно утверждать, что вектор изменения твердости положителен. Аналогичные рассуждения справедливы и в случае легирования вещества В атомами вещества А. В результате в системе А - В должен быть зафиксирован максимум твердости, а соответствующий ему сплав будет наиболее эффективным при изготовлении, например, режущего инструмента.
Проводя аналогичные рассуждения для такого свойства как электропроводность (способность вещества проводить электрический ток во внешнем электрическом поле) и учитывая, что дефекты препятствуют переносу зарядов, можно легко понять, почему в качестве проводников электрического тока используют чистые металлы, а нагревательные элементы (сопротивления) изготавливают из высоколегированных материалов (например, нихрома).
Диаграмма состояния "железо - углерод
Железоуглеродистые сплавы - стали и чугуны - имеют исключительно важное значения для любой отрасли техники, в том числе и для судостроения. Сталью называют сплав, который содержит до 2,14 % углерода, чугуном-2,14... 6,67 % С (речь идет о весовых %).
Таким образом, на практике используются только материалы с содержанием углерода до 6,67%. Оно отвечает цементиту - химсоединению Fe3C, что позволяет сузить концентрационную ось и говорить о диаграмме состояния "железо - цементит" (рис. 2.26).
В ней, в зависимости от внешних условий, могут существовать 5 фаз. Одна из них, жидкая (расплав) - находится выше линии ликвидус ACD. Ниже линии солидус AECF встречаются 2 твердых раствора внедрения с ограниченной растворимостью, химическое соединение и чистый компонент - С.
Феррит (Ф) - твердый раствор внедрения углерода в а - железе, имеющем кристаллическую решетку ОЦК. Область его существования в чистом виде (100 % Ф) - 0GSQ, пределы растворимости углерода - от 0 до 0,02 %(при температуре 727 °С). Максимальная температура существования - 911 °С (точка G диаграммы).
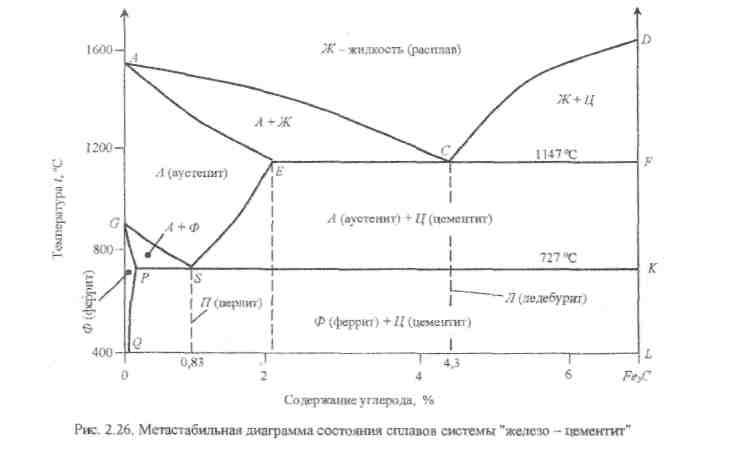
Аустенит (А) - твердый раствор внедрения углерода в у - железе с кристаллической решеткой ГЦК. Анализ его области AESG на диаграмме состояния показывает, что содержание С в нем может достигать 2,14 %, а температурный интервал существования составляет 727... 1539 °С.
Цементит (Ц) - химическое соединение (карбид железа) Fe3C, содержащее 6,67 % углерода. В чистом виде на диаграмме ему соответствует линия DFKL,
В остальных областях диаграммы состояния "железо - цементит" указанные фазы встречаются в различных сочетаниях.
Графит (Г) - наиболее устойчивая кристаллическая модификация чистого углерода. Следует отметить, что эта фаза присутствует только в стабильной диаграмме (т.е. полученной при очень медленном охлаждении расплава -до 2...4 суток, или при добавлении в него кремния и других компонентов) за счет частичного или полного распада цементита. Графит практически не встречается в сталях, однако является неотъемлемой составляющей второй группы железоуглеродистых сплавов - чугунов.
Помимо фазового состава, в сплавах системы нужно уметь выделять микроструктурные составляющие - однородные части системы, имеющие одинаковое строение (вид) под микроскопом. Перечисленные выше фазы - аустенит, феррит, цементит и графит - относятся к числу однофазных составляющих. Двухфазными микроструктурными составляющими являются перлит и ледебурит (см. ниже).
Рассматриваемая диаграмма относится к числу сложных. Помимо уже рассмотренных процессов кристаллизации и плавления (т.е. перехода из одного агрегатного состояния в другое), в сплавах данной системы в твердом состоянии могут происходить различные изменения. Для практики важное значение имеют следующие.
Полиморфное превращение чистого железа происходит при 911°С (точка С). При нагреве ОЦК - решетка переходит в гранецентрированную:

При охлаждении Fe направление реакции и, соответственно, кристаллическое строение меняется на противоположное.
Изменение растворимости углерода в твердых растворах (Ф и А) при увеличении или понижении температуры, отражаемое наклонными линиями диаграммы. Так, линия GS показывает, что при увеличении температуры аустенита от 727 °С до 911 °С содержание в нем углерода снижается от 0,83 % до 0 %.
Аустенитно-перлитное превращение происходит при охлаждении А, содержащего 0,83 % С, до температуры 727 °С: в нем наблюдается перераспределение углерода и он распадается на феррит и цементит:
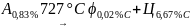
Образующаяся двухфазная смесь называется перлитом: П = Ф + Ц. Общее содержание в нем углерода остается неизменным - 0,83 %.
Для того, чтобы однозначно идентифицировать превращения на диаграммах состояния, вводится представление о критических точках - температурах, при которых происходит изменение фазового состава сплава (вещества). В железоуглеродистых сплавах важное для практики значение имеют следующие критические точки:
А1= 727 °С - температура аустенитно-перлитного превращения (линия PSK);
А3=911 ...727°С - минимальная температура существования аустенита при содержании в сплаве углерода в пределах 0... 0,83 % (линия GS);
Aст =727... 1147 °С - минимальная температура существования аустенита при содержании в сплаве углерода в пределах 0,83...2,14 % (линия SE).
Фазовые превращения и критические точки играют исключительно важную роль при проведении термической обработки металлов и сплавов.
Вопросы для контроля знаний при самостоятельной работе
Дайте определение: легирования, сплава, компонента, примеси, основного и легирующего элемента сплава
Приведите классификацию фаз в сплавах
Перечислите основные линии, встречающиеся в диаграммах состояния
Изобразите «стальной угол» диаграммы состояния «железо-цементит»
Перечислите основные критические точки на диаграмме состояния «железо-цементит», укажите их численные значения
Приведите формулу аустенитно-перлитного превращения при охлаждении
Дайте определение стали, чугуна, феррита, аустенита, цементита
Термообработка стальных деталей на судах
Несмотря на отсутствие специализированного оборудования на судах все же возможно проведение ряда термических операций, направленных на изменение свойств деталей в соответствии с условиями эксплуатации.
Термическая обработка самого распространенного на судах материала -стали, как правило, является комплексной и состоит из 2-х операций: закалки и последующего отпуска.
Сущность закалки состоит в повышении плотности дефектов кристаллического строения, приводящей к упрочнению - повышению твердости, прочности и других аналогичных свойств. Для достижения необходимого результата особое внимание необходимо уделить выбору следующих элементов режима термообработки:
температуры нагрева под закалку tзак;
охлаждающей среды (скорости охлаждения vохл).
Рассмотрим этот выбор на примере конструкционных углеродистых сталей (С 0,7 %). В исходном состоянии они являются двухфазным материалом, содержащим, в зависимости от марки:
98,8...89,5 % феррита - малопрочной, пластичной фазы, практически не содержащей углерод;
1,2... 10,5 % цементита - прочной, очень хрупкой фазы, в состав которой входит практически весь углерод, находящийся в стали.
Вполне очевидно, что упрочнение материала в целом должно происходить путем замены феррита на более прочную фазу. Для этого необходимо:
нагреть деталь до температуры выше критической А3, когда Ф исчезнет и превратится в аустенит - при этом за счет растворения цементита весь углерод окажется в аустените;
охладить деталь со скоростью выше критической, обеспечивающей подавление диффузионных процессов и сохранение расположения атомов С, характерного для высоких температур.
При такой последовательности действий образуется мартенсит - пересыщенный твердый раствор углерода в искаженной ОЦК-решетке железа (она имеет свое особое название - тетрагональная). Так, в закаленной на мартенсит стали 45 (0,45 % С) теоретическая степень пресыщения равна 75 - во столько раз возросла плотность образованных атомами углерода точечных дефектов, чем было до закалки в феррите. Практически результатом закалки является повышение прочности и снижение пластичности.
Численное значение критической точки А зависит от содержания в стали углерода. Поэтому на практике температура нагрева под закалку конструкционных углеродистых сталей, с учетом строения диаграммы состояния "железо-цементит", может быть вычислена по формуле:
tзак=911-220 С + 30...50°С
где С — определяемое по марке стали содержание в ней углерода, %.
При использовании легированных сталей температура нагрева под закалку на 60...80 °С выше определенных по приведенным формулам. Для ее точного нахождения необходимо обращаться к справочной литературе.
Контроль температуры нагрева на судах с наибольшей точностью осуществляют с помощью термопар, оптических или радиационных пирометров.
Однако даже их отсутствие особых трудностей не вызывает. При закалке визуально анализируется тепловое излучение стальной детали (свечение - цвета "каления"). При отпуске определяют цвета "побежалости" - цвет оксидной пленки железа, образующийся на поверхности и отвечающей вполне определенной температуре (табл. 2.16).
В интервале 330.,. 530 °С температура может быть определена с помощью простейших подручных средств. Так, при контакте с нагретой поверхностью в течение 2... 3 с сухая сосновая лучина сечением ~ 30 мм при 450 °С буреет, а при 490... 500 °С - вспыхивает.
В последнее время на суда стали поступать специальные наборы термореактивных красок, изменяющих свой цвет в зависимости от температуры поверхности, на которую они были нанесены.
Таблица 2.16- Соответствие цветов побежалости и каления температуре поверхности стальных деталей
Цвета побежалости |
t,°C |
Цвета каления |
t,°C |
Светло-желтый |
220 |
Темно-коричневый |
530. .580 |
Соломенно-желтый |
240 |
Коричнево-красный |
580... 650 |
Коричнево-желтый |
255 |
Темно-красный |
650... 730 |
Красно-коричневый |
265 |
Темно-вишневый |
730... 770 |
Пурпурно-красный |
275 |
Вишнево-красный |
770... 800 |
Фиолетовый |
285 |
Светло-вишнево-красный |
800... 830 |
Васильково-синий |
295 |
Светло-красный |
830... 900 |
Светло-синий |
315 |
Оранжевый |
900... 1050 |
Серый |
330 |
Темно-желтый |
1050...1150 |
Критическая скорость при закалке углеродистых сталей достигается путем охлаждения в воде, имеющей температуру около 20 °С. Для закалки легированных сталей используют, как правило, минеральные масла. Скорость охлаждения в них деталей оказывается в ~ 3...4 раза нюке, однако из-за меньшей подвижности атомов углерода, вызванной легированием (повышенное количество точечных дефектов), вполне достаточной для образования мартенсита.
Сущность отпуска - понижение плотности дефектов кристаллического строения в закаленном материале с целью повышения характеристик пластичности: ударной вязкости, относительного удлинения и сужения. В результате нагрева повышается диффузионная подвижность атомов углерода, позволяющая им вернуться в термодинамически более устойчивое состояние с меньшей свободной энергией.
Выбор температуры отпуска, как указывалось выше, производят с учетом условий работы деталей и характера изменения свойств предварительно закаленной стали в зависимости от температуры ее нагрева (рис. 2.34). В целом с повышением температуры отпуска происходит постепенное снижение прочностных характеристик и повышение пластичности материала. Поэтому, учитывая доминирующие эксплуатационные факторы, температуру и вид отпуска определяют как компромиссное решение.
Низкий отпуск (150...220 °С) используют для деталей, от рабочих поверхностей которых требуются высокая прочность, твердость, износостойкость, кавитационная стойкость: плунжеры и втулки топливных насосов высокого давления, кулачковые шайбы, элементы подшипников качения, шаберы, зубила и т.п. Образующийся мартенсит отпуска по этим показателям практически не уступает закаленному материалу. В то же время заметно возрастает пластичность, особенно ударная вязкость.
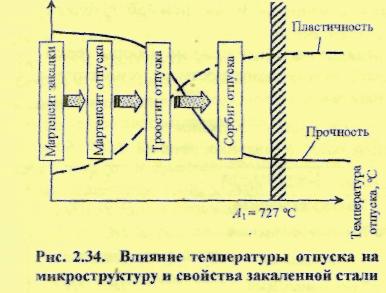
Средний отпуск (350...500 °С, микроструктура - троостит отпуска33) применяется для упругих элементов: пружин, рессор, мембран и других деталей, от которых требуется высокое значение предела упругости (пропорциональности).
Высокий отпуск при температуре 500...650 °С приводит к образованию сорбита отпуска, обладающего оптимальным сочетанием прочностных и пластических свойств. Сочетание закалки и высокого отпуска называется улучшением. Оно применяется при термообработке деталей, работающих в условиях значительных динамических нагрузок: поршневые пальцы, шестерни, анкерные связи и др.
Кроме перечисленных выше закалки и разновидностей отпуска, на судах довольно часто проводят отжиг стальных труб при ремонте трубопроводов. Газовой горелкой трубу нагревают до температуры 780...850 °С, что приводит к значительному повышению пластичности материала и в дальнейшем облегчает их гибку в имеющихся на судах трубогибах.
