
- •Державний вищий навчальний заклад
- •Міністерства освіти і науки України колоїдна хімія
- •Поверхневі явища й адсорбція
- •Адсорбція на межі "рідина - газ", "рідина - рідина"
- •Розрахунок параметрів адсорбційного шару
- •Закономірності адсорбції на поверхні твердих адсорбентів
- •Приклади розв’язку задач.
- •Задачі для самостійного рішення
- •2. Дисперсні системи та їх властивості
- •2.1. Загальна характеристика дисперсних систем
- •Класифікація дисперсних систем
- •Класифікація дисперсних систем за взаємодією дисперсної фази і дисперсійного середовища
- •Одержання і очищення колоїдних розчинів
- •2.2. Електрокінетичні явища в колоїдних розчинах
- •Коагуляція колоїдних систем
- •Властивості розчинів поліелектролітів
- •Застосування електрофорезу та електроосмосу
- •2.3. Мікрогетерогенні та грубодисперсні системи Загальна характеристика мікро гетерогенних та грубодисперсних систем
- •Суспензії
- •Емульсії
- •Аерозолі
- •Порошки
- •Приклади розв’язку задач.
- •Задачі для самостійного рішення.
- •Молекулярно-кінетичні властивості колоїдних систем
- •Броунівський рух
- •Осмотичний тиск
- •Седиментаційно-дифузійна рівновага
- •Приклади розв'язування задач
- •Задачі для самостійного розв'язування
- •Оптичні властивості колоїдних систем
- •Забарвлення колоїдних систем
- •Приклади розв'язування задач
- •Задачі для самостійного розв'язування
- •5. Розчини високомолекулярних сполук
- •Визначення молекулярних мас полімерів
- •Осмометричний метод
- •Віскозиметричний метод
- •Висолювання полімерів з розчинів
- •Набухання полімерів
- •Фізичні стани полімерів
- •Ділянка іі - високоеластичний стан; ділянка ііі - в'язкотекучий стан.
- •Напівколоїди Властивості розчинів напівколоїдів
- •Механізм утворення міцел.
- •Миюча дія мил
- •Структурно-механічні властивості зв'язанодисперсних систем
- •Приклади розв'язування задач
- •Теоретичні питання до контрольної роботи
- •Література
- •Колоїдна хімія
- •Навчально-методичне видання
- •Коваленко Данило Сергійович колоїдна хімія
- •Рецензент б.П. Зоря
Висолювання полімерів з розчинів
Розчини полімерів є істинними розчинами. Процес їх розчинення енергетично вигідний і супроводжується зменшенням вільної енергії Гіббса.
Полімер можна висолити з розчину. Висолювання — це виділення полімеру з розчину під дією великої кількості нейтральних солей. Енергія взаємодії іонів солі з молекулами води більша, ніж енергія взаємодії іонів з макромолекулами полімеру. Внаслідок цього полімер вилучається у вигляді окремої фази. За здатністю до висолювання іони розміщують у ліотропні ряди:

Набухання полімерів
Набухання - це самочинний процес поглинання низькомолекулярної рідини високомолекулярною речовиною, що супроводжується збільшенням її маси і об'єму.
Для оцінки якості деяких продуктів у товарознавстві широко використовують їх здатність до набухання. Печиво доброї якості повинно швидко і значно набухати у воді. Споживчі якості круп визначаються за їх здатністю поглинати воду при варінні. За ступенем набухання хліба визначається його свіжість. Відомо, що сушені плоди та овочі з низьким ступенем набухання погано розварюються і мають понижені споживчі властивості.
Набухання — вибіркове явище, тобто полімери здатні набухати в тих рідинах, які для них служать розчинниками. Желатин набухає у воді, каучук, гума - у вуглеводневих рідинах. Розрізняють два види набухання - необмежене і обмежене.
Необмежене набухання - це набухання, що переходить у повне розчинення (наприклад, каучук в бензолі, бензині). При обмеженому набуханні не проходить повного розчинення, набухання йде до певного визначеного (максимального) значення і подальший контакт з розчинником не змінює ні маси, ні об'єму полімеру (наприклад, набухання желатину у воді при кімнатній температурі, гуми в бензині).
Набухання характеризується ступенем набухання що означає масу рідини в грамах, яка поглинулась протягом певного часу і при певній температурі одним грамом полімеру:
![]()
де
![]() -
маса полімеру для набухання, г;
-
маса полімеру для набухання, г;
![]() -
маса полімеру після набухання до певного
часу t,
г.
-
маса полімеру після набухання до певного
часу t,
г.
Крива обмеженого набухання наведена на рис.24.
На ступінь набухання в одному і тому ж розчиннику впливає температура, тиск, рН середовища, наявність електролітів.
Швидкість набухання описується кінетичним рівнянням швидкості реакції першого порядку:
![]() ,
,
де
![]() -
швидкість набухання;
-
швидкість набухання;
- константа швидкості що залежить від природи полімеру, природи розчинника і температури;
![]() -
граничний ступінь набухання;
-
граничний ступінь набухання;
![]() -
ступінь набухання за певний час.
-
ступінь набухання за певний час.
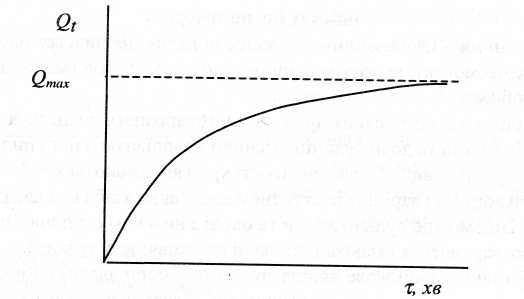
Рис.24. Крива обмеженого набухання.
Виходячи з рівняння швидкості реакції першого порядку, можна визначити константу швидкості набухання полімеру за рівнянням:
![]()
За процесом набухання можна спостерігати, періодично зважуючи полімерну речовину (ваговий метод), або вимірюючи об'єм рідини, що залишилась після набухання (об'ємний метод).
Фізичні стани полімерів
Залежно від температури полімери перебувають у трьох фізичних станах: склоподібному, високоеластичному та в'язкотекучому. Від фізичного стану полімерів залежать їх механічні властивості. Дослідження переходу полімеру з одного стану в інший, залежно від температури, проводять термомеханічним методом. Цей метод полягає в тому, що до зразка полімеру, закріпленого на кронштейні, прикладають постійне фізичне навантаження і плавно підвищують температуру. Схема установки для дослідження термомеханічних властивостей наведена на рис.25.
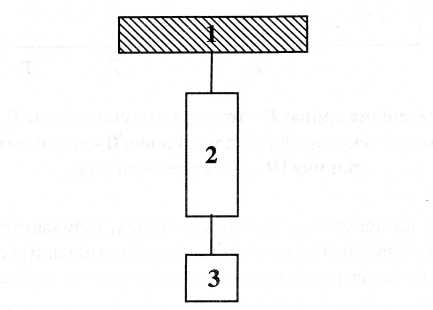
Рис.25. Установка для дослідження термомеханічних властивостей полімерів: 1 - кронштейн; 2 - зразок полімеру; 3 - постійне навантаження.
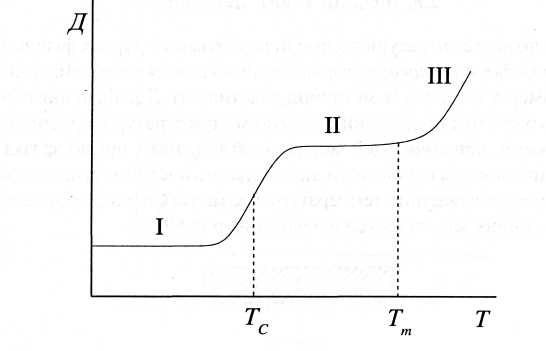
З підвищенням температури визначають деформацію зразка. Будують графічну залежність деформації від температури, яка називається термомеханічною кривою. Типовий вигляд цієї кривої зображений на рис.26.
 На
термомеханічній кривій спостерігається
два перегини. Перпендикуляри, опущені
з середини перегинів на вісь абсцис,
На
термомеханічній кривій спостерігається
два перегини. Перпендикуляри, опущені
з середини перегинів на вісь абсцис,
Рис.26. Термомеханічна крива: Тс—температура скловання;
Т –температура текучості; ділянка І - склоподібний стан;
