
5 Одержання бензолу
Промислове одержання
Каталітичний реформінг (ізомерізація) алканів


Напівкоксування вугілля
Нагрівання вугілля у відсутності повітря призводить до утворення вугільного газу, смоли, підсмольної води та напівкоксу
Вугільна смола - це суміш різних органічних сполук, здебільш ароматичної будови
В такий спосіб можуть бути одержані бензол та толуол.
Лабораторні методи
Сплавлення натрієвої солі бензойної кислоти з лугом

Відновлення фенолу
Пари фенолу повільно пропускають через нагрітий порошок цинку з утворенням бензолу і оксиду цинку

Тримеризація алкінів
(лекція 5.3)
Одержання алкілбензолів
Взаємодія металічного Na з сумішшю галогеналканів і галогенбензолу
![]()
6 Хімічні властивості бензолу
Порівняльна характеристика хімічних властивостей циклогексану, циклогексену і бензолу
Реакція |
Циклогексан (насичений аліциклічний вуглеводень) |
Циклогексен (ненасичений аліциклічний вуглеводень) |
Толуол (ароматичний вуглеводень) |
Взаємодія з Br2 в CH3Cl3 (в темряві) |
Не взаємодіє |
Br2 знебарвлення розчину без виділення HBr |
Не реагує з Br2 без каталізатору В присутності FeBr3, Br2 знебарвлюється і виділяється HBr |
Взаємодія з H2 (в присутності Ni каталізатору) |
Не взаємодіє |
1 моль циклогексену взаємодіє з 1 молем H2 за кімнатної температури |
1 моль толуолу взаємодіє з 3 молями H2 в умовах підвищеної температури під тиском. |
Взаємодія з розведеним KMnO4 |
Не взаємодіє |
KMnO4 знебарвлюється |
Не взаємодіє |
Взаємодія з конц. HNO3 та конц. H2SO4 |
Не взаємодіє |
Цтклогексен окислюється і колір темніє |
Утворюється рідина жовтого кольору |
Не зважаючи на те, що толуол є високоненасиченою сполукою він стійкий до окиснення і реакцій приєднання
Ці властивості використовують для розділення ароматичних і ненасичених сполук
Толуол взаємодіє з Br2 в присутності FeBr3. Ця реакція відбувається за механізмом заміщення
Реакції ароматичних сполук за механізмом електрофільного заміщення
Найбільш характерні реакції для ароматичних сполук:
Реакції електрофільного заміщення

В результаті електрофільної атаки бензольного кільця, відбувається заміщення одного атому водню
Роль електрофілу може відігравати катіон (E+) або інша електон-дифіцитна частинка з частковим позитивним зарядом (d+)
Механізм реакції електрофільного заміщення ароматичних сполук
Електрофіл атакує бензольне кільце з утворенням нестабільного ароматичного π- комплексу

Повільне утворення нового C-E зв’язку є лімітуючою стадією утворення неароматичного карбокатіону, проміжного σ- комплексу:

σ-комплекс втрачає протон з утворенням нейтрального заміщеного продукту
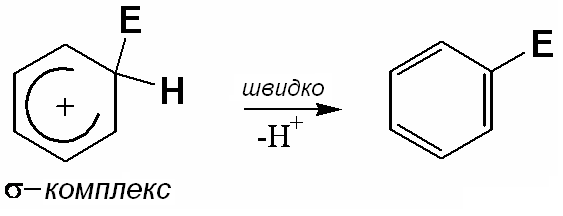
Електрофільні реакції заміщення ароматичних сполук

Галогенування
Бензол реагує з хлором та бромом в присутності каталізаторів типу AlCl3, FeCl3, FeBr3, з утворенням хлорбензолу або бромбензолу, відповідно.

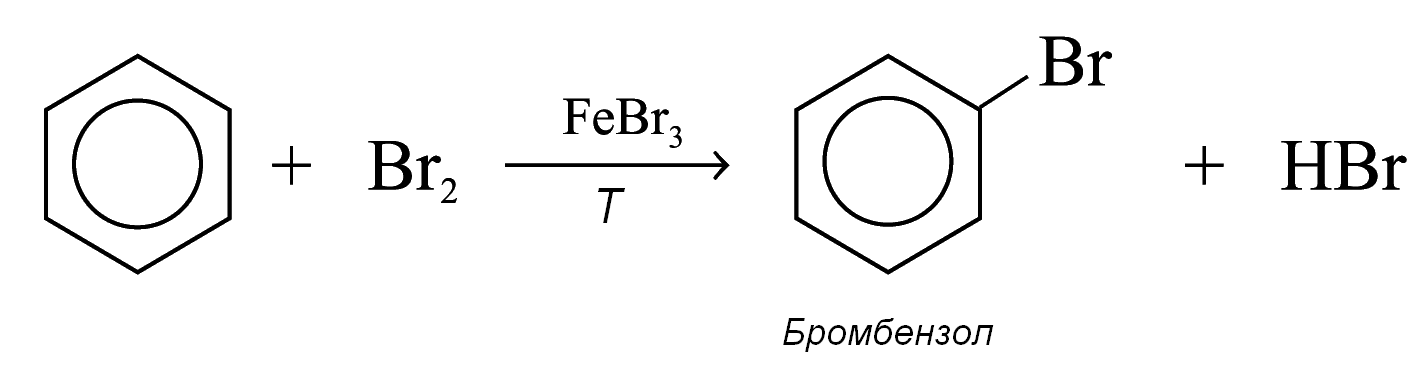
Нітрування

Конц. H2SO4 підвищує вихід реакції за рахунок збільшення концентрації електрофілу - NO2+ іону
Сульфування
Бензол реагує з димлячою сірчаною кислотою за кімнатної температури з утворенням бензолсульфокислоти

Нагрівання водного розчину бензолсульфокислоти біля 100°C, веде до розкладання останньої на бензол та сірчану кислоту

Алкілування за Фріделем-Крафтсом
В результаті нагрівання бензолу з галогеналканами в присутності каталізаторів типу AlCl3 утворюються алкіл бензоли

Ароматичний цикл повинен мати щонайменше таку ж активність як галогенбензол. Дезактивований цикл не вступає в реакцію.
Ацилювання за Фріделем-Крафтсом
Ацильна група, -COR вводиться в кільiце в результаті реакції бензолу з галогенангідридами карбонових кислот

Електронні ефекти в заміщених ароматичних кільцях
Замісники, що присутні в циклі можуть проявляти два типи ефектів :
Ефект активації (дезактивації) бензольного кільця. Деякі замісники активують кільце, роблячи його більш активним порівняно з бензолом, інщі дезактивують бензольне кільце.
Орієнтаційний ефект в реакціях подальшого заміщення. Природа замісника, що уже присутній в бензольному ядрі визначає позицію наступного замісника.
