
- •Спектроскопия. Что такое спектроскопия?
- •Техника спектрального анализа.
- •«Ударное» уширение.
- •Зависимость интенсивности спектральных линий от концентрации пробы..
- •Источники света. Общие требования к источникам света.
- •Дуга постоянного тока.
- •Стабилизация дуги.
- •Плазмотрон.
- •Дуга переменного тока.
- •II. Спектральные приборы.
- •Кривизна спектральных линий.
- •Дифракционная решетка.
Техника спектрального анализа.
Большинство установок для спектрального анализа условно можно разбить на три составляющие: I. источник света; II. спектральный прибор; III. Регистратор света.
Рис.1. Составляющие спектрального прибора.
Возбуждение спектров и источники света.
При нагревании газа до температур выше 800-1000 °С он начинает светиться. С увеличением температуры яркость свечения возрастает, и максимум интенсивности сдвигается в коротковолновую часть спектра. Для каждого вещества одновременно наблюдаются спектры трех типов:
Линейчатые. Они появляются в результате электронных переходов внутри атомов и ионов различных элементов.
Полосатые. Эти спектры характерны для молекул и являются результатом изменения электронной, колебательной (вибрационной) и вращательной (ротационной) энергии молекулы. В случаях, когда вращательная структура хорошо разрешена, полоса представляет собой отчетливую последовательность отдельных линий. Если структура не разрешена (не хватает разрешения спектрального прибора), то полоса выглядит в виде участка сплошного спектра.
Сплошные спектры. Помимо неразрешенных полос сплошной или непрерывный фон появляется в результате того, что свободные электроны нагретого газа, пролетая мимо ионов, изменяют вектор скорости своего движения, что приводит к излучению световой энергии. Электроны также могут быть захвачены положительно заряженными ионами. В результате этого также излучается энергия. Излучаемая свободными электронами энергия может иметь всевозможные значения (здесь нет дискретных квантовых уровней, обусловливающих линейчатую структуру спектра). Поэтому наряду с линейчатыми и полосатыми спектрами всегда существует непрерывный спектр, обязанный своим происхождением свободным электронам.
Возможны и другие механизмы излучения сплошного спектра, например, свечение накаленных частиц твердых тел (частицы электродов, пыли и т.п.).
В спектральном анализе чаще всего используются атомные, а иногда молекулярные спектры. Поэтому сплошной спектр всегда является источником помех, и по возможности его стараются ослабить.
В общих чертах возбуждение спектральных линий в источнике излучения происходит следующим образом. При достаточно высокой температуре газа среди его частиц много таких, энергия движения которых сравнима с энергией ионизации и химической связи. Поэтому в результате столкновений достаточно часто происходят процессы диссоциации и ионизации. Это приводит к появлению в газе помимо атомов и молекул также свободных электрических зарядов – в разном количестве положительных и отрицательных (ионов и электронов), что обеспечивает его электропроводность. Такой частично ионизированный газ называется плазмой. Джоулево тепло, выделяемое при прохождении электрического тока, поддерживает высокую температуру газа, необходимую для возбуждения свечения плазмы в таких источниках, как дуга и искра.
По мере роста температуры степень ионизации газа возрастает и, наряду с однократно ионизованными, появляются двух– и трехкратно ионизованные атомы.
Зависимость степени ионизации от температуры описывается формулой Саха:
![]() ,
(1)
,
(1)
где M0, N0, Ne - соответственно концентрации ионов, атомов и электронов; А – постоянная, зависящая от атомных констант; Еi – энергия ионизации; к – постоянная Больцмана; Т – температура газа.
Возбуждение спектральных линий.
К возбуждению спектральных линий приводят неупругие столкновения, приводящие к изменению кинетической и потенциальной энергий рассматриваемой системы. Например, невозбужденный атом А, сталкиваясь с достаточно быстрым электроном, может перейти в возбужденное состояние А*, а электрон теряет часть кинетической энергии, которая переходит в энергию возбуждения атома. Такой процесс называют ударом первого рода. Если возбужденный атом, столкнувшись с электроном, перейдет в нормальное состояние, отдав энергию возбуждения электрону, то такого рода процесс называют ударом второго рода.
Возбуждение определенного энергетического уровня атома может происходить различными путями. Рассмотрим эти возможные пути на примере схемы энергетических уровней атома натрия (см. рис.2). Для определенности возьмем возбужденное состояние 2 2Р3/2 . Это состояние может появляться, во – первых, в результате столкновения нормального атома (в основном состоянии) 12S1/2 с электроном либо с другой достаточно энергетичной частицей. Кроме того, атом может перейти из состояния 12S1/2 в состояние 22Р3/2 при поглощении кванта, частота которого соответствует энергии этого перехода.
Наконец, атомы могут попадать в состояние 22Р3/2 при излучении света: на уровень 22Р3/2 , как видно из рисунка 2 , возможны сопровождаемые излучением переходы с уровней 22 S1/2, 32 S1/2 , 32 D3/2, 5/2 , 42 D3/2, 5/2 и т.д. Следует учесть также, что состояние 22Р3/2 может образовываться в результате ударов второго рода, приводящих к распаду более высоких энергетических уровней, а также в результате диссоциации молекул, содержащих атомы натрия.
Переход атомов из энергетического состояния 22Р3/2 в какое – либо другое состояние возможен также в результате целого ряда процессов: спонтанного излучения с возвратом в нормальное состояние атома (λ = 5889,96 Ǻ ); индуцированного (вынужденного) излучения этой же линии под воздействием светового излучения на возбужденный атом; ударов второго рода, также возвращающих атом в нормальное состояние; ударов первого рода, приводящих к переходу атома в более высокое энергетическое состояние и т. д.
Если установились какие – то постоянные условия возбуждения, то количество атомов в данном состоянии будет определяться тем, что в каждый промежуток времени число актов, приводящих к заселению данного уровня, должно равняться числу актов, приводящих к его распаду.
Мощность, излучаемая единицей объема источника для частоты νkr, или интенсивность спектральной линии, соответствующей рассматриваемому переходу, будет определяться выражением:
Ikr = NkАkrhνkr, (2)
где Аkr - вероятность спонтанного перехода из состояния k в состояние r , Νк - число атомов (на 1 см3) в k-oм состоянии возбуждения, h- постоянная Планка, hνkr – энергия излучаемого кванта. (При этом предполагается, что интенсивностью индуцированного излучения можно пренебречь: последнее условие практически всегда имеет место в распространенных источниках света, применяемых в спектральном анализе). Кроме того, считается, что излучаемый
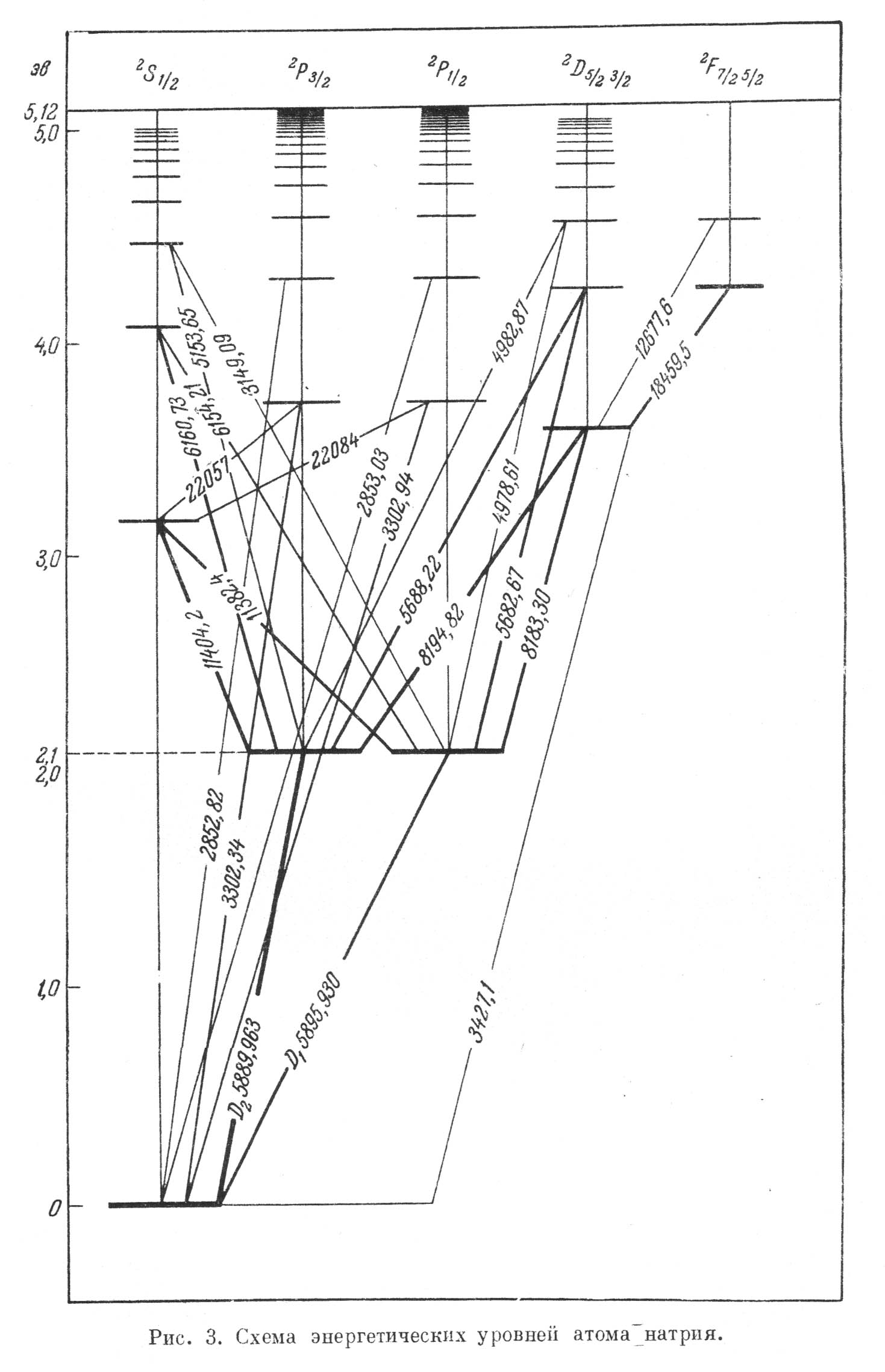
Рис.2. Схема энергетических уровней атома натрия.
свет не поглощается при прохождении через плазму. Таким образом, интенсивность спектральной линии определяется вероятностью соответствующего перехода, которая является атомной константой и концентрацией возбужденных атомов Νk. Последняя пропорциональна концентрации невозбужденных атомов данного элемента, содержащихся в плазме, и определяется совокупностью всех процессов, приводящих к заселению и распаду данного уровня. В общем виде учет всех этих процессов практически не возможен, так как обычно нет сведений о вероятностях каждого из них. Для нахождения числа возбужденных атомов, образующихся только при столкновениях нормальных атомов с электронами, необходимо знать кроме вероятности возбуждения и ее зависимости от скорости электронов, также и концентрацию электронов и их распределение по скоростям.
Эти сведения получить очень трудно, и поэтому расчеты такого рода могут быть сделаны лишь в очень грубом приближении, с возможной ошибкой в десятки и сотни раз.
Однако существует один практически важный случай, когда вычисления значительно упрощаются – это случай термически равновесной плазмы, когда плазма не обменивается энергией с внешним пространством и обмен энергией возможен только между частицами самой плазмы.
В такой плазме средняя кинетическая энергия поступательного движения атомов, ионов и электронов одинакова и равна 3/2кТ, а скорости всех частиц распределены по закону Максвелла:
![]() ,
(3)
,
(3)
где dΝ
– концентрация частиц, имеющих
относительную скорость в интервале от
![]() до
до
![]() (относительная
скорость
– безразмерное число, равное отношению
скорости частицы к наивероятнейшей).
При этом имеет место распределение
атомов по степеням возбуждения,
определенное законом Больцмана:
(относительная
скорость
– безразмерное число, равное отношению
скорости частицы к наивероятнейшей).
При этом имеет место распределение
атомов по степеням возбуждения,
определенное законом Больцмана:
![]() ,
(4)
,
(4)
где Ν0 и Νк - концентрации нормальных и возбужденных (до уровня k) атомов, Ек - энергия возбуждения k-го уровня, gк и g0 - статистические веса возбужденного и нормального состояний. Подстановка численных значений констант приводит к более удобному для расчетов выражению:
![]() (5)
(5)
Здесь Е к выражена в электронвольтах , Т – в градусах. Концентрация ионов в этих условиях вычисляется по формуле Саха (1). Если температура не слишком высока, и можно не рассматривать уменьшение концентрации невозбужденных атомов из–за ионизации и заселения возбужденных энергетических состояний, то можно положить Ν 0 = Ν, где N – общая концентрация атомов данного элемента в плазме. При этом полагается, что ближайшее возбужденное состояние отстоит от нормального достаточно далеко. Тогда из (2) и (4) для интенсивности Ikr спектральной линии для перехода между уровнями к и r получается выражение :
![]() .
(6)
.
(6)
Анализ выражения (6) показывает, что если Ек сравнима с kТ, то интенсивность спектральной линии сильно зависит от температуры.
При Е к kТ интенсивность соответствующих линий стремится к нулю. Если же Е к kТ, то экспонента 1, и интенсивности делаются независимыми от температуры. Однако в этом случае уже нельзя пользоваться приближением Ν = Ν 0 и следует учитывать убывание Ν 0 с ростом температуры. С ростом температуры растет также число ионов. Это приводит к тому, что при высоких температурах интенсивности линий атомов начинают убывать, а интенсивности линий от возбужденных ионов возрастают.
В реальной плазме полное термодинамическое равновесие невозможно. В ней есть потери за счет излучения, теплопроводности, ухода быстрых частиц и т.п. С другой стороны, энергия плазмы непрерывно пополняется за счет электрического тока или химических реакций (если в пламени). В стационарном состоянии мощность, поступающая в плазму, равна потерям. Насколько плазма далека от равновесия, зависит от соотношения между числом столкновений в единицу времени и величиной энергетических потерь. При больших давлениях число столкновений велико, и если отдаваемая мощность невелика, то плазма практически равновесна. Это имеет место в дугах и искрах при атмосферном давлении. В газовом разряде при низком давлении, когда велика длина свободного пробега, отступления от равновесия велики. Это сказывается в том, что ускоряемые в электрическом поле электроны имеют гораздо большую кинетическую энергию, чем атомы. Т.е. электронная температура гораздо выше атомной. А температура ионов выше температуры атомов и ниже температуры электронов.
Как уже говорилось, вычисление интенсивностей спектральных линий в термически неравновесной плазме практически невозможно. Однако, пренебрегая возбуждением атомов от тяжелых частиц по сравнению с электронами, можно вычислять интенсивности спектральных линий, пользуясь выражением (5), понимая в нем под Т не температуру плазмы, а температуру электронного газа Те.
Во всех случаях, когда распределение атомов по возбужденным состояниям соответствует закону Больцмана, температуру, соответствующую данному распределению, называют температурой возбуждения (Тв). Последняя обычно близка к температуре электронного газа Те. В том случае, когда для какой – то температуры можно написать больцмановское распределение, для отношения интенсивностей двух линий, одна из которых соответствует переходу между уровнями і и k, другая уровнями ℓ и m , из ( 6 ) можно получить :
![]() .
(7)
.
(7)
Отсюда видно, что отношение Iiк /Iℓm зависит только от атомных констант и температуры возбуждения. Соотношение (7) обычно служит для определения температуры возбуждения.
Возбуждение молекулярных полос и сплошного спектра.
Так как энергии связи большинства молекул не превышают нескольких эВ, то при температурах горячих источников света основная часть молекул диссоциируется. Молекулярные же спектры наиболее прочных радикалов и молекул, например CaO, OH, AlO, SiO, наблюдаются в периферических, более холодных частях плазмы электрической дуги, а также в пламенах.
В газоразрядных трубках малого давления наблюдаются молекулярные спектры простых молекул, которые часто используются для анализа. Энергиям возбуждения электронных уровней молекул соответствуют видимая и УФ-области спектра. На каждый из электронных уровней накладываются колебательные и вращательные переходы. Расстояние между соседними вращательными уровнями так мало, что линии вращательной структуры составляют тесную последовательность, которая зачастую плохо разрешается спектральным прибором и выглядит как участок сплошного спектра. Распределение интенсивности внутри полосы связано с распределением молекул по вращательным состояниям. Концентрация возбужденных молекул ΝJ, которым соответствует вращательное квантовое число J, задается выражением, аналогичным (4):
![]() ,
(8)
,
(8)
где Ν0 – заселенность основного вращательного уровня , а В – вращательная постоянная.
Это выражение, как и (4), справедливо только для случая термического равновесия и может служить для определения температуры плазмы. Если измеренная по распределению интенсивностей вращательной структуры температура не совпадает с той, которая определена по интенсивности спектральных линий, то это говорит о неравновесности плазмы.
Ширина спектральных линий.
Реальная линия не может быть строго монохроматичной, и соответствующая ей энергия распределена в некотором интервале длин волн. Излучение даже изолированного покоящегося атома вследствие соотношения неопределенностей немонохроматично.
Это соотношение записывается в виде
![]() ,
(9)
,
(9)
где Е
– энергия терма, t
– среднее время жизни возбужденного
состояния,
h – постоянная
Планка. Поэтому положение спектрального
терма может быть определено с точностью
до
![]() ,
и лишь с соответствующей точностью
может быть определена длина волны
спектральной линии, излучаемой при
переходе с этого терма. Так как для
излучающих уровней время жизни
возбужденного состояния ≈ 10-8сек,
то для λ
в средней
части спектра получается величина ≈
10 -3 Ǻ
.
,
и лишь с соответствующей точностью
может быть определена длина волны
спектральной линии, излучаемой при
переходе с этого терма. Так как для
излучающих уровней время жизни
возбужденного состояния ≈ 10-8сек,
то для λ
в средней
части спектра получается величина ≈
10 -3 Ǻ
.
Определенная из (9) ширина спектральной линии носит название естественной ширины. При решении большинства аналитических задач естественной шириной пренебрегают, т.к. она много меньше уширений, обусловленных другими причинами.
Доплеровское уширение.
Это уширение является следствием движения излучающих атомов. Известно, что если источник света движется вдоль линии наблюдения со скоростью V, то излучаемая им длина волны λ испытывает смещение, определяемое соотношением:
![]() (10)
(10)
(оно верно, когда
![]() ,
с
– скорость света).
,
с
– скорость света).
В равновесном источнике скорости атомов распределены по закону Максвелла, и учет этого распределения приводит к следующей зависимости интенсивности излучения от длины волны:
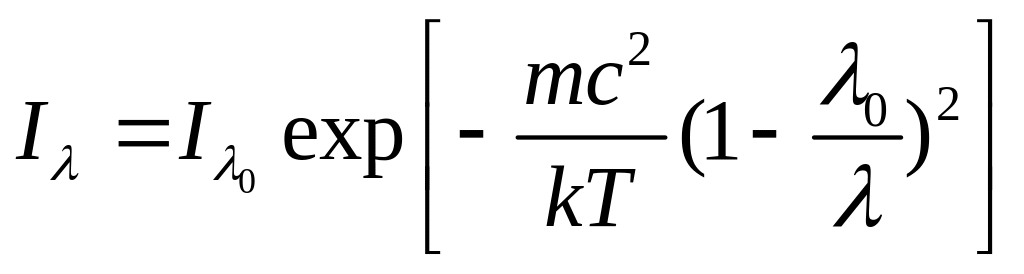 ,
(11)
,
(11)
где
![]() -
интенсивность в максимуме, длина волны
которого
λ0
, m-масса
излучающего атома.
-
интенсивность в максимуме, длина волны
которого
λ0
, m-масса
излучающего атома.
Назовем величину
λD,
равную
расстоянию между ординатами кривой (
11 ), для которых
![]() ,
доплеровской шириной спектральной
линии. Тогда из ( 11 ) легко получается
,
доплеровской шириной спектральной
линии. Тогда из ( 11 ) легко получается
![]() ,
(12)
,
(12)
где А - атомный вес.
Из этого выражения видно, что доплеровское уширение больше для легких атомов и растет с увеличением температуры.
Для атомов средней части периодической системы в обычной дуге (Т≈5000°) доплеровская ширина составляет в видимой области спектра 0,01-0,02 Ǻ , что легко может быть замечено на приборах с большой дисперсией.
