- •Основні правила охорони праці
- •Лабораторна робота № 2
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Теоретична частина
- •Експериментальна частина
- •Список рекомендованих джерел:
Експериментальна частина
№ п/п |
Хід роботи |
Спостереження |
Висновки |
1. |
Реакція з фелінговою рідиною. До розчинів глюкози, мальтози, сахарози, крохмалю об’ємом 1 см3 в окремих пробірках прилити реактив Фелінга об’ємом 1 см3. Нагрівати верхню частину суміші до початку кипіння. |
|
|
2. |
Реакція Селіванова на кетони. У 2 пробірки прилити реактив Селіванова об’ємом 3 см3. В одну з них додати розчин фруктози (3 краплі), в іншу – розчин глюкози (3 краплі). Обидві пробірки помістити у водяну баню на 8 хвилин. |
|
|
3. |
Реакція крохмалю і глікогену з йодом. У першу пробірку додати розчин крохмалю об’ємом 3 см3, у другу – розчин глікогену об’ємом 3 см3. В обидві пробірки додати розчин Люголя (1-2 краплі). |
|
|
4. |
Реакція Барфеда. До реактиву Барфеда об’ємом 2,5 см3 додати розчин цукру об’ємом 0,5 см3. Суміш гріти на водяній бані 10 хвилин. |
|
|
5. |
Гідроліз крохмалю. У пробірку налити розчин крохмалю (w = 1 %) об’ємом 5 см3; розчин H2SO4 (w = 10 %) об’ємом 3-5 см3. На кахельну плитку нанести 10 крапель йоду (I2/KI). Пробірку з крохмалем нагрівати на протязі 10-15 хвилин. Кожну хвилину відбирати скляною паличкою пробу для реакції з йодом. Якщо забарвлення йоду не змінюється, гідролізат нейтралізувати сухим NaHCO3 і провести реакцію з реактивом Фелінга. |
|
|
Загальний висновок: _________________________________________________________________________________________
_____________________________________________________________________________________________________________
_____________________________________________________________________________________________________________
_____________________________________________________________________________________________________________
_____________________________________________________________________________________________________________
ЛАБОРАТОРНА РОБОТА № 4
Тема: Якісні реакції білків і амінокислот
Мета: Набути вміння здійснювати якісні реакції білків.
Завдання:
Виявити наявність пептидного зв’язку (біуретова реакція).
Виявити наявність залишків α–амінокислот (нінгідринова реакція).
Здійснити реакції на виявлення окремих амінокислот (реакції Паулі, Адамкевича, ксантопротеїнова).
Теоретична частина
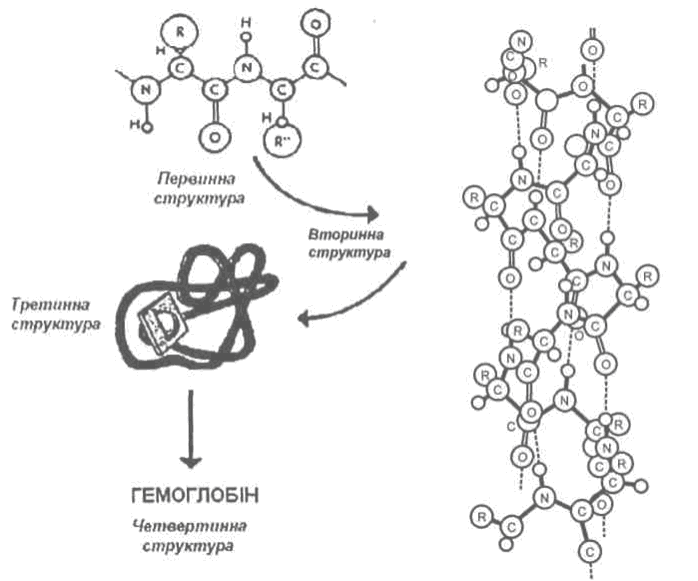
Білки – це високомолекулярні сполуки, які складаються з залишків α-амінокислот зв’язаних між собою пептидними зв’язками. В білках розрізняють чотири рівні структури – первинну, вторинну, третинну і четвертинну.
Первинна структура – це послідовність розміщення залишків α-амінокислот у поліпептидному ланцюгу. Вторинна структура – це розташування у просторі поліпептидного ланцюгу у вигляді α-спіралі або β-структури. Третинна структура – це просторове розташування α-спіралі або β-структури з утворенням субодиниць. Четвертинна структура – це об’єднання субодиниць у епімолекулу.