
Сульфанілова кислота
Сульфанілову отримують дією сульфатної кислоти на анілін.

Реактиви:
1. Анілін свіжоперегнаний (4.7 мл, 1.03 г/мл).
2. Сульфатна кислота концентрована (2.7 мл, 1.8 г/мл).
3. Вугілля активоване.
У фарфорову чашку вносять 4.7 мл свіжоперегнаного аніліну та невеликими порціями при струшуванні додають 2.7 мл конц. сульфатної кислоти. Суміш сильно розігрівається. Чашку накривають азбестом та нагрівають на піщаній бані при 170‑180оС (температура бані) 1.5‑2 год. Закінчення реакції встановлюють таким чином: пробу реакційної маси розчиняють у невеликій кількості води та додають конц. розчин гідроксиду натрію до лужної реакції. Якщо при цьому виділяються краплини аніліну. нагрівання слід продовжити.
Після закінчення реакції реакційну масу, дещо охолодивши, ще гарячою виливають, перемішуючи скляною паличкою, у стакан. що містить 100 мл холодної води (обережно!). Випадають кристали сульфанілової кислоти. Суміш охолоджують у бані з холодною водою, осад фільтрують, промиваючи фільтратом та мінімальною кількістю крижаної води.
Для очищення сиру сульфанілову кислоту переносять до стакану та розчиняють у мінімальній кількості гарячої води, додаючи активоване вугілля. Суміш кип’ятять 5 хв., фільтрують крізь складчастий фільтр на воронці для гарячого фільтрування. При охолодженні з фільтрату випадають пластівці дигідрату сульфанілової кислоти. Суміш охолоджують льодом, кристали фільтрують, промивають фільтратом та мінімальною кількістю крижаної води. Сушать між аркушами фільтрувального паперу.
Вихід близько 11 г. При тривалому зберіганні кристалізаційна вода поступово зникає.
Дигідрат втрачає кристалізаційну воду при 100оС. Безводна сульфанілова кислота: т. пл. 280-300оС (розкл.).
Допуск до роботи: техніка безпеки, схема реакції, розрахунки кількостей речовин, записи у журналі, хід виконання роботи.
Здача роботи: зовнішній вигляд, вихід продукту. Механізм реакції. Особливості проведення реакції електрофільного заміщення для похідних аніліну.
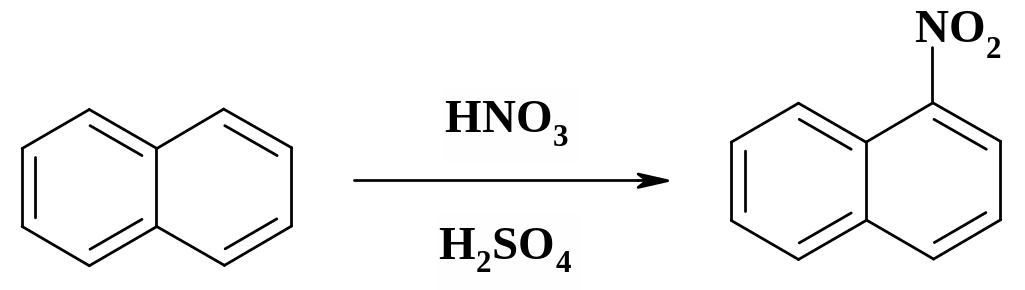
1-Нітронафталін
1‑Нітронафталін отримують нітруванням нафталіну сумішшю сульфатної та нітратної кислот.
Реактиви:
1. Нафталін (4.3 г).
2. Сульфатна кислота концентрована (4.2 мл, 1.8 г/мл).
3. Нітратна кислота концентрована (3.1 мл, 1.4 г/мл).
4. Метанол.
Вказану кількість сульфатної кислоти змішують з 7 мл води та зі вказаною кількістю нітратної кислоти. До цієї суміші, нагрітої до 50ºС, додають дрібно розтертий нафталін та ведуть реакцію 1 годину при вказаній температурі при перемішуванні паличкою. Після цього підвищують температуру до 60ºС та перемішують суміш при цій температурі ще 1 годину. Увага! Швидке нагрівання суміші призводить до екзотермічного та неконтрольованого полінітрування та окиснення, що призводить до втрати продукту.
Після цього суміш охолоджують. Нітронафталін плаває на поверхні суміші у вигляді коржу. Рідину декантують, а сирий нітронафталін топлять у киплячій воді при перемішуванні (тяга!). Суміш охолоджують, рідину зливають. Топлення у киплячій воді повторюють ще 2 рази. При такій обробці більша частина вихідного нафталіну відганяється з водяною парою. Після останнього топлення гарячий продукт вливають в холодну воду, в якій він застигає у вигляді маленьких світло-жовтих кульок. Осад фільтрують, віджимають між листами фільтрувального паперу та сушать на повітрі. Вихід близько 5 г.
Отриманий препарат можна без очищення використовувати для отримання 1‑нафтиламіну.
Для отримання чистого 1‑нітронафталіну отриманий продукт після висихання кристалізують з метанолу. Т. пл. 61.5ºС.
Допуск до роботи: техніка безпеки, схема реакції, розрахунки кількостей речовин, записи у журналі, хід виконання роботи.
Здача роботи: зовнішній вигляд, вихід продукту. Механізм реакції. Особливості сульфування та нітрування нафталіну (термодинамічний та кінетичний контроль реакції).
1-Нафтиламін
1‑Нафтиламін отримують відновленням 1‑нітронафталіну цинком в присутності кислоти.

Реактиви:
1. 1‑Нітронафталін (3.5 г).
2. Цинк гранульований (3 г).
3. Хлоридна кислота концентрована (15 мл, 1.19 г/мл).
У колбі місткістю 100 мл розчиняють 1‑нітронафталін у 15-20 мл етанолу, додають вказану кількість хлоридної кислоти та злегка підігрівають. В отриманий розчин поступово вносять цинк.
Після додавання всього цинку витримують суміш при 50ºС 30 хвилин. Після цього гарячий розчин фільтрують на складчастому фільтрі. Маточний розчин охолоджують холодною водою. З фільтрату при охолодженні випадають кристали гідрохлориду 1‑нафтиламіну. Їх фільтрують, промивають 3 мл холодного етанолу. Висушують на повітрі.
Вихід близько 2.5 г.
Якісна реакція:
1. При внесенні сульфанілової кислоти та краплі розчину нітриту натрію в підкислений оцтовою кислотою водний розчин 1‑нафтиламіну виникає рожеве забарвлення.
2. При нагріванні 1‑нафтиламіну, підкисленого хлоридної кислотою, з трихлоридом заліза виділяються синьо-зелені пластівці.
Допуск до роботи: техніка безпеки, схема реакції, розрахунки кількостей речовин, записи у журналі, хід виконання роботи.
Здача роботи: зовнішній вигляд, вихід продукту. Якісні реакції (на аміногрупу, на хлорид-аніон), за допомогою яких можна ідентифікувати отриману речовину. Методи відновлення нітрогрупи. Залежність результату відновлення від середовища.
3-Нітробензальдегід
3-Нітробензальдегід отримують нітруванням бензальдегіду в системі нітрат калію–концентрована сульфатна кислота.

Реактиви:
1. Бензальдегід (5 г, 1.06 г/мл).
2. Нітрат калію (5.5 г).
3. Сульфатна кислота концентрована (20 мл, 1.8 г/мл).
4. Хлорид натрію.
У товстостінному стакані місткістю 100 мл розчиняють при кімнатній температурі 5.5 г нітрату калію у 20 мл сульфатної кислоти. Стакан охолоджують сумішшю льоду з сіллю та при температурі у межах 0–5ºС та при перемішуванні (найкраще використовувати механічну мішалку) з крапельної лійки повільно доливають 5 г бензальдегіду. Після додавання бензальдегіду суміш перемішують додатково 1.5 години, після чого густу оранжеву масу виливають у стакан місткістю 200 мл, що містить 10 г товченого льоду. Осад, що утворився, фільтрують на воронці Бюхнера, промивають 10 мл 5%‑го розчину карбонату натрію, водою до нейтральної реакції, віджимають та сушать у вакуум-ексикаторі.
Вихід близько 5.9 г (83%), т. пл. 58–60ºС. При необхідності 3‑нітробензальдегід можна кристалізувати з бензолу чи лігроїну.
Якісна реакція:
1 мл концентрованого розчину продукту реакції в етанолі змішують з 1 мл розчину 2,4‑динітрофенілгідразину у суміші сульфатна кислота–етанол (1:1). Утворюється забарвлений малорозчинний осад 2,4‑динітрофенілгідразону 3‑нітробензальдегіду.
Допуск до роботи: техніка безпеки, схема реакції, розрахунки кількостей речовин, записи у журналі, хід виконання роботи.
Здача роботи: зовнішній вигляд, вихід та т. пл. продукту. Механізм реакції нітрування та якісної реакції на альдегідну групу. Методи отримання ароматичних альдегідів.
2,4,6-Трибромфенол
2,4,6-Трибромфенол отримують бромуванням фенолу у воді.

Реактиви:
1. Фенол (2.5 г).
2. Бром (13.3 г, 3.1 г/мл).
3. Етанол 50%‑ний (100 мл).
У стакані місткістю 1000 мл розчиняють 2.5 г фенолу в 150 г води. Окремо (в іншому стакані) готують концентрований водний розчин 13.3 г брому у воді та переносять його до крапельної лійки. До розчину фенолу при перемішуванні паличкою додають з крапельної лійки розчин брому, поки рідина у стакані не набуде жовтого забарвлення. що не зникає. Осад у вигляді білих пластівців фільтрують, висушують та після цього кристалізують з 50%‑ного етанолу.
Вихід 8.6 г (96%), т. пл. 95–6ºС.
Допуск до роботи: техніка безпеки, схема реакції, розрахунки кількостей речовин, записи у журналі, хід виконання роботи.
Здача роботи: зовнішній вигляд, вихід та т. пл. продукту. Механізм реакції радикального заміщення в ароматичному кільці. Методи отримання ароматичних галогенпохідних.
