
- •Тема: предмет и задачи иммунологии. Структура и функции иммунной системы
- •III. Уметь практически:
- •V. План изучения темы: теоретическая часть занятия:
- •Практическая часть изучения темы:
- •Рекомендуемая литература по теме занятия:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение:
- •Тема: антигены и антитела
- •IV. План изучения темы: теоретическая часть занятия:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение:
- •Тема: т-лимфоциты: основные этапы развития, субпопуляции, рецепторы и маркеры, современные методы идентификации
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение:
- •Тема: в-лимфоциты: основные этапы развития. Строение, функции. Современные методы идентификации
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение:
- •Тема: антигенпредставляющие и фагоцитирующие клетки
- •III. Уметь практически:
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение
- •Тема: гормоны и медиаторы иммунной системы. Их роль в иммунном ответе
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Приложение
- •Тема: иммунный ответ
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Обязательные для выполнения задания:
- •Тема: цитотоксические реакции иммунитета
- •V. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Обязательные для выполнения задания:
- •Тема: система hla и иммунологическая реактивность
- •IV. План изучения темы: теоретическая часть изучения темы:
- •Практическая часть изучения темы:
- •Вопросы для самоконтроля:
- •Приложение
- •Литература
- •Методика выделения лимфоцитов периферической крови в градиенте плотности фиколл-верографин
- •Практическое применение ифа.
- •Реакция торможения миграции лейкоцитов
- •Методика исследования.
- •Реакция бласттрансформации лимфоцитов
- •Функциональное состояние системы фагоцитирующих клеток. Фагоцитарная активность нейтрофилов
- •Методика определения фагоцитарной активности нейтрофилов.
- •Методика исследования.
- •Приготовление раствора:
- •Полимеразная цепная реакция (пцр)
- •Литература
Полимеразная цепная реакция (пцр)
образом Принцип метода полимеразной цепной реакции (ПЦР) (Polymerase chain reaction, PCR) был разработан сотрудником фирмы "Cetus"(США) Кэри Мюллисом в 1983 г., и в настоящее время широко используется как для научных иследований, так и для диагностики в практическом здравохранении и службе санэпиднадзора ( генотипирование, диагностика инфекционных заболеваний).
Основы метода ПЦР
В основе метода ПЦР лежит природный процесс - комплементарное достраивание ДНК матрицы, осуществляемое с помощью фермента ДНК-полимеразы. Эта реакция носит название репликации ДНК.
Естественная репликация ДНК включает в себя несколько стадий:
1) Денатурация ДНК (расплетение двойной спирали, расхождение нитей ДНК);
2) Образование коротких двухцепочечных участков ДНК (затравок, необходимых для инициации синтеза ДНК);
3) Синтез новой цепи ДНК (комплементарное достраивание обеих нитей)
Данный процесс можно использовать для получения копий коротких участков ДНК, специфичных для конкретных микроорганизмов, т.е. осуществлять целенаправленный поиск таких специфических участков, что и является целью генодиагностики для выявления возбудителей инфекционных заболеваний.
Открытие термостабильной ДНК-полимеразы (Taq-полимеразы) из термофильных бактерий Thermis aquaticus , оптимум работы которой находится в области 70-72оС, позволило сделать процесс репликации ДНК циклическим и использовать его для работы in vitro. Создание программируемых термостатов (амплификаторов), которые по заданной программе осуществляют циклическую смену температур, создало предпосылки для широкого внедрения метода ПЦР в практику лабораторной клинической диагностики. При многократном повторении циклов синтеза происходит экспоненциальное увеличение числа копий специфического фрагмента ДНК, что позволяет из небольшого количества анализируемого материала, который может содержать единичные клетки микроорганизмов получить достаточное количество ДНК копий для идентификации их методом электрофореза.
Комплементарное достраивание цепи начинается не в любой точке последовательности ДНК, а только в определеннных стартовых блоках- коротких двунитевых участках. При присоединении таких блоков к специфическим участкам ДНК можно направить процесс синтеза новой цепи только в этом участке, а не по всей длине ДНК цепи. Для создания стартовых блоков в заданных участках ДНК используют две олигонуклеотидные затравки (20 нуклеотидных пар), называемые праймерами. Праймеры комплементарны последовательностям ДНК на левой и правой границах специфического фрагмента и ориентированы таким образом, что достраивание новой цепи ДНК протекает только между ними.
Таким, ПЦР представляет собой многократное увеличение числа копий (амплификация) специфического участка ДНК катализируемое ферментом ДНК- полимеразой.
Для проведения амплификации необходимы следующие компоненты:
ДНК-матрица (ДНК или ее часть, содержащая искомый специфический фрагмент); Праймеры (синтетические олигонкулеотиды (20-30 нуклеотидных пар), комплементарные последовательностям ДНК на границах определяемого специфического фрагмента). Выбор специфического фрагмента и подбор праймеров играет важнейшую роль в специфичности проведения амплификации, что сказывается на качестве проведения анализа. Смесь дезоксинуклеотидтрифосфатов (дНТФ) (смесь четырех дНТФ, являющихся материалом для синтеза новых комплементарных цепей ДНК) Фермент Taq-полимераза (термостабильная ДНК-полимераза, катализирующая удлиннение цепей праймеров путем последовательного присоединения нуклеотидных оснований к растущей цепи синтезируемой ДНК) Буферный раствор (реакционная среда, содержащая ионы Mg2+, необходимые для поддержания активности фермента)
Р ис.
25. Схема ПЦР
ис.
25. Схема ПЦР
Для определения специфических участков генома РНК-содержащих вирусов, сначала получают ДНК-копию с РНК-матрицы, используя реакцию обратной транскрипции (RT), катализируемую ферментом ревертазой (обратной транскриптазой).
Для получения достаточного количества копий искомого характеристического фрагмента ДНК амплификация включает несколько (20-40) циклов.
Каждый цикл амплификации включает 3 этапа, протекающих в различных температурных режимах
1 этап: Денатурация ДНК (расплетение двойной спирали). Протекает при 93-95ов течение 30-40 сек.
2 этап: Присоединение праймеров (отжиг). Присоединение праймеров происходит комплементарно к соответствующим последовательностям на противоположных цепях ДНК на границах специфического участка. Для каждой пары праймеров существет своя температура отжига, значения которой располагаются в интервале 50-65оС. Время отжига -20-60 сек.
3 этап: Достраивание цепей ДНК. Комплементарное достраивание цепей ДНК происходит от 5’-конца к 3’-концу цепи в противоположных направлениях, начиная с участков присоединения праймеров. Материалом для синтеза новых цепей ДНК служат добавляемые в раствор дезоксирибонуклеотидтрифосфаты (дНТФ). Процесс синтеза катализируется ферментом термостабильной ДНК-полимеразой (Taq-полимеразой) и проходит при температуре 70-72оС. Время протекания синтеза - 20-40 сек.
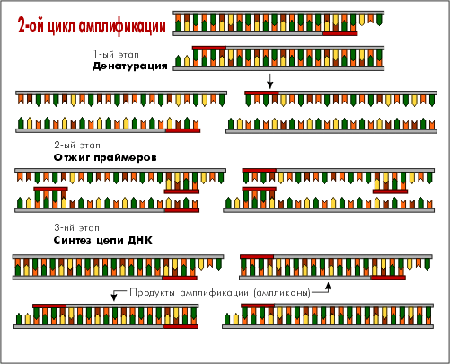
 Рис.
26. Схема ПЦР (продолжение).
Рис.
26. Схема ПЦР (продолжение).
Образовавшиеся в первом цикле амплификации новые цепи ДНК служат матрицами для второго цикла амплификации, в котором происходит образование искомого специфического фрагмента ДНК (ампликона). В последующих циклах амплификации ампликоны служат матрицей для синтеза новых цепей. Таким образом происходит накопление ампликонов в растворе по формуле 2n, где n-число циклов амлификации . Поэтому, даже если в исходном растворе первоначально находилась только одна двухцепочечная молекула ДНК, то за 30-40 циклов в растворе накапливается около 108 молекул ампликона. Этого количества достаточно для достоверной визуальной детекции этого фрагмента методом электрофореза в агарозном геле. Процесс амплификации проводится в специальном программируемом термостате (амплификаторе), который по заданной программе автоматически осуществляет смену температур согласно числу циклов амплификации.
Метод ПЦР в лабораторной диагностике
В основе метода ПЦР, как инструмента лабораторной диагностики инфекционных заболеваний лежит обнаружение небольшого фрагмента ДНК возбудителя (несколько сот пар оснований), специфичного только для данного микроорганизма, с использованием полимеразной цепной реакции для накопления искомого фрагмента. Методика проведения анализа с использованием метода ПЦР включает три этапа:
Рис. 27. Схема ПЦР (продолжение).
1. Выделение ДНК (РНК) из клинического образца
2. Амплификация специфических фрагментов ДНК
3. Детекция продуктов амплификации
Выделение ДНК (РНК)
На данной стадии проведения анализа клиническая проба подвергается специальной обработке, в результате которой происходит лизис клеточного материала, удаление белковых и полисахаридных фракций, и получение раствора ДНК или РНК, свободной от ингибиторов и готовой для дальнейшей амплификации.
Выбор методики выделения ДНК(РНК) в основном определяется характером обрабатываемого клинического материала.
Амплификация специфических фрагментов ДНК На данной стадии происходит накопление коротких специфических фрагментов ДНК в количестве, необходимом для их дальнейшей детекции. В большинстве методик определения специфических фрагментов генома используется т.н. “классический вариант направленной ПЦР. Для повышения специфичности и чувствительности анализа в некоторых методиках используется метод “гнездной” (nested) ПЦР, в котором используются 2 пары праймеров (“внешние” - для 1 стадии, и “внутренние” - для 2-ой стадии).
Детекция продуктов амплификации В большинстве методик на данном этапе проводится разделение смеси продуктов амплификации, полученной на 2-ой стадии, методом горизонтального электрофореза в агарозном геле. До проведения электрофоретического разделения, к амплификационной смеси добавляется раствор бромистого этидия, образущий с двухцепочечными фрагментами ДНК прочные соединения внедрения. Эти соединения под действием УФ-облучения способны флуоресцировать, что регистрируется в виде оранжево-красных светящихся полос после электрофоретического разделения амплификационной смеси в агарозном геле. В качестве альтернативы электрофоретическому методу детекции, имеющему некоторые недостатки: субъективность чтения результатов, ограничения по определению ДНК различных микроорганизмов в одной реакции, могут быть предложены гибридизационные схемы детекции. В этих схемах образующийся в результате амплификации фрагмент ДНК гибридизуется (образует 2-х цепочечные комплексы - "гибриды") со специфическим олигонуклеотидным зондом.
Преимущества метода ПЦР
Преимущества метода ПЦР как метода диагностики инфекционных заболеваний
Прямое определение наличия возбудителей Многие традиционные методы диагностики, например иммуноферментный анализ, выявляют белки-маркеры, являющиеся прдуктами жизнедеятельности инфекционных агентов, что дает лишь опосредованное свидетельство наличия инфекции. Выявление специфического участка ДНК возбудителя методом ПЦР дает прямое указание на присутствие возбудителя инфекции.
Высокая специфичность Высокая специфичность метода ПЦР обусловлена тем, что в исследуемом материале выявляется уникальный, характерный только для данного возбудителя фрагмент ДНК. Специфичность задается нуклеотидной последовательностью праймеров, что исключает возможность получения ложных результатов, в отличие от метода иммуноферментного анализа, где нередки ошибки в связи с перекрестно-реагирующими антигенами.
Высокая чувствительность Метод ПЦР позволяет выявлять даже единичные клетки бактерий или вирусов. ПЦР-диагностика обнаруживает наличие возбудителей инфекционных заболеваний в тех случаях, когда другими методами (иммунологическими, бактериологическими, микроскопическими) это сделать невозможно. Чувствительность ПЦР-анализа составляет 10-1000 клеток в пробе (чувствительность иммунологических и микроскопических тестов - 103-105 клеток).
Универсальность процедуры выявления различных возбудителей Материалом для исследования методом ПЦР служит ДНК возбудителя. Метод основан на выявлении фрагмента ДНК или РНК, являющегося специфичным для конкретного организма. Сходство химического состава всех нуклеиновых кислот позволяет применять унифицированные методы проведения лабораторных исследований. Это дает возможность диагносцировать несколько возбудителей из одной биопробы. В качестве исследуемого материала могут использоваться различные биологические выделения (слизь, моча, мокрота), соскобы эпителиальных клеток, кровь, сыворотка.
Высокая скорость получения результата анализа Для проведения ПЦР-анализа не требуется выделение и выращивание культуры возбудителя, что занимает большое количество времени. Унифицированный метод обработки биоматериала и детекции продуктов реакции, и автоматизация процесса амплификации дают возможность провести полный анализ за 4-4.5 часа.
Возможность диагностики не только острых, но и латентных инфекций Особенно эффективен метод ПЦР для диагностики трудно культивируемых, некультивируемых и персистирующих форм микроорганизмов, с которыми часто приходится сталкиваться при латентных и хронических инфекциях, поскольку этот метод позволяет избежать сложностей, связанных с выращиванием таких микроорганизмов в лабораторных условиях. Применение ПЦР-диагностики также очень эффективно в отношении возбудителей с высокой антигенной изменчивостью и внутриклеточных паразитов.
Следует отметить, что методом ПЦР возможно выявление возбудителей не только в клиническом материале, полученном от больного, но и в материале, получаемом из объектов внешней среды (вода, почва и т.д.) Применение метода ПЦР в практическом здравохранении
Использование метода ПЦР для диагностики инфекционных заболевании как бактериальной, так и вирусной природы имеет колоссальное значение для решения многих проблем микробиологии и эпидемиологии.
Применение этого метода также способствует развитию фундаментальных исследований в области изучения хронических и малоизученных инфекционных заболеваний.
Однако следует отметить, что метод ПЦР лишь дополняет спектр традиционных методов, используемых в микробиологической диагностике.
Наиболее рационально и эффективно применение ПЦР для обнаружения микроорганизмов трудно культивируемых в лабораторных условиях, атипичных форм бактерий. К ним также относятся внутриклеточные паразиты и микроорганизмы, способные длительно персистировать в организме хозяина. Высокоспецифичная, чувствительная и быстрая диагностика многих тяжелых заболеваний способствует не только их эффективному лечению, но и предотвращению распространения инфекции.
Наиболее эффективно и экономически обоснованно использование метода в урогинекологической практике - для выявления хламидиоза, уреаплазмоза, гонореи, герпеса, гарднереллеза, микоплазменной инфекции; в пульмонологии - для дифференциальной диагностики вирусных и бактериальных пневмоний, туберкулеза; в гастроэнтерологии - для выявления геликобактериоза ; в клинике инфекционных заболеваний - в качестве экспресс-метода диагностики сальмонеллеза, дифтерии, вирусных гепатитов В,С и G; В гематологии - для выявления цитомегаловирусной инфекции, онковирусов.
Н екоторые
аспекты применения ПЦР в различных
областях медицинской практики
рассматриваются в предлагаемых пособиях
для врачей (см. Методические
рекомендации)
екоторые
аспекты применения ПЦР в различных
областях медицинской практики
рассматриваются в предлагаемых пособиях
для врачей (см. Методические
рекомендации)
Рис.28. М: маркеры; 1: ПЦР-продукт, полученный с использованием dNTPs производства "Лаборатории Медиген"; 2-3: ПЦР-продукт, полученный с использованием dNTPs других коммерческих источников.
МЕТОДИЧЕСКИЕ РЕКОМЕНДАЦИИ ПО ПРОВЕДЕНИЮ РАБОТ В ДИАГНОСТИЧЕСКИХ ЛАБОРАТОРИЯХ, ИСПОЛЬЗУЮЩИХ МЕТОД ПОЛИМЕРАЗНОЙ ЦЕПНОЙ РЕАКЦИИ.
(Государственный комитет санитарно-эпидемиологического надзора российской федерации москва, 1995 г. )
ОСНОВНЫЕ ПОЛОЖЕНИЯ
1. Область применения |
Данный документ предназначен для учреждений здравоохранения и санэпиднадзора, использующих метод полимеразной цепной реакции в целях диагностики инфекционных заболеваний.
2. Обоснование необходимости |
Благодаря высокой специфичности и чувствительности метод полимеразной цепной реакции (ПЦР) находит широкое применение в диагностике возбудителей инфекционных заболеваний. Однако ПЦР-диагностика инфекций связана с проблемой, обусловленной высокой чувствительностью метода, - возможностью контаминации.
Попадание в реакционную пробирку следовых количеств положительной ДНК (специфических продуктов амплификации ДНК - ампликонов; ДНК-стандарта, используемой в качестве положительного контроля; положительной ДНК клинического образца) приводит к амплификации в процессе ПЦР специфического фрагмента ДНК и, как следствие, к появлению ложно-положительных результатов.
Сотрудник, занимающийся ПЦР-диагностикой, в своей работе сталкивается с двумя видами контаминации:
1. перекрестная контаминация от пробы к пробе ( в процессе обработки клинических образцов или при раскапывании реакционной смеси), приводящая к появлению спорадических ложно-положительных результатов;
2. контаминация продуктами амплификации (ампликонами), имеющая наибольшее значение, поскольку в процессе ПЦР ампликоны накапливаются в огромных количествах и являются идеальными продуктами для реамплификации.
Контаминация следовыми количествами ампликонов посуды, автоматических пипеток и лабораторного оборудования, поверхностей лабораторных столов или даже поверхности кожи сотрудников лаборатории приводит к появлению систематических ложно-положительных результатов.
Как правило, определить источник контаминации бывает очень трудно и требует значительных затрат времени и средств.
Накопленный к настоящему времени опыт работы лабораторий, использующих полимеразную цепную реакцию для диагностики инфекций (ПЦР-диагностические лаборатории) позволяет сформулировать основные требования к планировке таких подразделений и проведению самих анализов. Соблюдение данных требований обеспечиванет исключение возможности контаминации и получения ложно-положительных результатов.
3. Планировка помещений и основные принципы организации работы ПЦР-диагностических лабораторий |
1). Лаборатория должна быть разделена на зоны (комнаты) для каждой из стадий ПЦР-диагностики. Следует иметь не менее двух комнат:
- пре-ПЦР-помещение, где проводится обработка клинических образцов, выделение ДНК, приготовление реакционной смеси для ПЦР и постановка ПЦР (при наличии условий два последних этапа рекомендуется также проводить в дополнительном отдельном помещении); в этих помещениях запрещается проводить все другие виды работ с инфекционными агантами (микробиологический анализ, ИФА, другие диагностические тесты и т.д.), ПЦР-диагностика которых проводится в данной лаборатории.
- пост-ПЦР-помещение, где проводится детекция продуктов амплифиации; в пост-ПЦР-помещении допускается использовать другие методы детекции инфекций, диагностика которых проводится в данной лаборатории.
2). Комнату детекции продуктов амплификации (пост-ПЦР-помещение) следует расположить как можно дальше от пре-ПЦР-помещений.
3). Следует исключить движение воздушного потока из пост-ПЦР в пре-ПЦР-помещения.
4). В комнате приготовления реакционной смеси и в комнате обработки клинических образцов должны быть установлены настольные боксы с ультрафиолетовыми лампами.
5). Работа в лаборатории должна быть организована в одном направлении: от пре-ПЦР-помещений к пост-ПЦР-помещению.
6). Каждое помещение ПЦР-диагностической лаборатории должно иметь свой набор реагентов, автоматических пипеток, наконечников, пластиковой и стеклянной посуды, лаборатоного оборудования, халатов и перчаток, используемых только в данном помещении и не выносящихся в другие ПЦР-помещения. Оборудование, материалы и инвентарь в каждой комнате должны иметь соответствующую маркировку.
7). Обработка рабочей одежды из пре- и пост-ПЦР-помещений должна производиться раздельно.
8). Следует однократно использовать перчатки как в комнате обработки клинических образцов, так и в комнате приготовления реакционной смеси и постановки ПЦР.
9). Необходимо однократно использовать пробирки и наконечники для автоматических пипеток. Обязательно менять наконечники при переходе от одной пробы к другой с целью предотвращения перекрестной контаминации в процессе выделения ДНК или при раскапывании реакционной смеси.
10). Необходимо использовать наконечники для автоматических пипеток с аэрозольным барьером (или наконечники с ватными фильтрами, приготовленными в помещении, в котором не ведутся работы с ДНК) при обработке клинических образцов, а также при внесении выделенной ДНК в реакционную пробирку.
11). Каждый сотрудник лаборатории должен иметь персональный набор автоматических пипеток и реагентов.
12). В пре-ПЦР и пост-ПЦР-помещениях лаборатории должны работать разные сотрудники.
13). Клинические образцы должны храниться отдельно от реагентов.
14). Не следует использовать водяные бани, т.к. заполняющая их вода, просачиваясь в недостаточно плотно закрытые пробирки, может стать источником контаминации; следует использовать суховоздушные термостаты.
15). При исследовании материала зараженного или подозрительного на зараженность возбудителями инфекционных заболеваний I-IV групп работа должна проводиться с соблюдением “Санитарных правил СП 1.2.011-94 (Безопасность работы с микроорганизмами I-II групп патогенности)” и “Положения о порядке учета, хранения, обращения, отпуска и пересылки культур бактерий, вирусов, рикетсий, грибов, простейших, микоплазм, бактерийных токсинов, ядов биологического происхождения”, М., 1980.
16). Необходимо постоянно поддерживать чистоту на рабочем месте:
- каждое помещение должно иметь свой отдельный набор инвентаря для обработки и уборки рабочего места (ватно-марлевые тампоны, пинцет, 70о этанол, дезинфицирующий раствор и т.д.), и источники ультрафиолетового излучения, которые эффективно инактивируют ДНК-матрицы.
- при манипуляциях с клиническим материалом рабочую поверхность до и после исследования обрабатывают дезинфицирующим раствором (указанным для данного возбудителя) и затем 70о этанолом.
- следует обрабатывать рабочую поверхность в комнате приготовления реакционной смеси до работы 70о этанолом с целью борьбы с пылью.
17). Следует полностью исключить проведение в ПЦР-диагностической лаборатории работ, связанных с получением (клонированием) и выделением рекомбинантных плазмид, содержащих последовательности ДНК или фрагментов генов возбудителей, которые диагносцируются в данной лаборатории.
18). Персонал, работающий в ПЦР-диагностической лаборатории должен пройти соответствующее обучение.
4. Требования к проведению ПЦР-анализа |
4.1. Обработка клинических образцов.
1). Забор клинических образцов необходимо производить только в одноразовые пластиковые пробирки или в стеклянные пробирки, предварительно обработанные в течение 1 часа хромовой смесью, тщательно промытые дистиллированной водой и прокаленные.
2). Работать только в одноразовых перчатках.
3) необходимо использовать одноразовые наконечники для автоматических пипеток с аэрозольным барьером.
4). Обязательно менять наконечники при переходе от одной пробы к другой.
5). Использованные пробирки и наконечники должны сбрасываться в одноразовые контейнеры или в специальную емкость с 1Н. раствором соляной кислоты.
4.2. Постановка ПЦР.
1). Работать только в одноразовых перчатках.
2). Следует готовить смесь реактивов для ПЦР, расчитанную на все пробы, включая контрольные, и затем - раскапывать ее по пробиркам.
3). Использовать автоматические пипетки с переменным объемом и оноразовые наконечники.
4). В каждый момент работать только с одной пробиркой.
5) Во всех случаях постановки ПЦР следует обязательно применять отрицательные и положительные контроли в соответствии с инструкцией по применению диагностических наборов.
6). Подготовленные к ПЦР исследуемые образцы должны добавляться в реакционные смеси одноразовыми наконечниками с аэрозольным барьером в последнюю очередь. Использованные наконечники следует сбрасывать в емкость с 1Н. раствором HCl.
4.3. Детекция продуктов амплификации.
1). Анализ продуктов ПЦР должен производиться в изолированной комнате сотрудником лаборатории, не производящим обработки клинических образцов и операций с реакционной смесью.
2). Работать следует только в одноразовых перчатках.
3). Оборудование, реактивы, халаты, перчатки, а также уборочный инвентарь, используемые в комнате детекции продуктов амплификации (пост-ПЦР-помещение), должны храниться только в этой комнате и не должны попадать в пре-ПЦР-помещения.
4). В комнате детекции продуктов амплификации необходимо работать в сменной обуви.
5. Использование физических и химических методов борьбы с контаминацией |
1). Рабочие поверхности, оборудование и материалы следует облучать ультрафиолетом с максимумом излучения в области 260 нм. Облучение необходимо проводить в течение 1 часа до начала работы и в течение 1 часа после окончания работы.
2). Использованные наконечники для автоматических пипеток, пробирки и другие загрязненные ДНК материалы необходимо обрабатывать реагентами, вызывающими деградацию ДНК (1 Н HCl, 10% гипохлоритом натрия или 10% хлорной известью).
6. Оценка качества работы ПЦР-диагностической лаборатории |
1). Для оценки качества работы ПЦР-диагностической лаборатории следует периодически применять зашифрованные внутрилабораторные контрольные положительные и отрицательные образцы, охарактеризованные не только с помощью полимеразной цепной реакции, но и другими методами диагностики данной инфекции.
2). Следует периодически проводить оценку чувствительности диагностических наборов на основе полимеразной цепной реакции.
