
- •Закон Больцмана о равномерном распределении энергии по степеням свободы
- •Внутренняя энергия термодинамической системы
- •Работа и теплота
- •Первое начало термодинамики
- •Работа газа при изменении его объема
- •Графическое изображение работы
- •Теплоемкость
- •Молярные теплоемкости при постоянных объеме и давлении
- •Уравнение Майера
- •Температурная зависимость молярных теплоемкостей
- •Применение первого начала термодинамики к изопроцессам
- •Адиабатный процесс
- •Политропный процесс
- •Круговой процесс (цикл) Обратимые и необратимые процессы
- •Коэффициент полезного действия для кругового процесса
- •Энтропия
- •Неравенство Клаузиуса
- •Изменение энтропии в изотермическом и изохорном процессах
- •Второе начало термодинамики
- •Третье начало термодинамики
- •Тепловой двигатель. Теорема Карно
- •Принцип работы теплового двигателя
- •Термический кпд цикла Карно
Адиабатный процесс
Адиабатным
называется процесс, при котором
отсутствует теплообмен между системой
и окружающей средой:
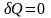 .
.
К адиабатным процессам можно отнести все быстропротекающие процессы. Например, сжатие и расширение воздуха в звуковой волне, расширение и сжатие горючей смеси в цилиндрах двигателей внутреннего сгорания.
Из перого начала термодинамики для адиабатного процесса следует, что
 ,
(43)
,
(43)
т.е. в случае адиабатного процесса работа совершается за счет убыли внутренней энергии системы.
Используя выражения (27) и (33) для произвольной массы газа запишем уравнение (43) в виде:
 .
(44)
.
(44)
Продифференцировав уравнение состояния идеального газа , получим
 .
(45)
.
(45)
Разделив
выражение (45) на (44) и учтем, что
 ,
найдем
,
найдем
 .
.
Интегрируя это уравнение в пределах от p1 до p2 и соответственно от V1 до V2, а затем потенцируя, получим
 или
или
 .
.
Так как состояния 1 и 2 выбраны произвольно, то
 . (46)
. (46)
Выражение (46) - уравнение Пуассона (уравнение газового состояния при адиабатном процессе).
Показатель адиабаты (показатель Пуассона):
 .
(47)
.
(47)
График зависимости между параметрами состояния идеального газа при называется адиабатой.
В
а)p
адиабатном ( ) и изотермическом (pV = const ) процессах наблюдаются существенные различия в характере изменения давления при расширении (рис.10 а) и сжатии (рис.10. б).Рисунок 10 – Графики адиабатного и изотермического процессов
Поскольку γ > 1, адиабата идет круче, чем изотерма. Это объясняется тем, что при адиабатном сжатии газ нагревается (увеличение р обусловлено не только уменьшением V (как при изотермическом процессе), но и повышением температуры). При адиабатном расширении газ охлаждается (уменьшение р обусловлено не только увеличением V (как при изотермическом процессе), но и уменьшением температуры).
Политропный процесс
Если в течение всего процесса теплоемкость газа неизменна, то такой процесс называют политропным. Для идеального газа уравнение политропного процесса имеет вид:
 (48)
(48)
где n - показатель политропы (любое действительное число).
Показатель политропы:
 . (49)
. (49)
При
С=0,
 из (48) получаем уравнение адиабаты.
из (48) получаем уравнение адиабаты.
При С=, n=1 – получаем уравнение изотермы.
При С=Сp, n=0 – получаем уравнение изобары.
При С=СV, n= - получаем уравнение изохоры.
Таким образом, все рассмотренные процессы являются частными случаями политропного процесса.
Круговой процесс (цикл) Обратимые и необратимые процессы
Термодинамический процесс называется обратимым, если он может происходить как в прямом так и в обратном направлении, причем если такой процесс происходит сначала в прямом, а затем в обратном направлении и система возвращается в исходное состояние, то в окружающей среде и в этой системе не происходит никаких изменений. Всякий процесс, не удовлетворяющий этим условиям будет необратимым. Все реальные процессы необратимы, поскольку сопровождаются диссипацией энергии (из-за трения, теплопроводности и т. д.).
Любой обратимый процесс является равновесным.
Обратимые процессы — это идеализация реальных процессов. Их рассмотрение существенно по двум причинам: 1) многие процессы в природе и технике практически обратимы; 2) обратимые процессы являются наиболее экономичными; имеют максимальный термический коэффициент полезного действия, что позволяет указать пути повышения КПД реальных тепловых двигателей.
Круговой процесс - процесс, при котором система, пройдя через ряд состояний, возвращается в исходное состояние.
 На
диаграмме p
– V
равновесный круговой процесс изображается
замкнутой
кривой (см.рис.11).
На
диаграмме p
– V
равновесный круговой процесс изображается
замкнутой
кривой (см.рис.11).
Рисунок 11 – Круговой процесс
Прямой цикл - цикл, за который совершается положительная работа (цикл протекает по часовой стрелке) (см.рис.1):
 >0.
>0.
Работа расширения (процесс 1а2), определяемая площадью фигуры 1a2V2Vl1, положительна (dV> 0). Работа сжатия (процесс 2B1), определяемая площадью фигуры 2b1V1V22, отрицательна (dV < 0). Работа, совершаемая газом за цикл, определяется площадью, охватываемой замкнутой кривой.
Прямой цикл используется в тепловых двигателях — периодически действующих двигателях, совершающих работу за счет полученной извне теплоты.
Обратный цикл - цикл, за который совершается отрицательная работа
(цикл протекает против часовой стрелки):
 <0.
<0.
Рисунок 12 – Обратный круговой процесс
Работа расширения (процесс 1а2), определяемая площадью фигуры 1a2V2V11, положительна (dV>0). Работа сжатия (процесс 2B1), определяемая площадью фигуры 2b1V1V22, отрицательна (dV< 0). Работа за цикл определяется площадью, охватываемой замкнутой кривой.
Обратный цикл используется в холодильных машинах — периодически действующих установках, в которых за счет работы внешних сил теплота переносится к телам с более высокой температурой.
