
Методы определения чисел переноса.
Для определения чисел переноса используют три метода.
По методу Гитторфа определяют аналитическим путем изменение количества электролита в анодном или катодном пространстве электрохимической системы при прохождении через нее постоянного тока и рассчитывают числа переноса по формуле
![]() (10)
(10)
где n — изменение содержания электролита; определяемое аналитически вблизи каждого из электродов, г-экв; F— число Фарадея, Кл моль-1; Q — общее количество электричества, пропущенное через электрохимическую систему и определяемое кулонометрически.
В настоящее время применяют кулонометры — системы, в которых весь ток расходуется лишь на одну электрохимическую реакцию — трех типов: весовые — серебряные и медные; объемные — водородные и ртутные; титрационные — чаще других используют анодное растворение серебра (кулонометр В. А. Кистяковского) или электролитическое окисление ионов иода.
Найденные по формуле (10) числа переноса не учитывают гидратацию ионов и перенос молекул растворителя через мембраны, разделяющие приэлектродные пространства при электролизе, поэтому они называются эффективными, или кажущимися. При выборе в качестве системы отсчета растворителя в целом расчет чисел переноса (особенно для концентрированных растворов) следует проводить по уравнению
![]() (11)
(11)
где![]() и
и
![]() — начальное и конечное содержания
электролита в катодном пространстве,
— начальное и конечное содержания
электролита в катодном пространстве,
г-экв;
![]() и
и
![]() —
начальная и конечная
концентрации воды там же.
—
начальная и конечная
концентрации воды там же.
По методу движущейся границы определяют расстояние l, на которое перемещается граница между двумя окрашенными или разной плотности растворами с одним общим ионом в узкой вертикальной трубке сечением s под действием постоянной разности потенциалов за определенный промежуток времени при выполнении условий:
1) регулирующего соотношения Кольрауша (с точностью до 10%):
![]() (12)
(12)
где t /tинд - числа переноса в исследуемом и индикаторном растворах; С, Синд — соответствующие концентрации;
2) число переноса индикаторного раствора
меньше исследуемого, т.е.![]() ;
;
3) индикаторный раствор имеет большую, чем исследуемый, плотность и располагается в нижнем слое — сохраняется резкая граница между растворами при электролизе.
Число переноса в этом методе рассчитывают по формуле
![]() (13)
(13)
где С — концентрация исследуемого раствора; z+ — заряд иона; С+ — концентрация иона; V = ls — объем раствора, прошедшего по трубке за время . Видно, что формула (13) идентична (10). Отметим, что при выборе в качестве системы отсчета растворителя в соотношение (13) нужно ввести поправку на изменение объема V, связанное с перемещением по трубке из-за электродных реакций воды:
![]() (14)
(14)
Также различают метод определения чисел переноса ионов, связанный с измерением диффузионного потенциала в концентрационных цепях с переносом.
В растворе перенос электричества осуществляется ионами, причем каждый вид ионов переносит определенное количество электричества в зависимости от содержания данных ионов в растворе, их валентности и скорости движения в электрическом поле.
Общее количество электричества е, прошедшего через раствор, складывается из количества электричества, перенесенного всеми ионами:
![]() (15)
(15)
Доля количества электричества, перенесенного ионами i, называется числом переноса ti:
![]() (16)
(16)
Для раствора электролита АВ, диссоциирующего по схеме
АВА++В-
числа переноса могут быть выражены равенствами:
![]() и
и
![]() (17)
(17)
где ек и еа – количество электричества, перенесенное катионами А+ и анионами В- соответственно.
Отсюда
![]()
Поскольку количество электричества, перенесенное ионами данного вида, пропорционально скорости их движения, то числа переноса можно определить через абсолютные скорости ионов:
![]() (18)
(18)
Или, учитывая, что = uF , через подвижности (электропроводности) ионов:
![]() (19)
(19)
Числа переноса зависят от подвижности всех ионов в растворе, природы растворителя, концентрации и температуры. Влияние изменения концентрации незначительно; при концентрации растворов ниже 0,2 н. числа переноса практически остаются постоянными. Благодаря этому можно легко определить значение ti при бесконечном разбавлении путем экстраполяции. Зная число переноса и эквивалентную электропроводность при бесконечном разбавлении, можно рассчитать подвижность ионов, решая уравнение:
![]() (20)
(20)
С увеличением температуры за счет неодинаковой степени дегидратации ионов А+ и В- числа переноса выравниваются и стремятся к 0,5.
Установка для определения чисел переноса.
Схема лабораторной установки для определения чисел переноса показана рис. 2
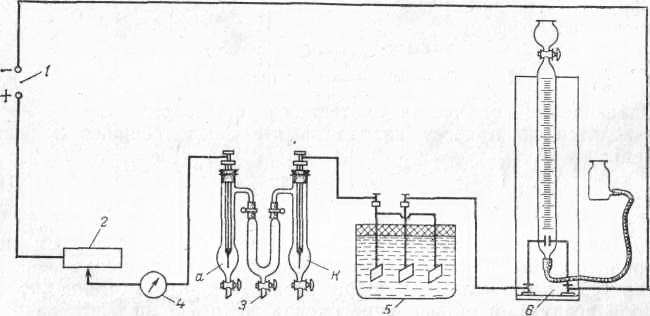
Рис. 2 Схема установки для определения чисел переноса ионов:
/—источник постоянного тока; 2 — реостат; 3 — электролизер для определения чисел переноса ионов (а — анодный сосуд; к – катодный сосуд); 4 — миллиамперметр; 5 — медный кулонометр; 6 — газовый кулонометр.
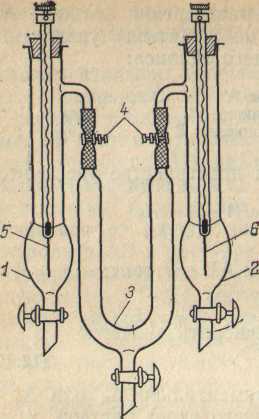
/ — анодный сосуд; 2 — катодный сосуд; 3 — соединительный сосуд; 4 — зажимы; 5, 6 — электроды.
Поскольку при измерении чисел переноса необходимо определять изменение содержания электролита у каждого электрода отдельно, то в электролизере 3 анодное и катодное пространство должны быть в достаточной степени разделены. Для этой цели удобно пользоваться прибором, изображенным на рис. 3.
Кулонометры. Количество протекающего через цепь электричества определяется с помощью кулонометров — приборов, основанных на электрохимическом принципе действия. Расчет количества электричества производится на основании законов электролиза Фарадея. Необходимым условием при этом является протекание на электроде одного единственного электрохимического процесса, отсутствие побочных химических реакций и механических потерь продукта, т. е. электродный процесс должен проходить с выходом по току 100%.
По методам определения количества образующихся веществ кулонометры подразделяются на весовые, объемные и титрационные.
Медный кулонометр (весовой) состоит из медных электродов — пластинок, погруженных в раствор CuSO4. На границе раздела «электрод — электролит» протекают процессы:
Сu2+
+ 2е -
![]() Сu (на катоде)
Сu (на катоде)
Сu — 2e- Сu2+ (на аноде)
Определение количества протекающего электричества eF производится по привесу катода за счет выделившейся на нем меди:
eF = m/31,77 (21)
где т — масса выделившейся меди, г; 31,77 — химический эквивалент меди.
Точность показаний кулонометра 0,1—0,5%- Основным источником погрешностей является частичное растворение медных электродов в кислом растворе, особенно в присутствии кислорода воздуха, и образование оксида меди (I) за счет реакции на катоде:
Си2+ + е- Cu+
в нейтральном растворе и при малых плотностях тока, а также осаждение меди на катоде в губчатой форме при высоких плотностях тока. Для повышения точности показаний кулонометра рекомендуется в качестве электролита использовать раствор следующего состава: CuSO4*5H2O - 150 г/л; H2SO4 - 50 г/л; С2Н5ОН - 50 г/л; вести электролиз при умеренных плотностях тока на катоде в пределах от 2 до 20 мА-см-2. В объемных кулонометрах количества выделяющихся на электродах веществ определяют измерением их объемов. Примером такого типа приборов является газовый кулонометр. Кулонометр состоит из градуированной бюретки, в нижний конец которой впаяны два платиновых электрода. Бюретку и уравнительную склянку заполняют 0,5 М раствором сульфата натрия.Для повышения точности показаний кулонометра рекомендуется перед каждым опытом насыщать раствор электролита водородом и кислородом. С этой целью собирают установку согласно рис.2, в которую включают только один газовый кулонометр (электролизер 3 и другие кулонометры не включаются) и пропускают ток 50 мА в течение 5—10 мин. Электролиз ведут при открытом кране. Затем, поднимая уравнительную склянку, заполняют газовую бюретку раствором настолько, чтобы в ней оставалось примерно 1—2 мл газа. После этого закрывают кран, уровни растворов в бюретке и склянке приводят к одной и той же высоте и отсчитывают объем V1 оставшегося в бюретке газа. Очевидно, давление газа в бюретке при этих условиях будет равно атмосферному. Аналогично определяется объем V2 газовой смеси и по окончании основного опыта. Разность V2—V1 = V будет соответствовать объему гремучей смеси, выделившейся в кулонометре за время опыта.
Количество электричества определяют по формуле:
eF = 4/3(p-h)V/(RT) (22)
где р — внешнее давление, мм рт. ст.; h — давление насыщенного пара воды при температуре опыта, мм рт. ст. (см. Справочник, Р, табл. 21).
